利用 CRISPR-Cas9 技术让小鼠重见光明
2017-02-22 左丽媛 中国生物技术网
据估计,65 岁以上有十分之一的老年人患有这种症状,并且随着老龄化的加剧这种疾病将会越来越多。AMD 在白种人中很常见,它会导致视觉扭曲和盲点。韩国基础科学研究所 (IBS) 基因组工程中心的科学家报告,他们使用 CRISPR-Cas9 技术在活体小鼠的某个支持视网膜的组织层进行“基因手术”。该研究发表在《Genome Research》上,将基础研究和小鼠模型应用结合在一起。
据估计,65 岁以上有十分之一的老年人患有这种症状,并且随着老龄化的加剧这种疾病将会越来越多。AMD 在白种人中很常见,它会导致视觉扭曲和盲点。韩国基础科学研究所 (IBS) 基因组工程中心的科学家报告,他们使用 CRISPR-Cas9 技术在活体小鼠的某个支持视网膜的组织层进行“基因手术”。该研究发表在《Genome Research》上,将基础研究和小鼠模型应用结合在一起。
导致失明的最常见视网膜病变包括:早产儿视网膜病变、糖尿病视网膜病变和老年性黄斑变性。在这些疾病中,血管内皮生长因子 (VEGF) 的分泌达到了不正常的高水平。对于 AMD,VEGF 会导致眼睛中形成新血管,但也会导致血液和体液进入眼睛,破坏视网膜的中央区域,即黄斑受损。
注射抗 VEGF 药物是治疗 AMD 的最常见方法,但每年至少注射 7 次,因为病变的视网膜色素上皮细胞会持续分泌 VEGF。IBS 的科学家认为,CRISPR-Cas9 技术可以改善这种状况。基因组工程中心的负责人 KIM Jin-Soo 解释说:“注射只能是治标不治本。通过编辑 VEGF 基因,我们能够长期地治愈这种疾病。”
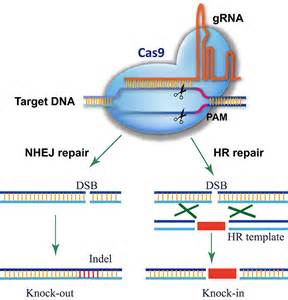
CRISPR-Cas9 能够在基因中的特定位置进行精准地剪切和修复。CRISPR-Cas9 系统的工作方式是在目标位置剪切 DNA,在这种情况下,就是对 VEGF 基因进行剪切。两年前,IBS 的科学家证明,一种预组装的 CRISPR-Cas9,或者说是 Cas9 核糖核蛋白(RNP),能够被导入到细胞和干细胞中对目标基因进行修改。这种预组装分子能够快速起效,而且可以在自身建立免疫反应之前就降解掉。尽管这种方法具有优势并且已经成功过,但是将预组装分子导入仍存在困难,这也就限制了它在治疗中的应用。
在研究中,研究团队成功地将 CRISPR-Cas9 注射到患湿性老年黄斑变性的小鼠眼中,并修改了 VEGF 基因。他们最初发现,注射法比用质粒导入更加有效。其次,这种化合物在 72 小时内就会降解消失。科学家检测了小鼠的基因组,发现 CRISPR-Cas9 分子只修改了 VEGF 基因,对其他基因没有影响。他们通过观察脉络膜新生血管 (CNV) 的方式监控眼部疾病进程,CNV 是视网膜和巩膜之间新形成的血管,它是湿性黄斑变性的常见问题,研究人员发现,CNV 区域减少了 58%。此外,锥体机能不良的副作用只持续了 3 天,在治疗后一个星期后没有再出现。
Kim Jin-Soo 说:“我们的方法通过关闭 VEGF 基因来抑制 CNV。我们预计在未来,外科医生可以利用这种方法对患者进行治疗。”
CRISPR-Cas9 过去常被用于修复导致遗传疾病和癌症的基因突变,这项研究提出了一种治疗非遗传退行性疾病的新方法。首尔国立大学的 KIM Jeong Hun 教授指出:“我们已经确认这种方法在动物模型中有效果,现在我们希望能够进行临床前试验。”
作者:左丽媛
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#CRISPR#
33
#CRISPR-Cas9#
41
#Cas9#
23
#CRISPR-Cas#
35
#Cas#
33