Science:CRISPR“直击”胚胎生长过程,下一步也许就是癌症!
2016-12-29 生物探索 生物探索
导读 发表在Science上的一项研究中,科学家们设计了一种在发育动物中标记和追踪细胞的新方法。在首次测试中,研究人员利用CRISPR技术揭示了一项惊人的发现,即成年斑马鱼中的许多组织和器官仅仅是从几个胚胎细胞形成的。5月26日,发表在Science上的一项研究中,哈佛大学的发育生物学家Alexander Schier和他的同事设计了一种在发育动物中标记和追踪细胞的新方法。在首次测试中,研究人
导读 发表在Science上的一项研究中,科学家们设计了一种在发育动物中标记和追踪细胞的新方法。在首次测试中,研究人员利用CRISPR技术揭示了一项惊人的发现,即成年斑马鱼中的许多组织和器官仅仅是从几个胚胎细胞形成的。
5月26日,发表在Science上的一项研究中,哈佛大学的发育生物学家Alexander Schier和他的同事设计了一种在发育动物中标记和追踪细胞的新方法。在首次测试中,研究人员利用CRISPR技术揭示了一项惊人的发现,即成年斑马鱼中的许多组织和器官仅仅是从几个胚胎细胞形成的。
Francis Crick研究所的发育生物学家James Briscoe说:“这是对CRISPR技术的一次创新性使用。”在CRISPR的一种原始用途中,模板DNA会告诉细胞如何修复双链缺口,但如果科学家不提供模板,细胞就无法精准修复断裂处,最终会留下“伤疤”,导致一些核苷酸缺失,或者添加“错误”的核苷酸。
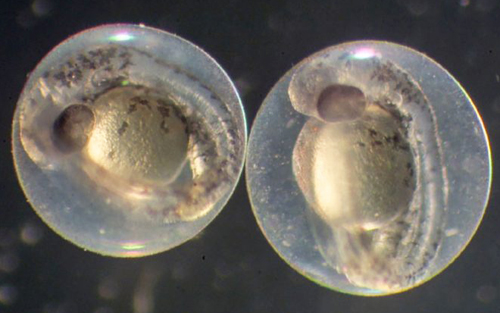
Three-day-old zebrafish embryos.
为了确保斑马鱼基因真的被删除,Schier通过引入多种不同的向导RNA靶向了多个位点。但是重复试验却带了截然不同的结果,包括删除部分的大小多种多样等。Schier及华盛顿大学的遗传学家Jay Shendure意识到,这种破坏的多样性可以被用于新的研究。
在斑马鱼胚胎基因组中,Schier和Shendure插入了一些额外的DNA,包括10种不同的CRISPR靶向序列。随后,他们向单细胞胚胎中注射了Cas9酶和10种与靶向序列匹配的向导RNA。随着胚胎的发育,CRISPR系统会反复的破坏和靶向每个细胞中的DNA,最终形成了一种独特的“条形码”。
当细胞分裂时,子细胞最初会拥有相同的“条形码”,但当Cas9作用于不同的位置时,就会产生差异。“条形码”的第一次变化似乎发生在胚胎变成两个细胞的阶段,随后基因编辑系统会在运行约4个小时后“耗尽力气”。当胚胎发育成成千上万个细胞后,留下来的“条形码”将随着细胞的继续增殖在成年动物细胞中出现。

A cellular family tree
四个月后,科学家们收集了成年斑马鱼的器官,从约20万个细胞中分离出一千多种不同的“条形码”。结果发现,大部分器官中超过一半的细胞共享着不到7个“条形码”。在除大脑外的所有器官中,25种不同的“条形码”组成了90%以上的细胞。Briscoe说:“组织可能是由比我预想的要小得多的一组细胞形成的。”
科学家们将这一新技术称为GESTALT(Genome Editing of Synthetic Target Arrays for Lineage Tracing),它有望帮助阐明单细胞最终发展成动物的过程;同时,GESTALT还有望揭示癌症研究中的重要问题,如多少前体细胞引发了肿瘤,扩散的癌症细胞如何与最初的肿瘤相关等。
然而,研究人员表示,这一技术也有它的缺点,例如它并没有可靠地标记每一代的细胞。但是,相比其它一些追踪细胞和它们后代的方法(如染色或依赖自然突变),借助CRISPR技术产生的“条形码”可能更有效,且容易使用。Schier说:“我认为,从概念上来讲,这是最令人兴奋的事情,你可以记录DNA的历史。”
其它相关研究
事实上,在这一文章发表前,研究人员已经提出了将CRISPR系统插入了细胞记忆中的其它方法。来自MIT的一个团队提出了一个叫mSCRIBE(mammalian Synthetic Cellular Recorder Integrating Biological Events)的系统。在这一研究中,科学家们向细胞中插入了单个CRISPR靶向序列,并改造位点使其能够编码向导RNA。随后,Cas9酶破坏DNA,导致序列突变,从而产生突变的向导RNA。突变的向导RNA再引导Cas9作用于靶向序列,如此循环下去。在这一过程中DNA序列和向导RNA在不断变化。
近阶段,“魔剪”CRISPR展示出了其多方位的应用实力。5月5日,发表在Science上的一项研究中,科学家们开发出了一项新技术,利用基因编辑系统CRISPR来快速鉴别基因变异。[详细]
另一方面,科学家们也逐渐认识到可以利用CRISPR技术来激活基因的表达;5月23日,Nature Methods杂志上发表了一项相关的结果,遗传学大牛George Church是该研究的通讯作者之一。
此外,5月25日,发表在Nature Communications上的一项研究中,纽约大学的研究团队基于CRISPR/Cas9系统开发了一个定向检测基因组区域的活体成像系统。该系统能够精确观测基因组位点和细胞核结构,揭示细胞核改变在基因表达调控和其它细胞过程中的重要作用。
原始出处:
作者:生物探索
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#下一步#
51
#CRISPR#
45
#胚胎#
33
#SCIE#
32