iNKT细胞通过分泌IFNγ抑制脂肪组织炎症,恢复肥胖个体血糖,缓解胰岛素抵抗!
2024-11-28 《基因启明》公众号 《基因启明》公众号
我国的成人糖尿病患病率居世界首位,其中约有41%的糖尿病患者为超重人群,24.3%的糖尿病患者为肥胖人群。
亮点
1、脂肪组织中的iNKT细胞能够产生免疫相关细胞因子,改善肥胖引发的炎症。
2、活化的iNKT细胞通过控制脂肪炎症进展,恢复肥胖小鼠的血糖,缓解胰岛素抵抗。
3、iNKT细胞以IFNγ依赖方式抑制脂肪组织炎症,从而“逆转”糖尿病。

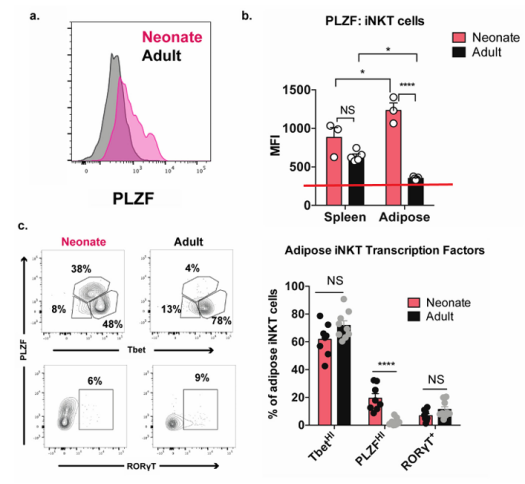
脂肪组织iNKT细胞随着“年龄”的增长而失去PLZF表达
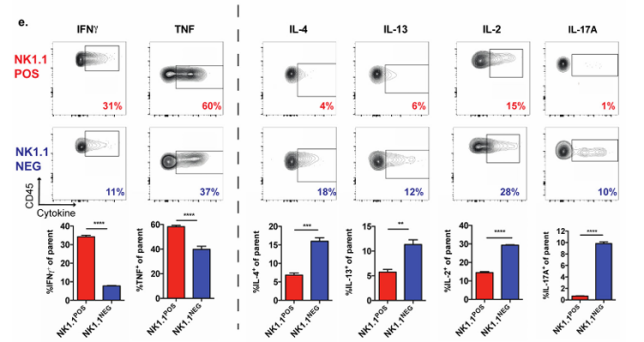
NK1.1产生保护性细胞因子
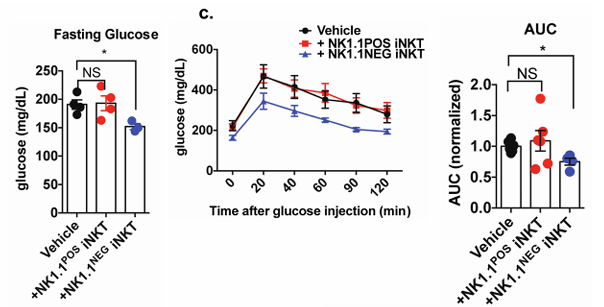
小鼠的血糖和葡糖糖耐量
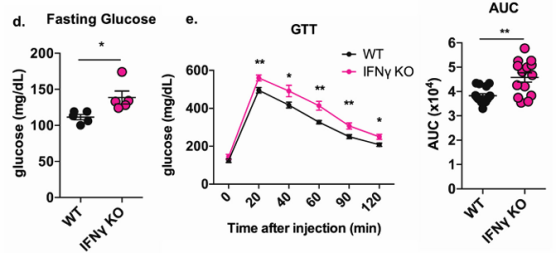
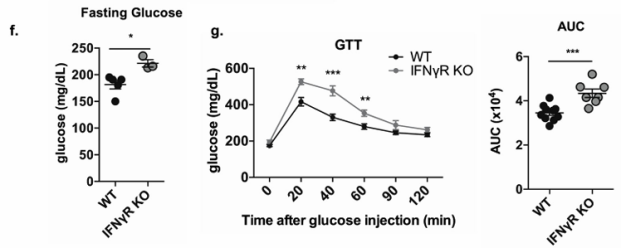
脂肪组织iNKT细胞产生的IFNγ改善胰岛素抵抗
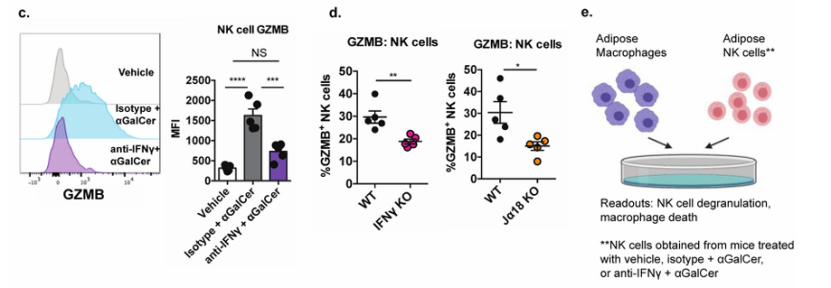
iNKT细胞来源的IFNγ允许NK细胞具有细胞毒性
来源:
微信公众号: 基因启明
参考文献:
LaMarche NM, Kane H, Kohlgruber AC, Dong H, Lynch L, Brenner MB. Distinct iNKT Cell Populations Use IFNγ or ER Stress-Induced IL-10 to Control Adipose Tissue Homeostasis. Cell Metab. 2020 Aug 4;32(2):243-258.e6. doi: 10.1016/j.cmet.2020.05.017. Epub 2020 Jun 8. PMID: 32516575; PMCID: PMC8234787.
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#糖尿病#
16