ACS术后又发心律失常,CCU主任是怎么做的?
2019-06-20 张静 中国医学论坛报今日循环
室性心律失常包括室性早搏(室早)、非持续性与持续性室性心动过速(室速)、心室扑动(室扑)与心室颤动(室颤)。
室性心律失常包括室性早搏(室早)、非持续性与持续性室性心动过速(室速)、心室扑动(室扑)与心室颤动(室颤)。
室性心律失常发生的病理因素包括心室肌肥厚、局部纤维化、室壁张力异常、交感兴奋性增高和电解质异常等。
虽然无结构性心脏病患者及离子通道病患者室性心律失常并非少见,但缺血性心脏病仍是室性心律失常的常见原因。
急性冠脉综合征(ACS)后患者心肌坏死,心肌电活动不稳定,极易出现室性心律失常[1],紧急开通闭塞的冠脉尤为重要。
冠脉血流再灌注可以大大降低ACS患者室性心律失常的发生,但术后持续发生的室性心律失常仍需要适当的药物治疗(抗心律失常药物)及非药物治疗(电复律、电除颤、起搏、导管消融、左心辅助装置)。
ACS患者术后
室性心律失常的药物治疗
ACS患者术后应用抗心律失常药物的原则
早期应用β受体阻滞剂可预防心律失常发作,减少ACS术后患者室速或室颤发生[2-3]。
电复律或电除颤可紧急终止ACS患者的室性心律失常,如果室速或室颤频繁发作,且不能被电复律或电除颤有效控制,可考虑应用胺碘酮治疗[4]。
如果β受体阻滞剂或碘酮无效,或者胺碘酮禁用,可以考虑应用盐酸尼非卡兰。尼非卡兰是一种新型的Ⅲ类抗心律失常药物,2014年该药在我国批准上市,用于其他药物无效或不能使用的情况下危及生命的室速、室颤。
也可以考虑静脉应用利多卡因,近期利多卡因在室速、室颤治疗中的临床地位得到了提升。室速、室颤时纠正低镁及低钾血症是有益的。
他汀类药物通过预防冠脉事件的反复发作,减少冠心病患者的死亡率, 因此推荐常规应用。
ACS患者术后室早的处理
ACS患者术后出现室早比较常见,其很少引起血流动力学紊乱,无需特殊治疗,持久或频繁的室早需要进一步血运重建[如再次血管造影和/或经皮冠脉介入治疗(PCI)][4]。
心肌梗死(心梗)手术后幸存的患者出现非持续性室速如无禁忌证推荐应用β受体阻滞剂;血流动力学相关的非持续性室速,可考虑给予胺碘酮治疗[4]。
ACS患者术后持续性室速或室颤的处理
尽管通过再灌注治疗,ST段抬高性心肌梗死患者住院死亡率下降,但心梗后短期内的死亡率仍受到关注。
ACS患者术后可因冠脉开通不彻底、急性缺血复发等引起反复持续性室速尤其是多形性室速或室颤,从而导致心梗后早期(10天内)心脏性猝死(SCD)事件的发生,立即行冠脉造影检查进行理想的血运重建、并进行合理的药物治疗(包括β受体阻滞剂、双联抗血小板及他汀治疗)、防治心衰是预防猝死的基石[5]。
对于ACS患者术后持续性室速或室颤的处理目前建议:
复发的多形室速易转变为室颤,β受体阻滞剂有效;
此外深度的镇静治疗可能减少室速或室颤发作;
应用胺碘酮可紧急抑制血流动力学相关的室性心律失常;
不推荐应用其他抗心律失常药物如普鲁卡因胺、普罗帕酮等(见表1)。
表1 急性冠脉综合征术后患者心脏性猝死的预防和处理
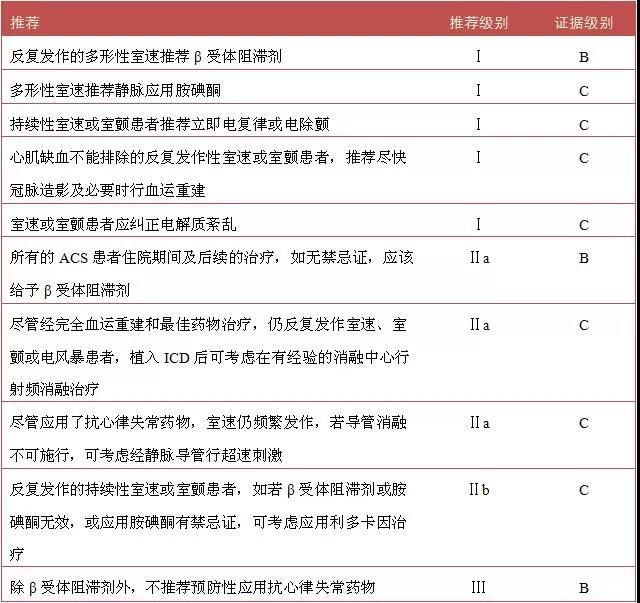
ACS患者术后
室性心律失常的非药物治疗
ACS患者术后心脏复律除颤器(ICD)的植入
持续性多形性室速/室颤的发生往往导致SCD的发生,对于不可逆原因所致的持续性多形性室速/室颤的主要治疗措施为应用ICD[6]。
当患者出现室性心律失常时,需对室性心律失常的类型(单形性、多形性、多源性室速或室颤)和室速的周长进行评估。
若ACS患者出现:
不完全血运重建;
室性心律失常出现在ACS发生48 h后;
或患者之前已存在左心功能损害,
等特殊情况时可考虑早期(<40天)植入ICD(见表2)。
对于有可能在短时间内再发持续性多形性室速/室颤但不适合植入ICD的患者,可考虑穿戴式心律转复除颤器治疗[6]。
表2 ACS后患者植入ICD适应症

ACS患者术后室速或室颤频繁发作者的射频消融处理
由缺血和/或再灌注心肌损伤引起的室早所触发的室速或室颤常常起源于部分受损的浦肯野氏纤维,导管消融非常有效,应该推荐[7],故对于经完全血运重建并经最佳药物治疗后的室速或室颤仍频繁发作者,可考虑植入ICD后行射频导管消融治疗。
几乎在所有病例均可从心内膜行基质消融。精确的导管标测和成功消融室速或室颤的触发灶是较复杂的,对手术技巧要求较高,因此建议手术应在有经验的导管消融中心进行[8]。
除此之外,ACS术后的几年内约1%~2%的患者常常在发生室速,在有经验的心脏中心导管消融可有效治疗反复发作的室速。但对于能耐受的持续性单型性室速、LVEF>40%且没有ICD支撑的患者,导管消融是否能获益尚值得进一步探索。
体外支持设备
如若上述推荐的治疗措施对反复发作的室速或室颤无效可考虑应用左室辅助装置或体外生命支持治疗以维持血流动力学稳定,如主动脉内球囊反搏(IABP)、体外膜肺氧合(ECMO)。
这样的干预通过增加冠脉灌注、减轻心脏做功、降低心肌氧耗可能为冠脉介入治疗赢得时间。尽管左室辅助装置可稳定患者的血流动力学,但室速或室颤的复发率高,干预治疗难度大[9]。
ACS术后常因心肌细胞坏死、冠脉开通不彻底、心梗再发等出现室性心律失常,恶性室性心律失常会引起SCD,合理应用心脏辅助装置及药物为患者的最优化治疗赢取时间,从而降低死亡率,提高生活质量。
作者:张静
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






利多卡因做过气管镜检查的都含过,麻醉喉头,大瓶的次一些,小瓶的只能住院病人找科里护士长拿药,每个人二瓶。CCU住院直接押金五千,不准陪护,定点探视,门外随时听候医生传唤,我妈紧急送医,害得我请假半月买饭侍奉,工作不幸被裁,孝子难当生活不易。
104
#ACS#
35