Tecentriq一线治疗转移性非小细胞肺癌,CHMP持积极意见
2021-03-27 Allan MedSci原创
它还将是首个也是唯一的具有三种给药方式的单剂癌症免疫疗法,允许每两周、三周或四周一次给药,使医生和患者可以灵活地管理治疗。
罗氏公司今天宣布,欧洲药品管理局(EMA)人用药品委员会(CHMP)已建议批准将Tecentriq®(atezolizumab)作为具有高PD-L1表达且无表皮生长因子受体(EGFR)或间变性淋巴瘤激酶(ALK)基因组肿瘤异常的转移性非小细胞肺癌(NSCLC)的一线疗法。根据该建议,预计欧洲委员会将很快对Tecentriq作出最终决定。
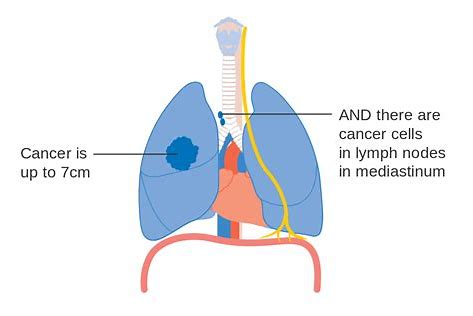
CHMP的建议是基于III期IMpower110研究的数据,该研究表明,与化学疗法相比,Tecentriq单一疗法可将总生存期(OS)提高7.1个月(20.2个月 vs. 13.1个月)。Tecentriq的安全性似乎与其已知的安全性一致,并且没有新的安全性信号。据报告,在接受Tecentriq的患者中,3-4级与治疗相关的不良事件发生率为12.9%,而接受化疗的患者为44.1%。
罗氏首席医学官Levi Garraway博士说:“我们仍然致力于提供有效和量身定制的肺癌治疗方案,这一宣布是朝着这一目标迈出的重要一步”。
如果获得批准,Tecentriq将提供一种新的治疗选择,而不会出现与化学疗法相关的不良反应。它还将是首个也是唯一的具有三种给药方式的单剂癌症免疫疗法,允许每两周、三周或四周一次给药,使医生和患者可以灵活地管理治疗。
原始出处:
作者:Allan
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#非小细胞#
58
#TEC#
63
Tecentriq单一疗法
100
#CHMP#
84
#转移性#
60