磁性纳米颗粒,最新Nature系列综述,精确热疗!
2024-11-10 BioMed科技 BioMed科技
在这篇综述中,约翰霍普金斯大学Jeff W. M. Bulte等人探讨了磁性纳米粒子介导的成像技术与磁流体热疗相结合的潜在用途,即选择性和精确地加热肿瘤位置,同时避免对周围健康组织的损伤。
磁性纳米粒子与诊疗
磁性纳米粒子,包括由超顺磁性氧化铁(SPIO)形成的纳米粒子,被用于各种磁成像和治疗技术。基于检测体内磁性纳米粒子的体内成像技术包括磁共振成像(MRI)、磁性粒子成像(MPI)、磁动超声(MMUS)和磁光声成像(MPAI)。临床前数据表明,通过监测从相同磁性纳米颗粒采集的成像数据,可以在治疗过程中动态调节加热磁性纳米颗粒所需的条件,包括能量考虑、颗粒修饰、定位和暴露时间。
自20世纪80年代中期以来,各种磁性纳米粒子制剂已被用作临床或临床前药物,用于诱导磁流体热疗(MFH),并与各种磁成像技术结合使用。因此,成像引导的MFH可以被认为是一种有前景的非侵入性技术,可用于同时识别和消除肿瘤细胞。这种综合方法比传统的MFH具有显著的优势,包括减少不良反应和提高治疗效果。事实上,使用磁性纳米颗粒的成像引导精确热疗系统有望改变癌症治疗方法。
最新综述
在这篇综述中,约翰霍普金斯大学Jeff W. M. Bulte等人探讨了磁性纳米粒子介导的成像技术与磁流体热疗相结合的潜在用途,即选择性和精确地加热肿瘤位置,同时避免对周围健康组织的损伤。成像引导的MFH可以根据肿瘤和邻近器官内磁性纳米颗粒的生物分布信息以及热剂量的体积分布提供个性化的治疗计划。还讨论了MFH磁成像技术临床转化的要求——开发具有良好生物安全性、最佳磁加热性能和最大磁成像信号的磁性纳米粒子制剂;以及将磁成像和加热硬件集成到单个平台中。相关综述以“Imaging-guided precision hyperthermia with magnetic nanoparticles”为题发表在Nature Reviews Bioengineering。

【文章要点】
一、高温热疗
一旦积聚在肿瘤内,纳米粒子很容易从外部施加的来源吸收能量,并将这种能量传递给肿瘤细胞,从而造成热损伤。使用交变磁场(AMF)局部升高体内靶位点的温度是磁性纳米粒子介导肿瘤加热的一种方法。这一过程称为高温热疗(Hyperthermia),可将靶组织的温度升高至破坏性(热消融)水平(>47°C)或保存活性(热致敏)水平(41-45°C),使癌症细胞更容易受到放射治疗和/或化学治疗的影响。与正常细胞相比,癌症细胞适应温度升高的能力较弱。因此,与经受相同温度升高的健康细胞相比,肿瘤细胞中蛋白质折叠、酶活性、细胞生长和细胞分化的损伤都更为突出。然而,使用AMF来升高肿瘤的温度需要仔细评估安全性。外周神经的热刺激会引起不适或不自主的肌肉收缩,涡流的感应会导致局部发热和不希望的组织损伤。通过优化AMF参数、实施实时监测和改进磁性纳米粒子的设计,可以减轻这些风险。基于纳米颗粒的治疗范式面临的其他主要挑战是,当静脉注射时,只有一小部分纳米颗粒被输送到肿瘤部位,主要是因为纳米颗粒在网状内皮系统中的隔离和肿瘤内输送的内在(血管)屏障。纳米颗粒的低肿瘤摄取阻碍了磁性纳米颗粒介导的热疗的临床转化。使用成像引导的能量输送方法和改进的将磁性纳米颗粒靶向肿瘤的方法,例如通过与癌症细胞上过表达的叶酸受体结合,可以帮助提高热疗程序的准确性和癌症选择性(图1)。
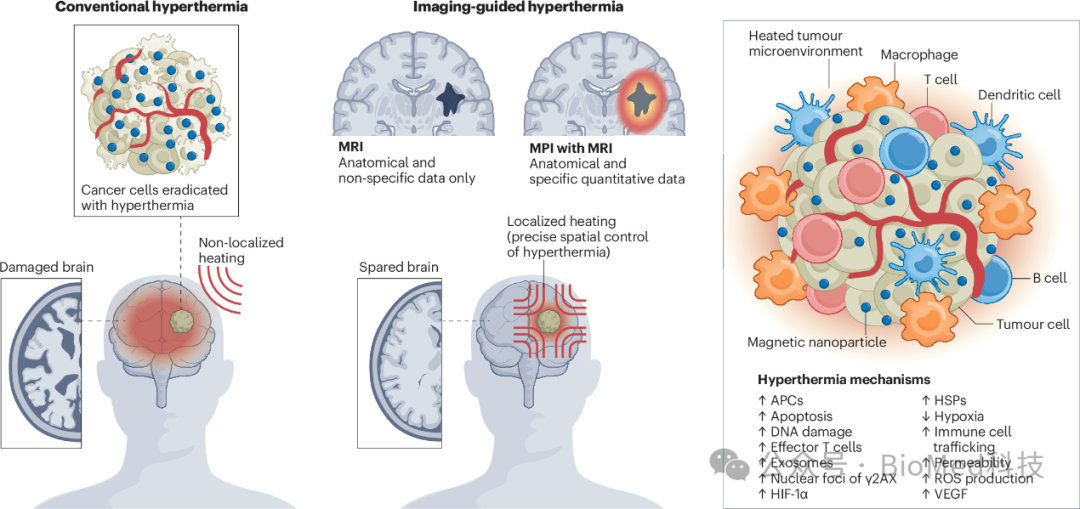
图1 精确成像引导热疗治疗实体肿瘤
二、磁流体热疗
MFH是最常见的热疗方式,其中磁性纳米粒子在AMF存在的情况下产生热量。磁性纳米颗粒有效地将AMF能量转化为热量,从而导致负载这些纳米颗粒的癌症细胞的温度升高。MFH手术中使用的电磁波位于低射频范围(约100 kHz至1 MHz),这被认为是安全的,可以到达人体内任何深度的肿瘤。此外,该频率范围降低了神经刺激等不良反应的风险,这使得这种方法适用于临床应用。在该范围内调整激发频率以匹配磁性纳米粒子的自然共振,从而最大限度地提高加热响应。场强的增加进一步提高了肿瘤温度,并可能缩短治疗时间;因此,操纵磁场强度(通常从0kA m-1变化到18kA m-1(对应于高达22.7mT的磁通密度)对于将MFH期间的温度升高保持在安全范围内也至关重要(图2)。
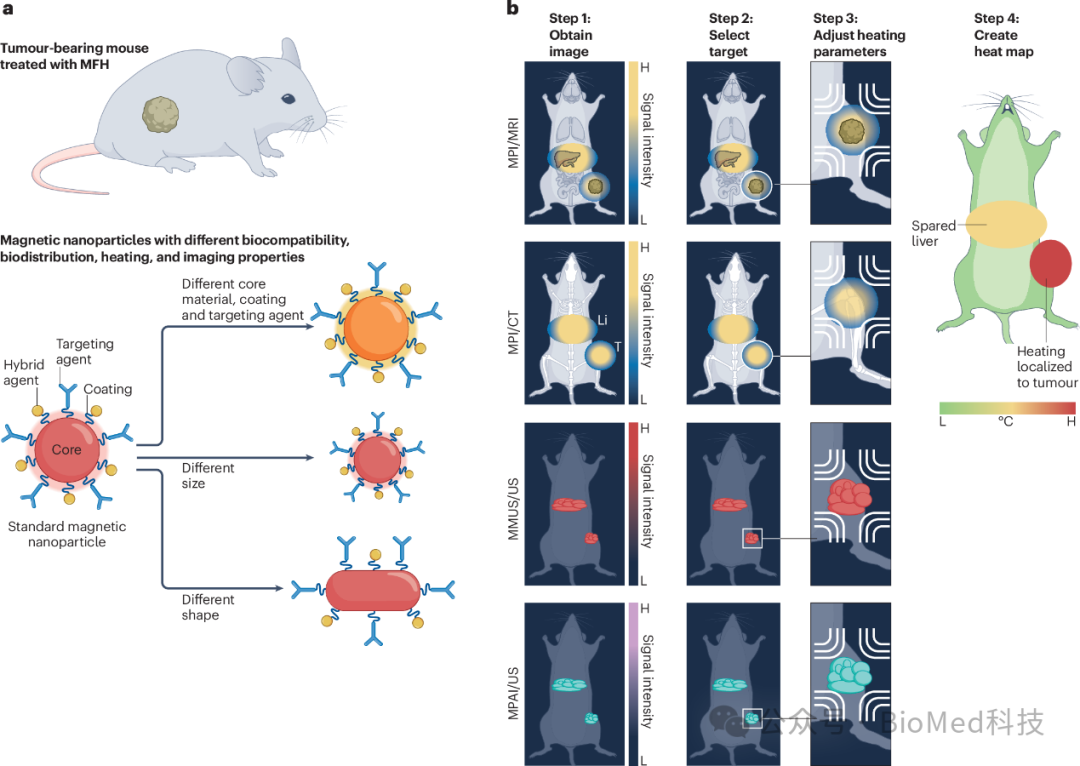
图2 磁流体热疗的应用
三、SPIO纳米粒子
SPIO纳米粒子具有超顺磁性,这一特性描述了在外部磁场下具有单个磁畴的小铁磁或亚铁磁粒子的独特行为,在这种情况下,它们表现出暂时的磁性,没有永久的偶极矩。这一特性使SPIO纳米粒子能够有效地将外部磁场的能量转化为热量,同时确保它们在应用后不会保持磁化或相互作用,从而防止SPIO纳米粒子的自发聚集。纳米粒子聚集与稳定性降低、超顺磁性丧失、生物利用度降低、细胞摄取受损、药代动力学改变、潜在毒性作用以及治疗和诊断实用性降低有关。SPIO纳米粒子的优异稳定性和分散性使其成为精确、可控热疗和磁成像应用的理想选择。SPIO纳米粒子可以通过物理或化学方法合成。尽管物理方法可以产生大量(批量合成),但它们会导致纳米粒子均匀性差。化学方法的产率低于物理方法,但可以提高纳米粒子的均匀性和分散性。理想的SPIO磁性纳米粒子满足以下条件:可重复的批量合成;长期胶体稳定性,磁性不变;生物相容性;以及促进配体偶联以进行官能化和靶向的表面。符合这些标准的SPIO磁性纳米粒子是具有无机和有机结构域的混合结构。有机域是通过纳米颗粒外表面的工程设计创建的。最流行的表面工程方法包括:用(优选两亲性)聚合物涂覆外表面,如葡聚糖、树枝状聚合物(即小树枝状聚合物)或脂质;将SPIO纳米颗粒包封在有机涂层内;以及通过配体交换稳定SPIO。此外,纳米粒子核尺寸是超顺磁性行为的重要因素,因为饱和磁化值随着纳米粒子尺寸的增加而增加。
四、成像引导的精确热疗
多功能磁性纳米颗粒,包括SPIO纳米颗粒,是成像引导癌症治疗的理想候选物,因为它们既可以显示非造影扫描不可见的肿瘤,又可以提供MFH治疗。目前,超声、CT和MRI通常用于在热疗过程中引导射频消融探头并评估这种治疗的结果。在不断发展的医学成像领域,热疗指导可以通过许多其他方式提供,尽管一些选择尚未显示出足够的转化潜力。例如,将磁动光学相干断层扫描(MM-OCT)引入临床实践可能有助于指导热疗。MM-OCT是一种高分辨率技术,既可以对肿瘤的微观结构进行成像,又可以实时揭示组织对热疗的反应。将MM-OCT功能纳入手持或基于导管的设备平台可以实现热剂量的原位评估,这将通过提供高温生理效应的即时反馈来补充现有的成像技术,从而提高MFH治疗的精度和效率(图3)。
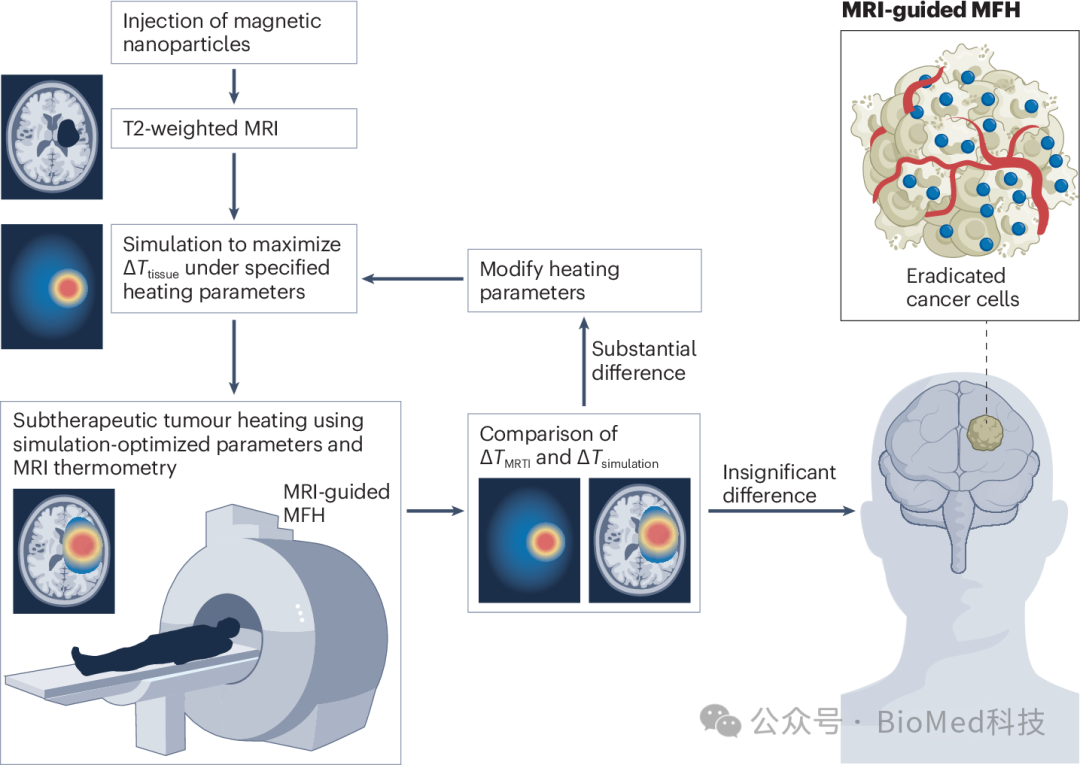
图3 成像引导磁流体热疗的工作流程
结论与展望
作者最后指出,将磁成像和MFH系统集成到一个统一的平台中,需要创新的设备工程来融合这两种有前景的技术,这是一个对未来充满希望的挑战。例如,开发混合MRI和MPI引导的MFH系统可以利用MRI的优势提供空间信息,利用MPI提供磁性纳米粒子的精确量化。鉴于肿瘤内磁性纳米颗粒分布中不可避免的异质性,这种多模态方法有望动态调节向含有磁性纳米颗粒的肿瘤输送的外部能量。
原文链接:
https://www.nature.com/articles/s44222-024-00257-3
作者:BioMed科技
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#肿瘤# #磁性纳米颗粒#
6