FDA批准oteseconazole(奥特康唑)用于复发性外阴阴道假丝酵母菌病治疗
2022-04-29 MedSci原创 MedSci原创
日前,FDA已批准Mycovia Pharmaceuticals公司开发的口服抗真菌药物Vivjoa(oteseconazole,中文名奥特康唑),用于在不具有生殖潜力的女性中,降低复发性外阴阴道假丝
日前,FDA已批准Mycovia Pharmaceuticals公司开发的口服抗真菌药物Vivjoa(oteseconazole,中文名奥特康唑),用于在不具有生殖潜力的女性中,降低复发性外阴阴道假丝酵母菌病(RVVC)的复发几率。此前,Mycovia在新闻稿中指出,如果获批,oteseconazole将成为FDA批准的第一个治疗RVVC的药物。该药去年7月份提交FDA优先审查。
值得一提的是,恒瑞医药从Mycovia Pharmaceuticals公司引进这款新型抗真菌药。今年1月,恒瑞医药已在中国提交了它的新药上市申请。
Oteseconazole (VT-1161) 是一种有效、可口服的抗真菌剂,有效结合并抑制白色念球菌的 CYP51 (Kd,<39 nM),但对人 CYP51 无明显作用。

图片来源:FDA官网
RVVC也被称为慢性酵母感染,是一种不同于外阴阴道念珠菌病(VVC)的疾病,定义为每年三次或三次以上有症状的酵母感染急性发作,主要症状包括阴道瘙痒、灼热、刺激和炎症。一些女性可能会经历异常阴道分泌物、性交疼痛或排尿疼痛,引起各种但往往是严重的不适和疼痛。RVVC是一种慢性传染病,每年影响全球近1.38亿女性,仅美国就有600万女性,中国约有2900万RVVC 患者。目前,针对RVVC还没有获批的治疗方法。
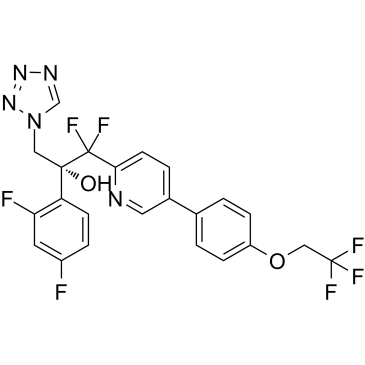
oteseconazole(VT-1161)化学结构式(图片来源:medchemexpress.com)
oteseconazole 批准上市基于3项3期的临床试验阳性结果:2项全球VIOLET研究、1项美国ultraVIOLET研究,包括11个国家232个临床地点的870多名患者。这2项VIOLET研究都达到了主要和关键次要终点。在为期48周的试验中,超过90%的患者接受oteseconazole治疗后能够有效预防感染复发(p<0.001)。此外,ultraVIOLET研究的结果证实了oteseconazole治疗VVC初始发作的有效性,并与当前VVC标准护理药物氟康唑(fluconazole)相比,加强了其治疗RVVC的有效性和安全性。汇总的3期数据显示,oteseconazole在近一年内保护了90%以上的患者免于复发。
此外,ultraVIOLET试验也达到其所有主要终点与关键次要终点。试验结果表明,oteseconazole治疗VVC初始发作有效,并与目前标准治疗相比,进一步证明了其治疗RVVC的疗效和安全性。到50周时,治疗组复发率为5.1%,对照组为42.2%(p<0.001)。并且,oteseconazole可保护95%的受试者近一年不复发。
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言




#ConA#
91
#AZ#
90
#FDA批准#
87
#复发性#
94