南方医科大学陈天宇/邹志鹏/黄彬/梁文全《自然·通讯》:揭示了调控早期骨关节炎软骨下骨破骨细胞活化的负反馈回路
2024-10-15 BioMed科技 BioMed科技
该研究揭示了一个新的调控破骨细胞分化的负反馈回路:RANKL-UCHL1-sCD13,靶向这一回路可以抑制骨关节炎中软骨下骨的异常重塑,进而阻止骨关节炎的进展。
骨关节炎(OA)早期的主要病理特征是软骨下骨破骨细胞异常活化导致的骨吸收增加。然而,这一过程中破骨细胞活化的机制仍不清楚。
2024年10月10日,南方医科大学陈天宇、邹志鹏、黄彬、梁文全共同通讯在Nature Communications 在线发表题为“A RANKL-UCHL1-sCD13 negative feedback loop limits osteoclastogenesis in subchondral bone to prevent osteoarthritis progression”的研究论文,该研究揭示了一个新的调控破骨细胞分化的负反馈回路:RANKL-UCHL1-sCD13,靶向这一回路可以抑制骨关节炎中软骨下骨的异常重塑,进而阻止骨关节炎的进展。
该研究分析了正常人和OA患者的软骨下骨样本,发现去泛素化酶UCHL1在OA患者的软骨下骨破骨细胞中表达上调。重要的是,在OA患者和小鼠模型中,UCHL1的表达与OA进展期间的破骨细胞活性之间存在强烈的关联。破骨前体细胞UCHL1的条件性敲除加剧DMM诱导的骨关节炎进展,而通过AAV9介导的UCHL1过表达则能缓解这一过程。机制上,该研究发现了一个先前未知的负反馈回路,即RANKL-UCHL1-sCD13,RANKL刺激破骨细胞前体中UCHL1的表达,随后UCHL1稳定CD13蛋白并增加可溶性CD13(sCD13)的释放,触发对MAPK途径的自分泌抑制效应,从而抑制破骨细胞的形成。
总之,这些发现揭示了一个先前未知的负反馈环路,即RANKL-UCHL1-sCD13,该环路不仅调控破骨细胞的形成,还为OA提供了一种潜在的治疗靶点。

骨关节炎是一种常见的致残性疾病,全球约有3亿人受到影响。然而,目前尚缺乏有效的治疗方法或干预措施来阻止骨关节炎的进展。随着全球人口老龄化趋势的加剧和肥胖率的上升,该病所带来的社会和家庭负担将日益加重。因此,迫切需要开发有效的骨关节炎治疗方法。
目前,骨关节炎被认为是一种全关节疾病,其主要病理特征包括关节软骨的退变、软骨下骨的异常重塑、骨赘的形成以及滑膜的炎症。越来越多的研究表明,软骨下骨的异常重塑往往先于软骨本身的退变,并且这种异常重塑被认为是引发关节软骨退变的关键触发因素。软骨下骨异常重塑导致上覆软骨承受的机械应力发生变化,进而促进了软骨的退变和OA的进展。破骨细胞是人体唯一的骨吸收细胞,其过度激活别认为是造成OA早期软骨下骨异常重塑的主要原因。
破骨细胞由单核细胞/巨噬细胞谱系的前体细胞融合而成。RANKL作用于单核/巨噬细胞表面的RANK受体,激活下游MAPK和NF-kB信号通路,从而启动破骨细胞分化和骨吸收功能。不过,关于破骨细胞在软骨下骨中异常活化的具体机制仍有待阐明。
在生物学中,负反馈回路是一种重要的自我调节机制,对于维护机体的稳态至关重要。这种机制通过抑制或减弱初始变化的方向来保持系统的平衡,有助于防止过度反应。然而,软骨下骨破骨细胞过度活化的负反馈机制还未见报道,强化这一机制可能是抑制破骨细胞异常活化的一种潜在策略。
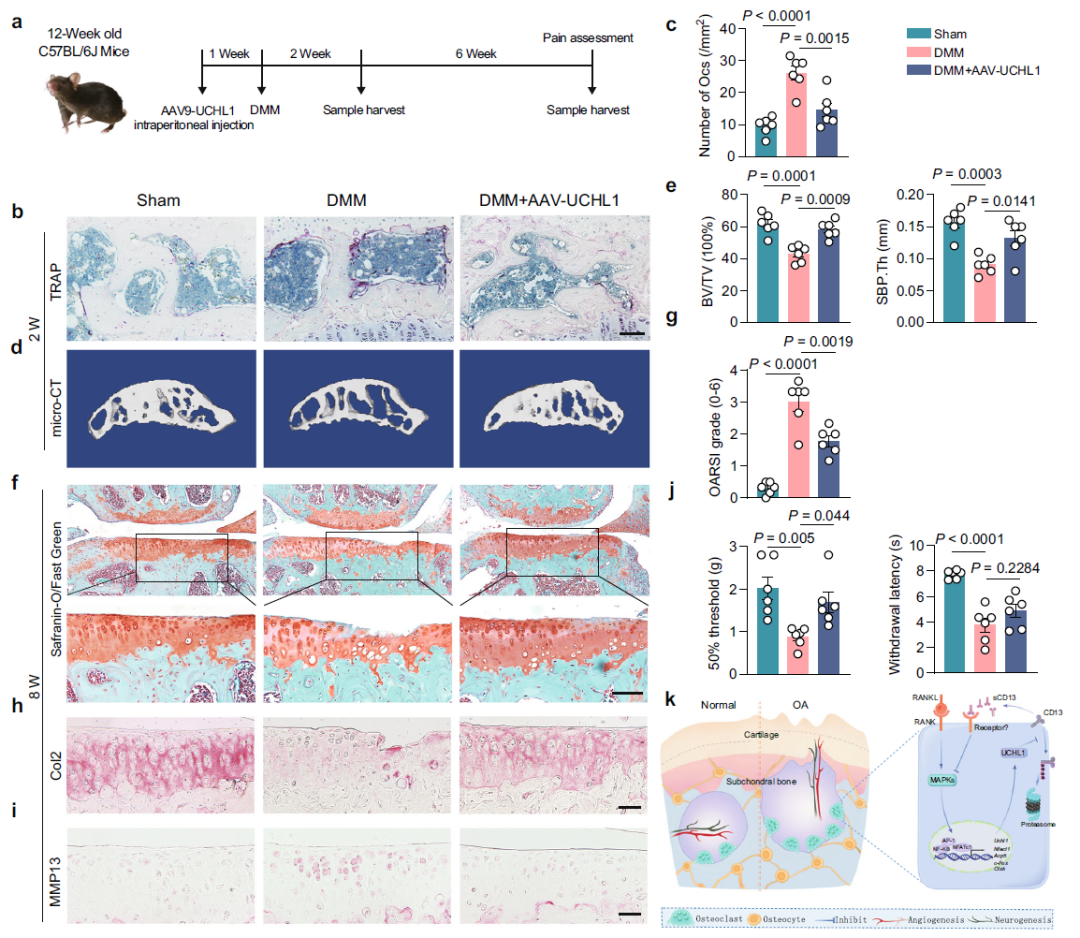
靶向RANKL-UCHL1-sCD13负反馈轴抑制软骨下骨破骨细胞活化缓解OA进展(图源自Nature Communications )
在此背景下,本研究揭示了一个先前未知的调控破骨细胞分化的负反馈回路:RANKL-UCHL1-sCD13。在正常情况下,该环路有助于维持破骨细胞的内稳态;但在OA患者中,尽管该负反馈机制有所增强,但仍不足以抵抗OA发展的始动因素。然而,通过AAV过表达UCHL1来进一步增强这一负反馈环路,则可抑制软骨下骨破骨细胞的分化,从而减缓骨关节炎的进展。因此,靶向调控RANKL-UCHL1-sCD13负反馈轴,可能为OA提供了一条新的治疗途径。
原文链接:
https://doi.org/10.1038/s41467-024-53119-2
作者:BioMed科技
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#足踝外科#。。。
2
#骨关节炎# #软骨下骨#
58