Nat Commun:CD318、TSPAN8和CD66c为胰腺癌CAR-T细胞疗法的候选靶标
2021-03-11 xiaozeng MedSci原创
胰腺癌是西方国家中癌症相关死亡的第四大主要原因。
胰腺癌是西方国家中癌症相关死亡的第四大主要原因。目前,手术治疗仍是唯一可能治愈的方法,且只有大约20%的患者在诊断时表现出可进行手术切除的疾病阶段。因此,新型的治疗策略的研究迫在眉睫。
一种新的具有潜力的治疗方法是CAR(嵌合抗原受体)-T细胞疗法,且在治疗B细胞恶性肿瘤中显示出空前的疗效。该疗法通常依赖于泛B细胞抗原,如CD19或CD20,且无法区分健康细胞和肿瘤细胞。其会导致所有B细胞均被消耗,且迄今为止仍然是实体瘤CAR-T细胞疗法的主要问题之一。
针对胰腺导管癌(PDAC)有效的细胞免疫治疗的一个主要障碍是缺乏合适的肿瘤特异性抗原。为了应对这一挑战,研究人员旨在提出一种用于CAR-T靶点治疗的系统方法。
PDAC的候选CAR靶标
在该研究中,研究人员结合流式细胞术筛选、生物信息表达分析和免疫荧光等实验。研究人员鉴定了CLA、CD66c、CD318和TSPAN8为371种抗原中的四种靶候选物,并产生了32种对这些分子特异型的CAR。
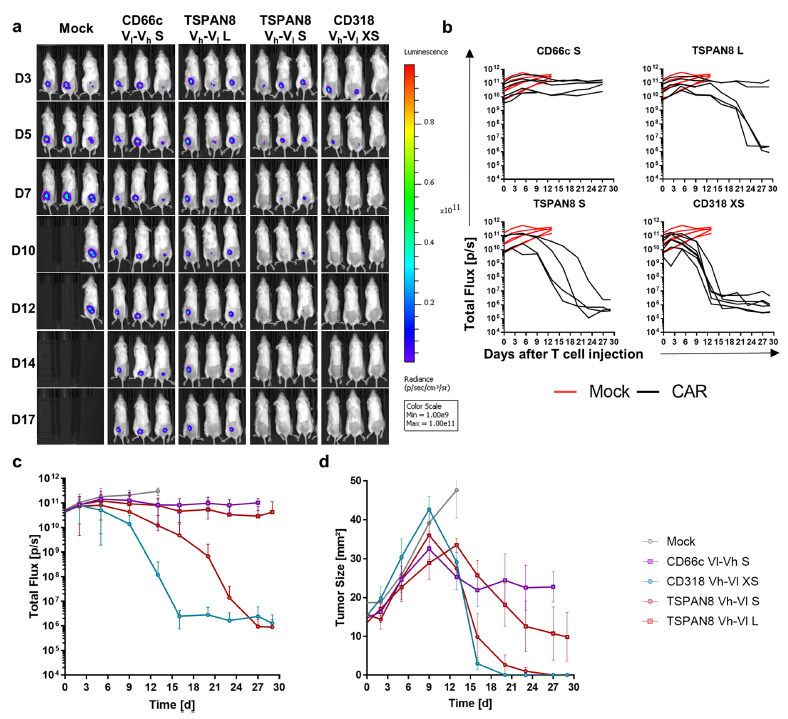
移植瘤模型中评估CAR-T细胞的在体功能
基于靶细胞裂解、T细胞活化和细胞因子释放,研究人员评估了CAR-T细胞的活性。在CD66c、CD318和TSPAN8特异性的CAR-T细胞中,CD318表现出了从疾病稳定到彻底根除肿瘤的功效,其次是TSPAN8,基于功能性和预测的安全性,其是最有希望的潜在的候选靶标。
总而言之,这项研究揭示了基于CAR-T细胞的PDAC免疫疗法的潜在候选靶标,以及针对这些分子的功能性CAR构建体。
原始出处:
Schäfer, D., Tomiuk, S., Küster, L.N. et al. Identification of CD318, TSPAN8 and CD66c as target candidates for CAR T cell based immunotherapy of pancreatic adenocarcinoma. Nat Commun 12, 1453 (05 March 2021).
作者:xiaozeng
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#SpA#
52
#Nat#
43
#CD31#
40
#COMMUN#
40
#CAR-#
45