2024v1版NCCN非小细胞肺癌指南更新,EGFR突变和ROS1重排新增治疗推荐
2024-01-19 苏州绘真医学 苏州绘真医学
近日,美国国家综合癌症网络(NCCN)更新了 2024 年非小细胞肺癌(NSCLC)临床实践指南。指南基于分子和生物标志物,针对晚期或转移性疾病系统治疗新增了 5 项治疗推荐。

▲2024v1版NCCN非小细胞肺癌临床实践指南
近日,美国国家综合癌症网络(NCCN)更新了 2024 年非小细胞肺癌(NSCLC)临床实践指南。指南基于分子和生物标志物,针对晚期或转移性疾病系统治疗新增了 5 项治疗推荐:①EGFR 19Del和21号外显子L858R突变一线治疗中新增了奥希替尼+培美曲塞+(顺铂或卡铂)方案(非鳞癌);②EGFR 20号外显子插入突变一线治疗新增了埃万妥单抗(Amivantamab-vmjw)+卡铂+培美曲塞方案(非鳞癌);③携带EGFR 19Del或21号外显子L858R突变的患者如果在奥希替尼治疗后出现疾病进展,后续治疗可使用埃万妥单抗+卡铂+培美曲塞(非鳞癌);④ROS1重排一线治疗新增瑞普替尼;⑤携带ROS1重排的患者在接受恩曲替尼、克唑替尼、瑞普替尼或塞瑞替尼治疗后出现疾病进展,后续治疗可选择瑞普替尼。

▲2024v1版指南新增EGFR突变和ROS1重排治疗推荐(NSCL-J)

▲2023v4版指南,以供比较

▲EGFR 19Del和21号外显子L858R突变一线治疗新增奥希替尼+培美曲塞+(顺铂或卡铂)(NSCL-21)
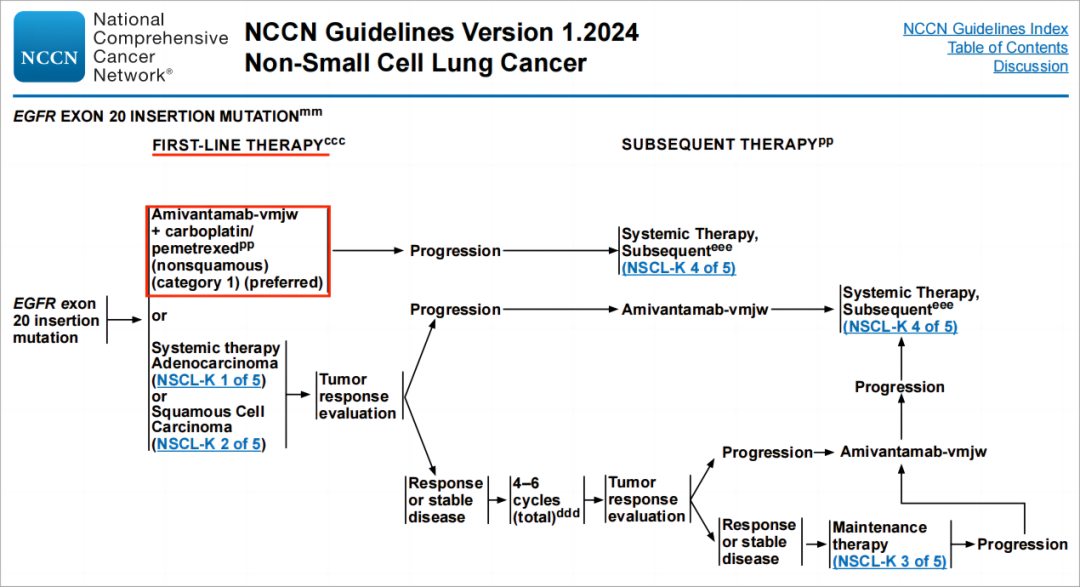
▲EGFR 20号外显子插入突变一线治疗新增埃万妥单抗+卡铂/培美曲塞(NSCL-25)

▲携带EGFR 19Del或21号外显子L858R突变的患者经奥希替尼治疗后出现疾病进展,后续治疗可使用埃万妥单抗+卡铂+培美曲塞(NSCL-22)

▲ROS1重排一线治疗新增瑞普替尼

▲携带ROS1重排患者在接受恩曲替尼、克唑替尼、瑞普替尼或塞瑞替尼治疗后进展,后线治疗可选用瑞普替尼
以上五项更新分别得到了FLAURA2研究(更新①)、PAPILLON研究(更新②)、MARIPOSA-2研究(更新③)和TRIDENT-1研究(更新④⑤)数据的支持。
EGFR突变
FLAURA2研究
研究设计
FLAURA2是一项全球III期、开放标签、随机研究,旨在评估奥希替尼联合铂-培美曲塞化疗与奥希替尼单药作为EGFRm晚期NSCLC一线治疗的疗效和安全性。
入组患者应符合如下标准:年龄≥18岁(日本≥20岁),诊断为病理证实的非鳞状局部晚期/转移性NSCLC,携带ex19del/L858R突变;WHO PS 0-1,未接受过晚期NSCLC的系统性/EGFR-TKI治疗;稳定的中枢神经系统转移患者可以入组,且至少 2 周不需要类固醇治疗。

▲研究设计
符合条件的患者(N=557)以 1:1 的比例随机分配至奥希替尼联合化疗组(奥希替尼80 mg每日一次+培美曲塞500 mg/㎡+顺铂75 mg/㎡或卡铂AUC5,共 4 个周期,随后每 3 周接受奥希替尼80 mg QD+培美曲塞500 mg/㎡维持治疗)或奥希替尼单药治疗组(80 mg QD),直至出现疾病进展/达到停药标准;患者按种族(中国人/非中国亚洲人/非亚洲人)、EGFRm检测方法(本地实验室/中心实验室)和WHO PS(0/1)分层。主要终点是研究者根据RECIST v1.1标准评估的PFS。其它关键次要终点包括:OS、PFS2、客观缓解率(ORR)、健康相关生活质量(QoL)、CNS PFS和基于CTCAE v5版标准评估的安全性。
研究结果
截止 2023 年 4 月 3 日,在联合化疗组和单药组中,研究者评估的中位PFS分别为 25.5 个月和 16.7 个月(中位随访时间分别为 19.5 个月和 16.5 个月),HR为 0.62,95%CI:0.49-0.79,P<0.0001,有显著的统计学差异,达到了主要研究终点。在联合化疗组和单药组中,BICR评估的中位PFS为 29.4 个月和 19.9 个月(中位随访时间分别为 19.4 个月和 14.6 个月),HR为0.62,95% CI:0.48-0.80,P=0.0002,也存在显著的统计学差异。
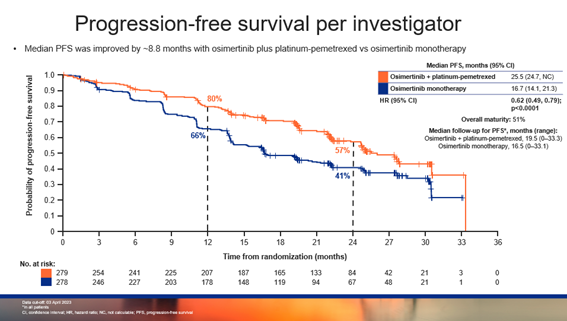
▲研究者评估的PFS
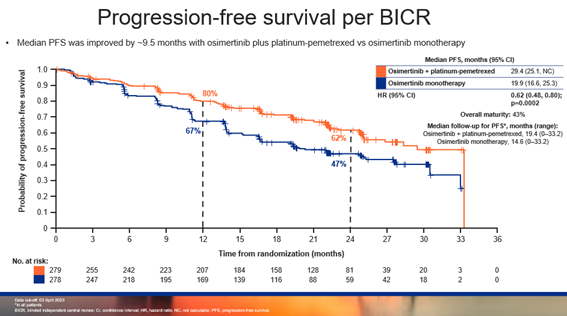
▲BICR评估的PFS
亚组分析结果显示,在所有亚组中具有一致的PFS获益。在基因突变亚组中,EGFR ex19del患者在两组中的中位PFS分别为 27.9 个月和 19.4 个月(HR = 0.60),L858R患者在两组中的中位PFS分别为 24.7 个月和 13.9 个月(HR = 0.63),联合治疗提高了L858R患者约 11 个月的中位PFS,获益程度接近ex19del亚组。
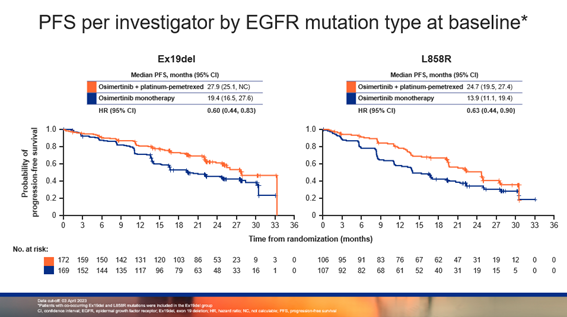
▲基于EGFR突变亚型的PFS
在脑转移亚组中,奥希替尼联合化疗相较于奥希替尼单药可提升脑转移患者的中位PFS约 11 个月(24.9 个月 vs 13.8 个月),降低疾病进展或死亡风险 53%(HR = 0.47);在基线无脑转移亚组中,奥希替尼联合化疗组的中位PFS更长,达到 27.6 个月(vs 21.0个月;HR = 0.75)。此外,在亚裔中国人群中,PFS获益趋势明显,降低疾病进展或死亡风险 51%(HR = 0.49)。
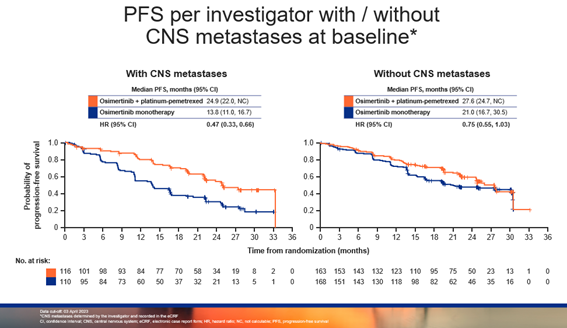
▲研究者根据基线有无脑转移评估的PFS
在疗效应答方面,奥希替尼联合化疗组的客观缓解率(ORR)高达 83%,相比当前标准治疗(SoC)奥希替尼单药(76%)有明显提升,中位缓解持续时间(DoR)也表现优异。在数据截止时,PFS2和OS尚未成熟,奥希替尼联合化疗组与奥希替尼单药组的PFS2分别为 30.6 个月 vs 27.8 个月(HR=0.70;P=0.0132),中位OS暂未达到(HR=0.90;P=0.5238)。
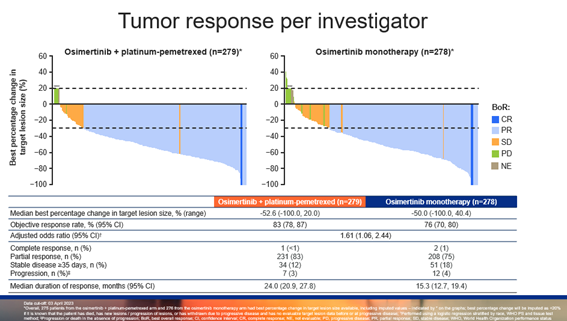
▲研究者评估的肿瘤缓解情况
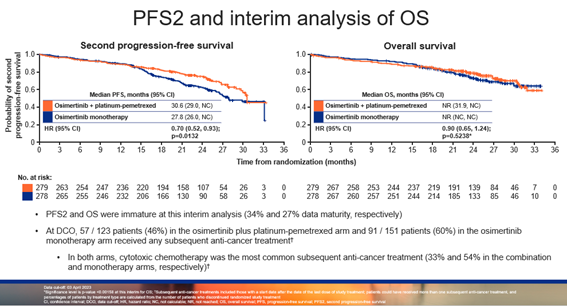
▲中期分析时的PFS2和OS数据(均未成熟)
PAPILLON研究
研究设计
PAPILLON是一项随机、开放标签、III期临床研究,评估埃万妥单抗(Amivantamab-vmjw)联合化疗与单独化疗在未经治疗的EGFR外显子20插入突变晚期或转移性NSCLC患者中的疗效和安全性。符合入组条件的患者必须有组织学或细胞学证实的局部晚期或转移性非鳞状NSCLC,并有记录确认为原发性EGFR 20号外显子插入激活突变;有可测量的病灶(基于RECIST v1.1标准);ECOG体力评分为 0-1。PAPILLON试验纳入的 308 名患者中大多数是女性,超过一半是亚洲人,23% 有脑转移病史。中位随访时间为 14.9 个月。研究的主要终点是盲法独立审查中心评估的PFS。
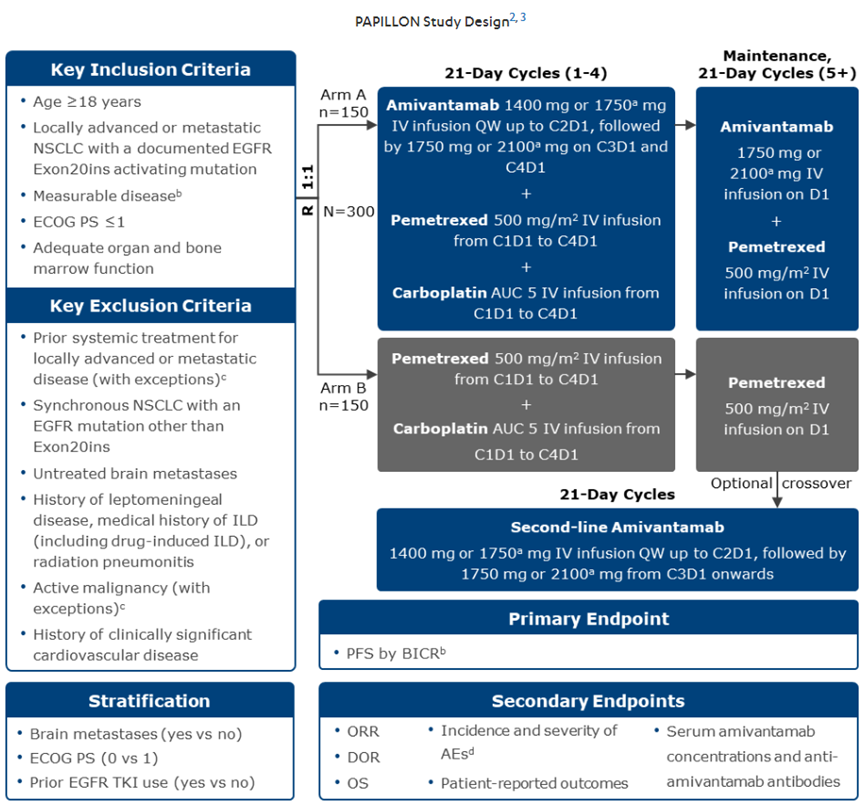
▲研究设计
研究结果
2023年ESMO大会上公布的最新数据显示,与单独化疗相比,埃万妥单抗联合化疗可使患者中位PFS由 6.7 个月延长至 11.4 个月,并使患者疾病进展或死亡风险降低 60% 以上(HR:0.395,95%CI 0.30-0.53;P<0.0001),ORR由 47% 提升至 73%。
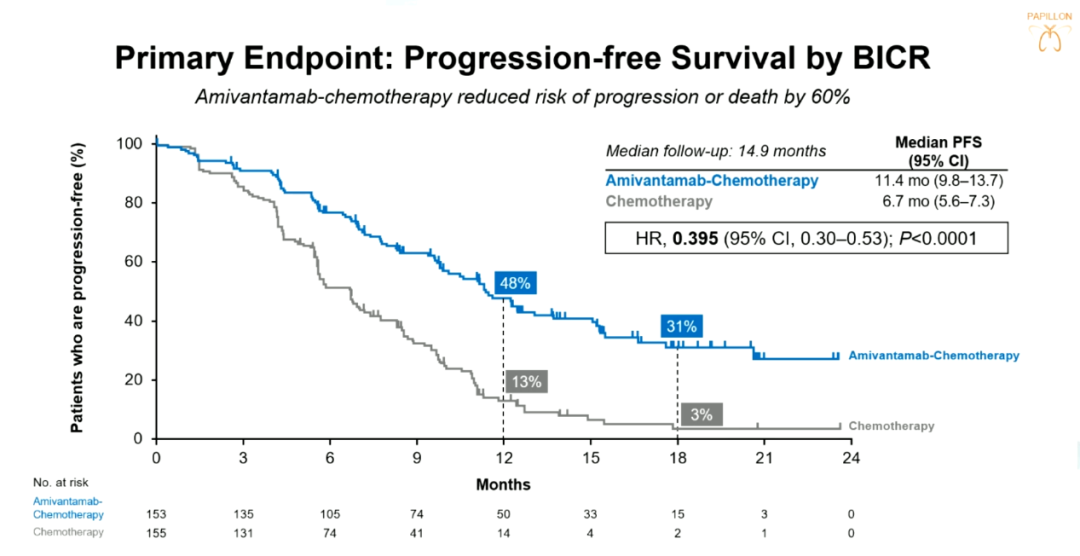
▲主要研究终点PFS
此外,值得一提的是,根据PAPILLON研究中PFS2数据提示,埃万妥单抗联合化疗的中位PFS2无法估计(NE),相比单纯化疗可降低患者 50% 以上的二次疾病进展或死亡风险(HR:0.493,95%CI 0.32-0.76;P<0.001)。化疗组有 66% 的患者在疾病进展后接受了二线埃万妥单抗单药治疗,中期OS数据分析(成熟度33%)显示,埃万妥单抗联合化疗组相对于单纯化疗组仍有OS获益的趋势(HR=0.675,95%CI 0.42-1.09;P=0.106),提示埃万妥单抗联合化疗可为EGFR ex20ins晚期NSCLC患者的一线治疗带来综合临床获益。
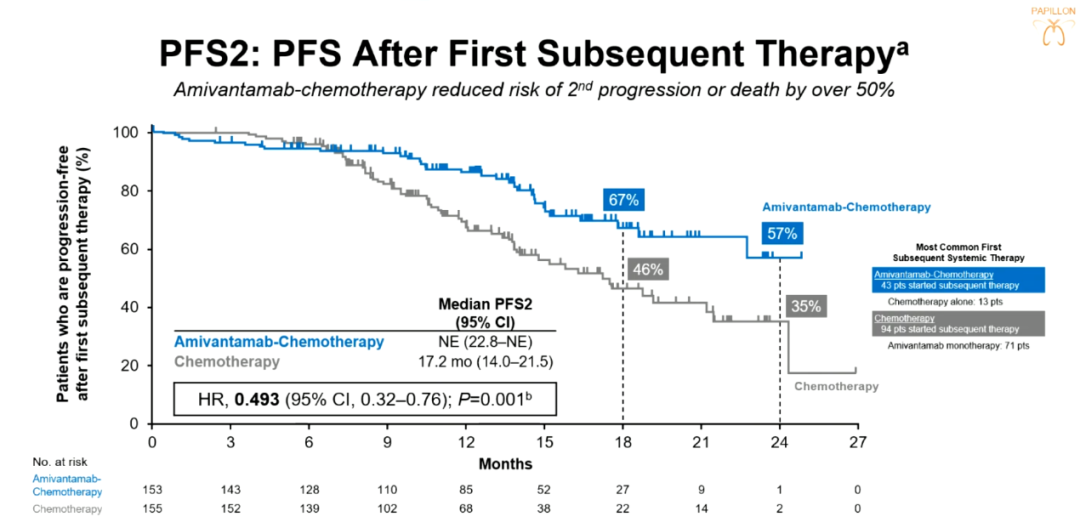
▲PFS2
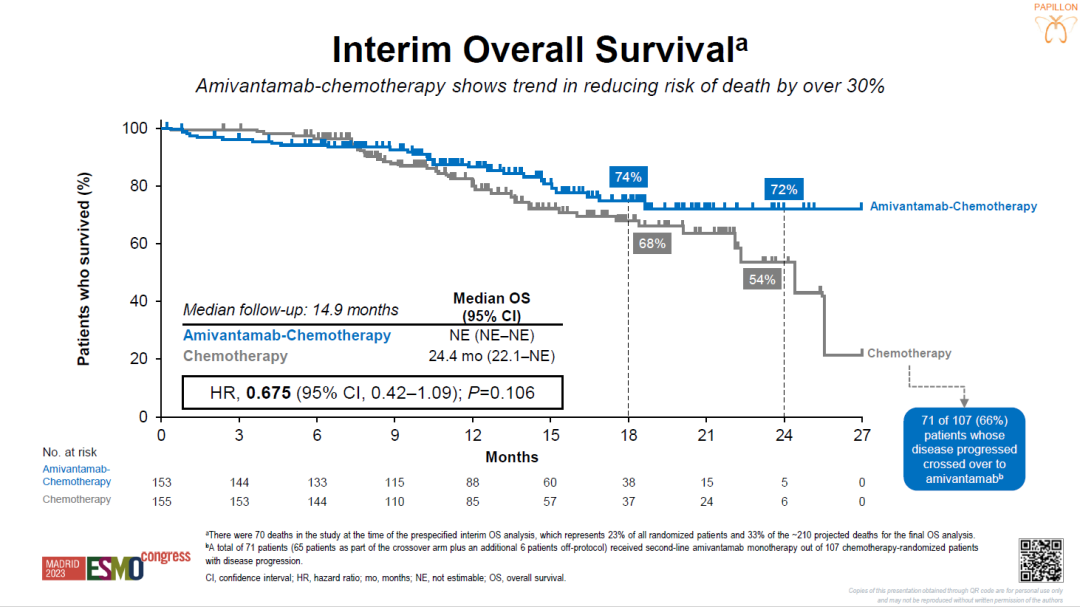
▲OS
MARIPOSA-2研究
研究设计
MARIPOSA-2是一项随机、开放标签的III期临床研究,该研究主要评估疾病进展或奥希替尼耐药后,埃万妥单抗+拉泽替尼(lazertinib)+卡铂+培美曲塞联合治疗方案(LACP,A组)和卡铂+培美曲塞(CP,B组)对EGFR常见突变的局部晚期或转移性非鳞NSCLC的疗效和安全性。另设埃万妥单抗+卡铂+培美曲塞组(ACP,C组)以评估拉泽替尼在LACP方案中的作用。临床中共入组 657 例患者并且按照 2:2:1 的比例分别入组LACP组、CP组和ACP组。

▲研究设计
研究结果
中位随访 8.7 个月时,ACP组、LACP组以及单纯化疗组患者的中位PFS分别为 6.3 个月、 8.3 个月以及 4.2 个月,与单独化疗相比,ACP(HR:0.48,95%CI 0.36-0.64;P<0.001)与LACP(HR:0.44,95%CI 0.35-0.56;P<0.001)方案均可显著延长患者PFS,并使患者疾病进展或死亡风险降低 50% 以上。此外,对于颅内疗效方面,相较于化疗组,ACP组和LACP组可分别显著降低 45% 和 42% 的颅内疾病进展或死亡风险;颅内ORR方面,ACP、LACP组分别为 64%、63%,而化疗组为 36% 。
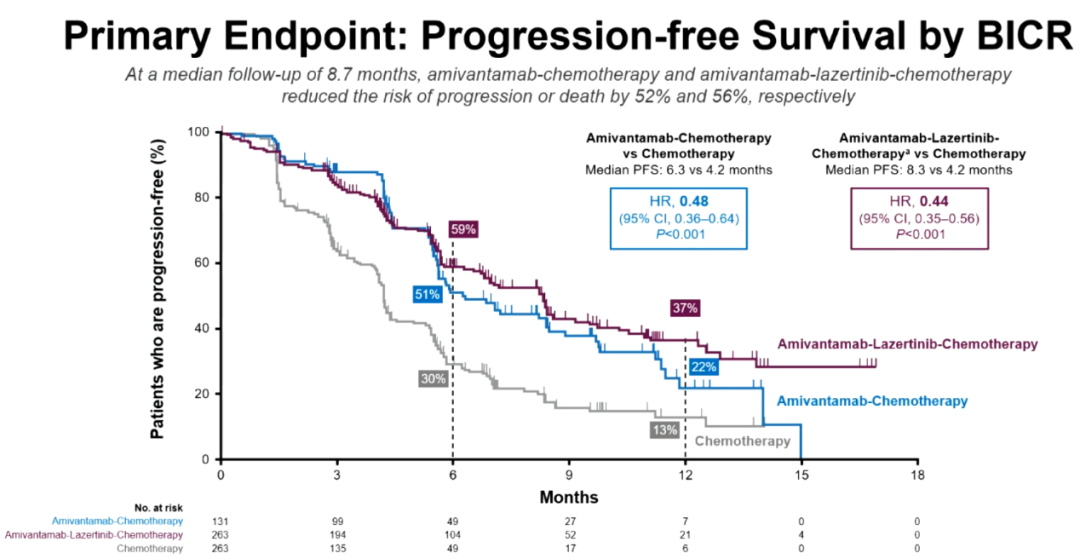
▲PFS
安全性方面,ACP组的血液学AE发生率低于LACP组,在三联方案中,≥3级血液学毒性更常见,即中性粒细胞减少(55%)、血小板减少(37%)和白细胞减少(27%);在ACP组中,≥3级AE为中性粒细胞减少症(45%)、白细胞减少症(20%)和血小板减少症(15%)。
ROS1重排
TRIDENT-1研究
2023 年 11 月 16 日,再鼎医药合作伙伴百时美施贵宝公司(BMS)宣布,瑞普替尼(repotrectinib,Augtyro™)已获美国食品和药物监督管理局(FDA)批准,用于治疗ROS1阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。瑞普替尼获FDA批准是基于 1/2 期TRIDENT-1研究的数据。

研究设计
TRIDENT-1(NCT03093116)是一项全球、开放标签、多中心、首次人体试验,由两个部分组成:在研究的第一部分中,研究人员着手确定瑞普替尼的推荐 2 期剂量(RP2D),以评估剂量限制性毒性(DLT)并检查该药物的药代动力学特征(PK),特别是最大血浆浓度和血浆浓度时间曲线下面积。研究的第二部分,主要终点是通过盲法独立中央审查(BICR)和RECIST v1.1标准评估的ORR。次要终点包括缓解持续时间(DOR)、临床获益率(CBR)、无进展生存期(PFS)、总生存期(OS)和颅内ORR。
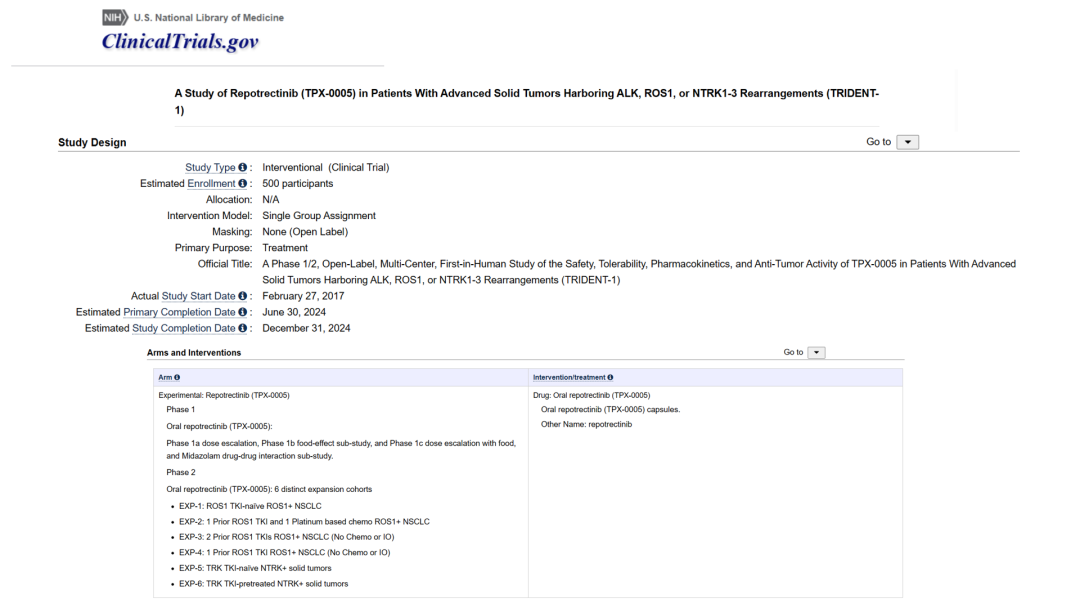
▲研究设计
研究结果
TRIDENT-1研究结果显示,在TKI初治患者(n = 71)中,客观缓解率(ORR)为 79% ,无进展生存期(PFS)为 35.7 个月,中位缓解持续时间(mDOR)为 34.1 个月。在既往接受过一种ROS1 TKI且未接受过化疗的患者中(n = 56),ORR为 38%,mDOR为 14.8 个月。在基线时可测量的脑转移患者中,在 8 名未接受TKI治疗的患者中,有 7 名观察到了颅内应答;在 12 名接受过TKI治疗的患者中,有 5 名观察到了颅内应答。
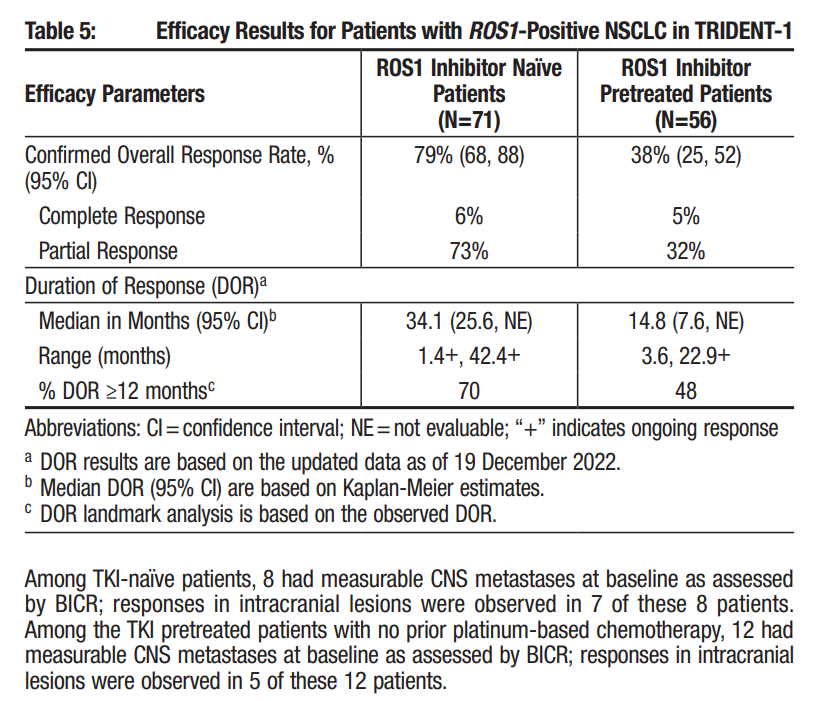
▲TRIDENT-1研究中ROS1阳性NSCLC患者的疗效数据
安全性数据
最常见的不良反应(≥20%)为头晕、味觉障碍、周围神经病变、便秘、呼吸困难、共济失调、疲劳、认知障碍和肌无力。最常见(≥2%)的3级或4级实验室异常为血红蛋白减少、淋巴细胞减少、白细胞减少、ALT增加、中性粒细胞减少、γ-谷氨酰转移酶增加、ALP增加、尿酸盐增加、镁增加和磷酸盐减少。
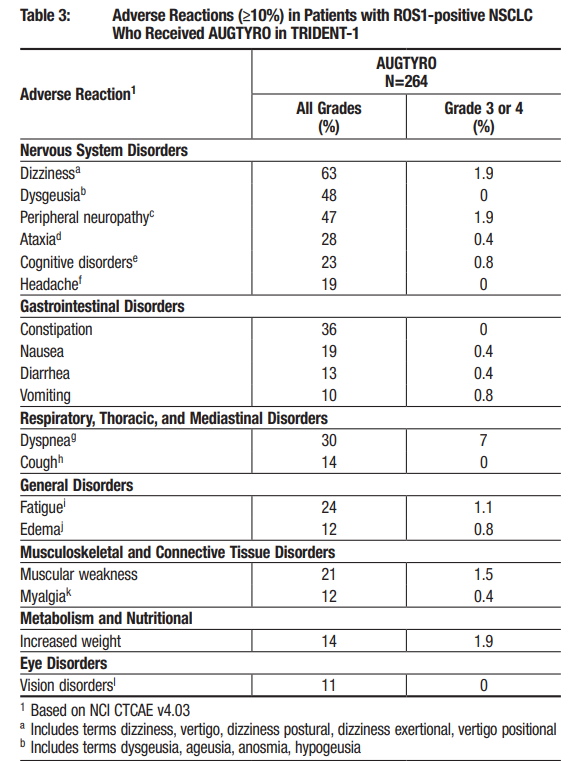
▲不良事件

作者:苏州绘真医学
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#非小细胞肺癌# #EGFR突变# #ROS1重排#
26