【ERJ】对筛查出的肺动脉高压致病BMPR2变异体的未受影响携带者进行深度表型分析
2024-08-23 肺动脉高压研究进展 肺动脉高压研究进展
本研究也强调了动物模型在验证人类研究发现中的重要作用。通过转基因Bmpr2Δ71Ex1/+大鼠模型,我们不仅验证了人类UCs中的发现,还为未来的机制研究提供了一个有价值的实验平台。

研究背景:
BMPR2基因中的致病变异被认定为遗传性肺动脉高压(PAH)的主要遗传风险因素。然而,由于其不完全外显,仅有部分携带该基因变异的个体最终会发展为PAH。因此,通过多模态筛查未受影响的携带者(UCs)进行深入表型分析,有助于早期诊断,并识别可能导致未来PAH发展的易感特征。这种筛查不仅能提高疾病的早期发现率,还能为高风险人群的预防性治疗提供依据。
研究方法:
本研究共招募了28名未受影响的BMPR2变异携带者(UCs),平均年龄为44±16岁,其中57%为女性。同时,研究还包括21名健康对照组,平均年龄为43±18岁,其中48%为女性。所有参与者都进行了年度筛查,筛查项目包括心脏磁共振成像(cMRI)、经胸超声心动图(TTE)、心肺运动试验(CPET)和右心导管插管术(RHC)。通过这些筛查手段,构建了右心室压力-容积(PV loop),用于评估负荷独立的收缩力,并与健康对照组进行比较。此外,我们还使用了转基因Bmpr2Δ71Ex1/+大鼠模型,以验证在人类研究中发现的结果。
研究结果:
研究发现,UCs的心脏容积显著低于健康对照组。具体而言,UCs的索引右心室舒张末期容积为80±18 mL/m²,而对照组为64±14 mL/m²(p=0.003);索引右心室收缩末期容积为34±11 mL/m²,对照组为27±8 mL/m²(p=0.024);左心室舒张末期容积为69±14 mL/m²,对照组为60±11 mL/m²(p=0.019)。这些结果表明,UCs的心脏在结构上存在显著变化。
在使用转基因Bmpr2Δ71Ex1/+大鼠模型进行的研究中,也观察到这些大鼠的心脏容积较WT大鼠显著减小,进一步验证了在人类UCs中发现的现象。PV环分析显示,UCs具有显著更高的后负荷(Ea)(0.15±0.06 vs. 0.27±0.08;p<0.001),以及收缩末期弹性(Ees)(0.28±0.07 vs. 0.35±0.10;p=0.047),同时右心室-肺动脉耦合(Ees/Ea)较低(2.24±1.03 vs. 1.36±0.37;p=0.006)。
在4年的随访期间,有两名UCs发展为PAH。这两名UCs在诊断时其NT-proBNP和TTE指标均正常,这表明即使是常规筛查指标正常的个体,也可能面临PAH的风险。因此,深入的多模态筛查对于早期发现PAH具有重要意义。
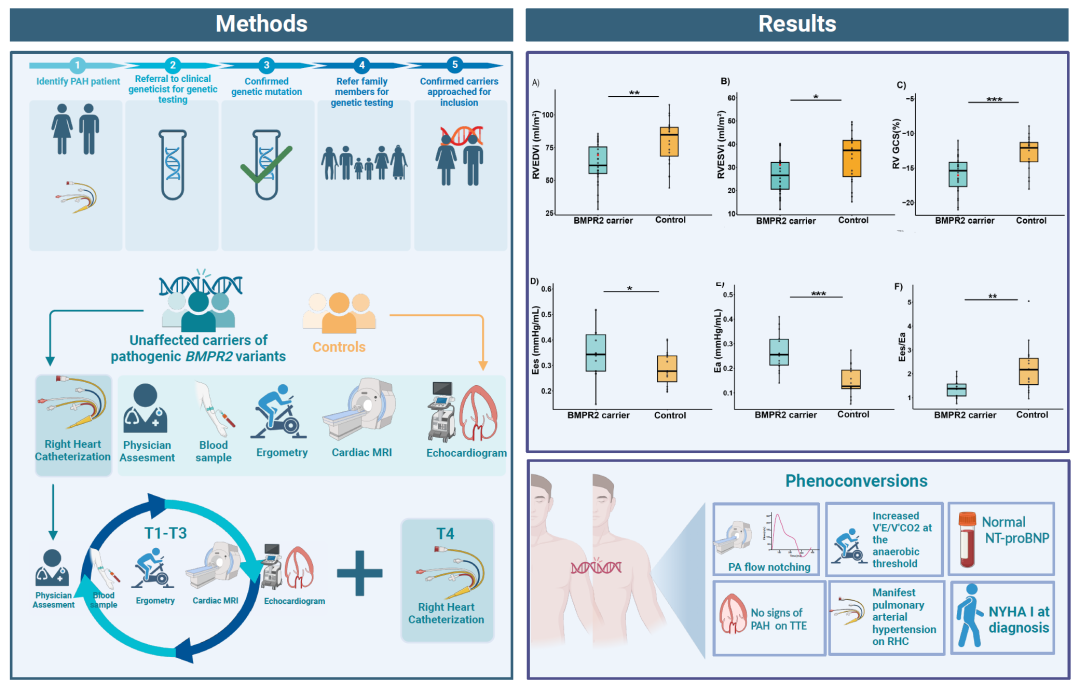
Graphical Abstract:在遗传咨询后,招募了致病性BMPR2变异的未受影响携带者(UCs)和健康家庭成员(对照组)参与研究。采用多模态筛查方法,对UCs在基线和随访四年时进行额外的右心导管插管(RHC)。主要研究发现包括UCs的索引右心室收缩末期容积(RVESVi)和舒张末期容积(RVEDVi)较低,以及较高的右心室全局周向应变(RV GCS)。血流动力学和压力-容积环分析显示UCs的右心室收缩末期弹性(Ees)更高,右心室后负荷(Ea)增加,右心室-肺动脉耦合(Ees/Ea)发生改变。在研究期间,两名参与者发展为肺动脉高压(PAH)。
研究结论:
本研究发现,未受影响的BMPR2突变携带者(UCs)具有一种改变的心脏表型,这种表型在转基因Bmpr2Δ71Ex1/+大鼠中也得到模拟验证。具体表现为右心室和左心室的舒张末期容积和收缩末期容积均显著降低,同时后负荷和收缩末期弹性增加,而右心室-肺动脉耦合则降低。这些心脏结构和功能上的变化可能为未来发展PAH的高风险人群提供了早期预警信号。
基于这些发现,建议对携带BMPR2致病变异的个体进行更为频繁和深入的多模态筛查。这不仅有助于早期诊断PAH,还能为高风险人群制定个性化的预防和治疗策略提供依据。未来的研究应进一步探讨这些心脏表型变化的机制,以及如何在临床实践中有效应用这些发现来改善PAH的早期检测和管理。有效的筛查方案需要较长时间的随访,以充分评估这些筛查方法的敏感性和特异性,从而为携带BMPR2致病变异的个体提供更为精准和有效的医疗服务。
此外,本研究也强调了动物模型在验证人类研究发现中的重要作用。通过转基因Bmpr2Δ71Ex1/+大鼠模型,我们不仅验证了人类UCs中的发现,还为未来的机制研究提供了一个有价值的实验平台。未来的研究应继续利用这些动物模型,深入探讨BMPR2基因变异导致PAH的病理生理机制,寻找潜在的治疗靶点,为改善PAH患者的预后提供新的思路和方法。
参考文献:
Tóth EN, Celant LR, Niglas M, Jansen S, Tramper J, Baxan N, Ashek A, Wessels JN, Marcus JT, Meijboom LJ, Houweling AC, Nossent EJ, Aman J, Grynblat J, Perros F, Montani D, Vonk Noordegraaf A, Zhao L, de Man FS, Bogaard HJ. Deep phenotyping of unaffected carriers of pathogenic BMPR2 variants screened for pulmonary arterial hypertension. Eur Respir J. 2024 Jul 11:2400442. doi: 10.1183/13993003.00442-2024. Epub ahead of print. PMID: 38991711.
作者:肺动脉高压研究进展
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









感谢您的分享
85
#肺动脉高压# #Bmpr2#
44