AXS-05获得FDA突破性疗法认定,用于治疗阿尔茨海默症躁动
2020-06-28 Allan MedSci原创
生物制药公司Axsome近日宣布,美国食品药品监督管理局(FDA)已授予AXS-05突破性疗法认定,用于治疗阿尔茨海默症(AD)躁动。
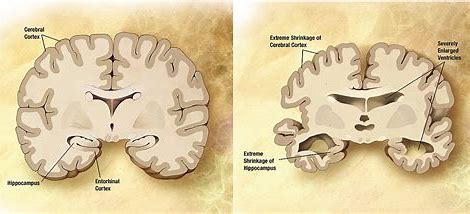
生物制药公司Axsome近日宣布,美国食品药品监督管理局(FDA)已授予AXS-05突破性疗法认定,用于治疗阿尔茨海默症(AD)躁动。AXS-05是一种新型研究性NMDA受体拮抗剂。目前尚无批准的治疗AD躁动的疗法。
关键性II/III期临床试验(ADVANCE-1研究)的积极结果支持了AXS-05在AD躁动中的应用,这项研究共招募了366例阿尔茨海默症患者,患者被随机分为AXS-05组、安非他酮组或安慰剂组。结果表明,与安慰剂相比,AXS-05可快速改善患者的躁动。在主要终点上,与安慰剂相比,AXS-05组患者的Cohen Mansfield兴奋性调查表(CMAI)总分在第5周时较基线有显著下降(p=0.010)。AXS-05组患者的CMAI总分也优于安非他酮组(p<0.001)。AXS-05具有良好的耐受性,与认知障碍或镇静无关。
治疗中最常见的不良反应事件是嗜睡(AXS-05组占8.2%,安非他酮组占4.1%,安慰剂组占3.2%)、头晕(分别为6.3%,10.2%,3.2%)和腹泻(分别为4.4%,6.1%和4.4%)。
原始出处:
作者:Allan
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#阿尔茨海#
65
#阿尔茨#
53
情况
120
#阿尔茨海默#
60
#突破性疗法#
61