酒精性肝病(ALD)是由于长期大量饮酒导致的肝脏疾病。ALD在西方国家常见,但近些年中国ALD的发病率也呈明显上升趋势。ALD早期常表现为酒精性脂肪肝,进而可发展为酒精性脂肪性肝炎(ASH)、肝纤维化和肝硬化,严重酗酒时可导致肝功能衰竭,部分患者甚至会发展为肝细胞癌(HCC)。虽然肝穿刺活检在ALD中的应用存在一定争议,但其在确定患者病因、评估疾病发展阶段和患者预后,以及评估患者是否需要治疗干预和监测治疗效果等方面具有重要意义。因此,提高病理学医生对ALD病理学特征及其临床意义的认识尤为重要。
1ALD的主要组织病理学特征
1.1 酒精性脂肪肝
肝细胞脂肪变是酒精性肝损伤最早和最常见的组织学表现。脂肪变主要发生在肝小叶中央区,在病变严重的情况下,可累及整个肝小叶。酒精性脂肪肝有3种脂肪变类型,即大泡性脂肪变、微泡性脂肪变和混合性脂肪变。通常以大泡性脂肪变为主,其特征是肝细胞内存在单个较大的圆形脂滴,导致肝细胞增大、胞核移位(图1a)。此外,有些肝细胞内可见多个体积较小、轮廓清晰可辨认的脂滴空泡,仍属于大泡性脂肪变的范畴,可能代表了肝细胞内脂肪积累的不同阶段(图1a)。微泡性脂肪变是指肝细胞胞质内存在数量多、轮廓不清而无法计数的微小脂滴,导致肝细胞具有泡沫状胞质,细胞核居中,也被称为酒精性泡沫样变性(AFD)(图1b)。AFD是急性酒精性肝病的一种病变形式,可伴汇管区纤维化、窦周纤维化、巨线粒体和胆汁淤积,但气球样变和Mallory小体少见,而且无明显炎症性坏死。大泡性脂肪变的大脂滴破裂溢出进入肝血窦,则可以引起组织细胞反应,称为脂质肉芽肿,常分布于中央静脉周围(图1a)。由炎症介导的肝细胞坏死在酒精性脂肪肝阶段较为少见。
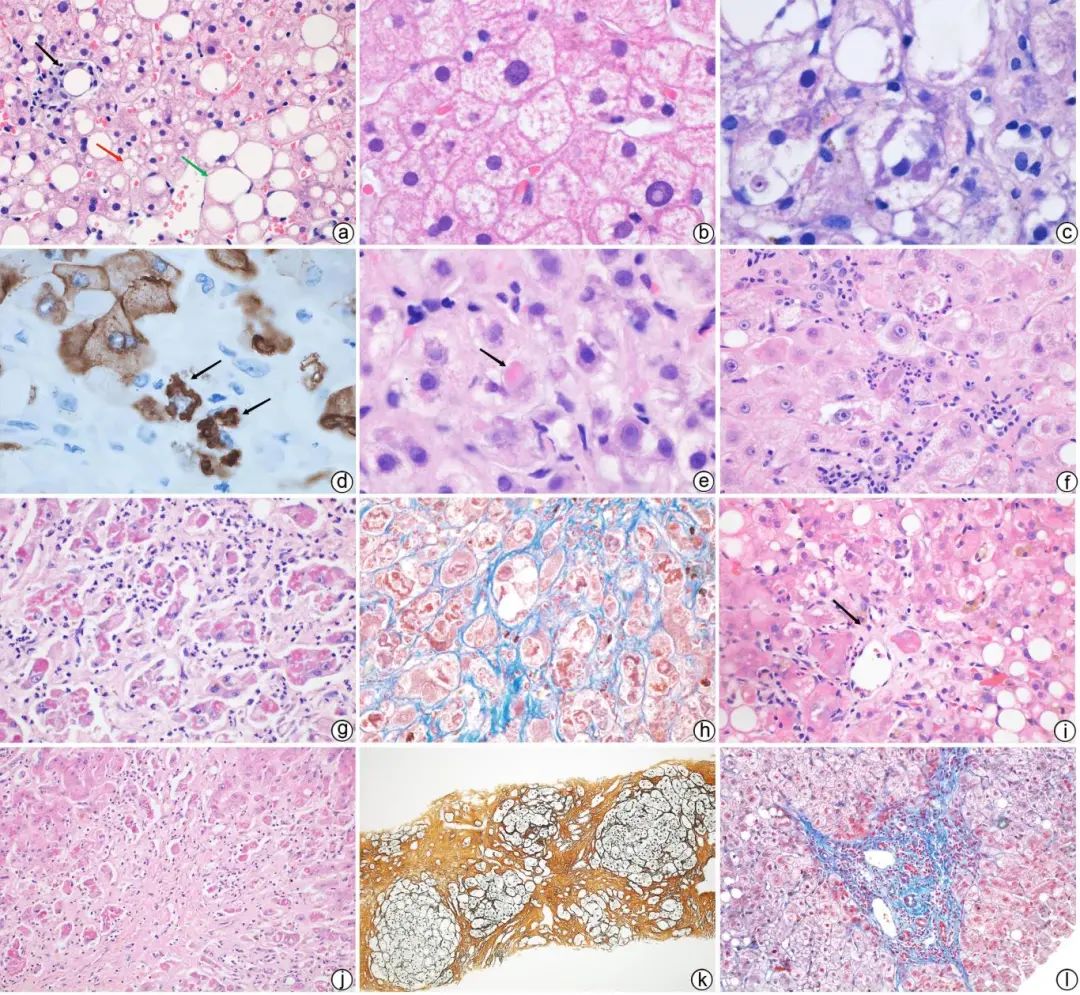
注:a,肝细胞大泡性脂肪变,绿色箭头示大泡性脂肪变中的大脂滴,红色箭头示小脂滴,但轮廓清晰仍属大泡性脂肪变,黑色箭头示脂质肉芽肿(HE染色,×400);b,肝细胞微泡性脂肪变(HE染色,×1 000);c,肝细胞气球样变伴Mallory小体形成(HE染色,×1 000);d,免疫组化CK8/18染色,箭头所示为染色阳性的绳索样Mallory小体(DAB显色,×1 000);e,巨线粒体(箭头所示)(HE染色,×1 000);f,肝实质内中性粒细胞浸润,部分包绕在气球样变的肝细胞周围,被称为“卫星现象”(HE染色,×400);g,ALD相关肝衰病例可见多量Mallory小体及中性粒细胞浸润(HE染色,×400);h,窦周纤维化(Masson染色,×400);i,中央静脉周围纤维化,箭头示胶原纤维在中央静脉外侧壁沉积,导致静脉壁明显增厚(HE染色,×400);j,小叶中心硬化性玻璃样坏死(HE染色,×200);k,小结节性酒精性肝硬化(网状纤维染色,×100);l,汇管区星芒状纤维化(Masson染色,×200)。
图1 ALD的主要组织病理学特征
1.2 ASH
ASH的主要特征是肝细胞脂肪变、气球样变(常含Mallory小体)和肝小叶炎,同时伴有不同程度的肝纤维化。这些病变主要发生在肝小叶中央区。多数病例存在肝细胞脂肪变,通常为大泡性脂肪变或混合性脂肪变,偶尔伴有小灶微泡性脂肪变。在近期戒酒的人群中,脂肪变可能是轻微或不存在的,但ASH的其他特征仍然存在。因此,与非酒精性脂肪性肝炎(NASH)不同,肝细胞脂肪变不是诊断ASH的必需条件。
气球样变反映了酒精诱导的肝细胞骨架的损伤,也是进行性肝损伤机制中的关键步骤。肝细胞由于细胞膜依赖能量的离子泵发生功能障碍,使细胞不能维持离子和液体的平衡,造成细胞内液体积聚,部分细胞体积明显增大(比正常细胞大2~4倍),变圆,胞质空淡,称为气球样变(图1c)。与大泡性脂肪变的肝细胞不同,气球样变的肝细胞仍保留疏松网状胞质,核居中。许多气球样变肝细胞内含有绳索状的嗜酸性小体,称为Mallory小体,常常环绕在细胞核周围(图1c)。Mallory小体由错误折叠和聚集的角蛋白丝聚集而成。通过细胞角蛋白8/18(图1d)、泛素和p62免疫组化染色可以帮助识别Mallory小体。在气球样变的肝细胞中偶尔可见另一种嗜酸性小体,呈球形或针状,称为巨线粒体(图1e)。巨线粒体主要分布在小叶中心,常与Mallory小体共存。研究发现巨线粒体的存在可能与患者最近大量饮酒有关,且病变进展为肝纤维化或肝硬化的风险显著增加。
ASH的肝细胞坏死可以从轻度的点状坏死到较严重的融合性坏死以及桥接坏死都有可能出现。小叶中常可见到数量不等的中性粒细胞聚集,有时包绕在气球样变的肝细胞周围,则称为“卫星现象”(图1f)。有研究发现,中性粒细胞与肝细胞结合,可通过氧化应激和溶酶体酶的释放介导细胞死亡。中性粒细胞浸润被认为与重型ASH的发生和发展密切相关。在ALD相关肝衰竭病例中,往往可见较多含Mallory小体的气球样变肝细胞伴多量中性粒细胞浸润(图1g)。ASH的汇管区炎症通常比其他形式的慢性肝炎(如病毒性肝炎)轻微,常为混合性炎症细胞浸润,包含淋巴细胞、中性粒细胞、浆细胞和嗜酸性粒细胞等。
酒精性肝炎(AH)曾被视为与ASH等同,但最近被认识到二者存在一定区别。ASH是一种组织学表现,而AH是一组临床综合征,后者定义为有潜在ALD和长期饮酒的患者出现突发黄疸、全身乏力、失代偿性肝病和凝血障碍等严重的临床症状。在临床上,ASH可见于只有轻度肝功能异常的无症状患者,而AH患者临床症状较为严重。在组织病理学方面,AH患者的肝活检常表现为严重的ASH、AFD,同时伴发胆汁淤积。
1.3 酒精性肝纤维化及肝硬化
ASH的肝细胞损伤、炎症以及细胞内脂滴的释放都可以促进肝纤维化的发展。病变早期,小叶中央区肝窦内肝星状细胞增生活化,释放细胞外基质,导致窦周间隙内胶原纤维沉积,逐渐形成包绕气球样变肝细胞的“鸡笼样”窦周纤维化。上述特征可以通过Masson三色染色、天狼星红染色以及网状纤维染色更好地观察明确(图1h)。窦周纤维化缺乏成熟纤维间隔中特征性的弹力纤维,因此被认为是一种早期的纤维化形式。在一些中重度饮酒者的肝组织中,胶原纤维在中央静脉外侧壁沉积,导致静脉壁明显增厚,形成中央静脉周围纤维化(图1i)。有学者将其定义为终末肝小静脉(中央静脉)周围2/3以上范围的纤维化,其纤维厚度至少达4 μm。中央静脉周围纤维化是肝纤维化进展的重要预测因子。在某些重症ALD患者的肝活检组织中,可见闭塞的中央静脉周围出现大片肝细胞坏死或脱失,伴多量胶原沉积,被称为硬化性玻璃样坏死(图1j)。这种损伤模式几乎只在ALD中存在,而且常常导致严重的门静脉高压和腹水,提示患者预后不良,因此对这种损伤模式的识别十分重要。
目前,关于酒精性肝纤维化的研究大多集中在小叶中心。然而,汇管区纤维化也是ALD病变进展的一部分,表现为胶原纤维增多,部分呈放射状伸入周围肝小叶,呈“星芒状”纤维化(图1k)。汇管区纤维化的主要原因可能与炎症细胞浸润和胆管反应相关。此外,也有学者提出,当ALD出现汇管区纤维化时,应考虑伴发胆管疾病、酒精性胰腺炎或病毒性肝炎的可能,需要结合临床进一步评估。
酒精性肝硬化始于中央小叶区域纤维化,逐渐形成连接邻近中央静脉或汇管区的纤维间隔,分割包绕原有肝小叶,同时再生结节的形成和伴随的结构破坏最终导致了肝硬化形成。酒精性肝硬化最初表现为小结节性肝硬化,结节直径一般<3 mm(图1l)。然而,小结节性肝硬化并非一成不变,部分患者戒酒后,其小结节性肝硬化可能向大结节性肝硬化转变。
2ALD的其他病理学改变
2.1 肝内胆汁淤积
部分ALD患者可出现明显的黄疸,血清总胆红素和碱性磷酸酶显著升高,其临床病理学特征与肝外胆道梗阻非常相似,肝活检可见汇管区水肿,伴显著的细胆管反应和中性粒细胞浸润(图2a);肝实质出现明显的肝细胞和毛细胆管淤胆(图2b)。目前,在NAFLD中尚未发现这种胆汁淤积性肝损伤模式。需要注意的是,有些重症ALD患者的肝活检出现汇管区细胆管增生、扩张伴淤胆,被称为“Lenta胆管炎”(图2c)。这种形态高度提示患者有合并感染的可能,病死风险升高。此外,Yamada等在ALD中还注意到了小叶间胆管的病变,胆管上皮炎、上皮细胞空泡化、细胞核固缩和嗜酸性变性等病理改变可能与酒精性肝损伤中的胆汁淤积有关。
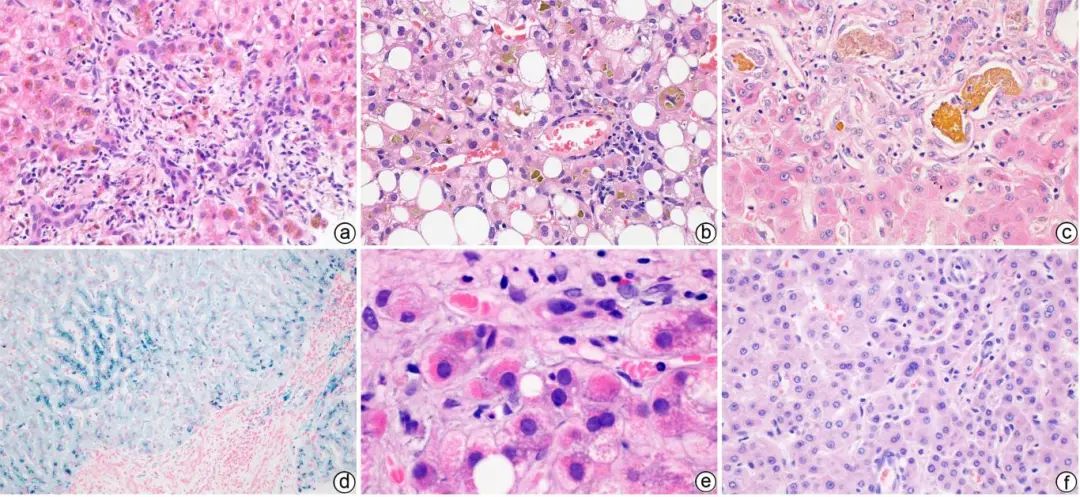
注:a,汇管区水肿,伴显著的细胆管反应和中性粒细胞浸润,模拟大胆管梗阻样形态(HE染色,×400);b,肝小叶3区毛细胆管淤胆(HE染色,×400);c,汇管区细胆管增生伴扩张及淤胆(Lenta胆管炎)(HE染色,×400);d,中度含铁血黄素沉积,位于汇管区周围(普鲁士蓝染色,×200);e,肝细胞嗜酸性变(HE染色,×1 000);f,高级别异型增生结节中的小细胞变(HE染色,×400)。
图2 ALD的其他病理学改变
2.2 含铁血黄素沉积
在ALD中,常见含铁血黄素沉积在肝细胞和Kupffer细胞内(图2d)。病变早期,含铁血黄素沉积通常较轻,呈随机分布。而在部分酒精性肝硬化患者中,含铁血黄素沉积可能更加显著,呈区带分布于汇管区周围,与遗传性血色病相似,基因检测是针对该情况更好的鉴别手段。目前研究发现,活动性酒精中毒是导致肝脏铁沉积的一个重要因素,与肝脏坏死性炎症活动的严重程度相关。对于肝硬化患者而言,铁沉积也是进展为HCC的重要危险因素。
2.3 毛玻璃样肝细胞与嗜酸性肝细胞
在部分ALD患者的肝活检中可见“毛玻璃样”肝细胞,其归因于酒精诱导的肝细胞滑面内质网的增生。在接受氰胺戒酒治疗的患者中也可见毛玻璃样包涵体。肝细胞还可以发生嗜酸性改变,其特征是线粒体数量增加导致细胞质呈强嗜酸颗粒状,常分布于酒精性肝硬化结节的周边(图2e)。这种改变可能代表了肝细胞对于外界病理刺激的一种适应性反应。
2.4 HCC
全球范围内酒精性肝硬化患者HCC的年发病率为0.9%~5.6%,5、10年的HCC的累积发病率分别为3%和9%。ALD相关HCC在组织学上与其他慢性肝病引起的肝硬化癌变的病变模式一致,肝硬化结节内形成异型增生结节,包括低级别异型增生结节和高级别异型增生结节。其中,后者以肝细胞小细胞变为主(图2f),其发生HCC的风险显著增加。ALD相关HCC主要发生于老年男性,几乎完全发生在肝硬化的背景下,通常表现为晚期肿瘤,患者的生存率明显低于NAFLD相关HCC。
3ALD的分级和分期
尽管ALD作为最常见的肝脏疾病之一,其组织病理学特征已得到深入的研究,但目前仍缺乏一个被普遍接受的ALD分级分期系统。2006年,Yip等参照NASH的评分标准提出了ALD的分级系统,用于预后评估以及临床试验肝穿刺活检的比较。我国《酒精性肝病防治指南(2018更新版)》推荐ALD的病理学诊断报告需包括肝脂肪变程度(F0~3)、炎症坏死程度(G0~4),以及肝纤维化分期(S0~4)。2021年,SALVE组织病理学小组制定了ALD的SALVE分级分期系统。该系统通过肝细胞脂肪变、炎症活动性(包括气球样变、Mallory小体及中性粒细胞浸润)和胆汁淤积的半定量评分进行分级,并在NASH临床研究网络和Laennec分期系统的基础上描述了7个SALVE纤维化阶段,可以反映ALD纤维化的模式和程度。上述分级分期系统各有优缺点,临床应用尚未统一完善,需要临床进一步验证并达成共识。
4ALD的鉴别诊断
ALD的组织学改变并不是特异的。大泡性脂肪变是一种常见的组织学变化,与肥胖和其他代谢综合征密切相关。微泡性脂肪变除了发生在ALD以外,亦可见于其他与线粒体β氧化障碍相关的疾病中,如Reye综合征和妊娠期急性脂肪肝。气球样变、Mallory小体和窦周纤维化可以在NASH、Wilson病、慢性胆汁淤积性肝病及药物性肝损伤中出现。肝实质内局限性中性粒细胞浸润可见于各种原因导致的脂肪性肝炎,如NASH和胺碘酮导致的ASH样药物性肝损伤。此外,中性粒细胞聚集灶(微脓肿)更多见于巨细胞病毒感染及肝移植后灌注损伤。伴有胆汁淤积的ALD需要与大胆管梗阻、肝内小胆管损伤、药物性肝损伤、急性病毒性肝炎、败血症/脓毒败血症及遗传性胆汁淤积性肝病进行鉴别。巨线粒体也可见于NAFLD和一些其他慢性肝病,但相较于ALD,数量往往较少。ALD中含铁血黄素的沉积多为轻度(1~2级),如果出现中-重度含铁血黄素沉积(3~4级),且铁颗粒呈区带状分布,则需要通过基因检测排除遗传性血色病的可能。毛玻璃样肝细胞与嗜酸性肝细胞可以通过地衣红染色或免疫组织化学染色与含有HBsAg的经典毛玻璃肝细胞作出区分。
临床上,ASH与NASH的鉴别是最受关注的问题。虽然二者形态上有重叠,但在很多病变特征上存在一定程度上的差异(表1)。如果患者有明确或疑似酒精摄入的病史,肝活检组织形态中出现明显中央静脉周围纤维化、硬化性玻璃样坏死、Lenta胆管炎以及汇管区明显细胆管反应伴中性粒细胞浸润,则更倾向于ASH诊断。气球样变、肝细胞坏死/凋亡、Mallory小体、巨线粒体、小叶中性粒细胞浸润和窦周纤维化在ASH中往往更加突出。相反,如果可见较多的糖原核,则提示NAFLD的可能性更大。
![]()
5小结
由于许多ALD患者存在凝血功能障碍和腹水,且临床无创检测手段不断发展,肝活检在ALD患者诊断和治疗中的作用存在争议。在临床实践中,ALD患者是否应用肝活检必须根据个体化情况进行权衡,需要考虑到肝活检可能提供的信息、对治疗的影响以及并发症的风险。在排查是否合并其他肝脏疾病、ASH和NASH之间进行鉴别诊断、明确炎症活动度和纤维化的程度以及指导重症ALD治疗等方面,肝活检仍然是必不可少的辅助手段。对于肝脏专科病理学医生而言,不仅要认识ALD经典的病理学特征,还要能够识别与ALD患者预后不良相关的组织学线索,例如严重的坏死性炎症、多量中性粒细胞浸润、小叶中心硬化性玻璃样坏死、严重的窦周纤维化及中央静脉周围纤维化、广泛的Mallory小体形成以及明显的肝内胆汁淤积等,上述病理学表现均需要详细描述,为临床提供预后信息。
全文下载
https://www.lcgdbzz.org/cn/article/doi/10.12449/JCH240602

作者:临床肝胆病杂志
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#酒精性肝病# #病理学诊断#
49