Connexin可能在香烟烟雾引起的肺动脉高压中起关键作用
2022-04-03 刘少飞 MedSci原创
最近的研究表明,CS 暴露引起的肺血管内皮功能障碍可能是 PH 自然史中的初始事件,这反过来可能与连接蛋白(Cx)表达的异常改变有关。Cx 和 CS 诱导的 PH 发展之间的关系尚未被直接研究。
自 1973 年以来,肺动脉高压 (PH) 被定义为静息时平均肺动脉压 (mPAP) 升高≥ 25 mmHg。2018年,在第六届世界肺动脉高压研讨会(WSPH)上提出重新考虑PH的血流动力学定义,将PH重新定义为存在mPAP > 20 mmHg并伴有肺血管阻力(PVR)≥3 Wood Units( WU)。PH 是一种常见疾病,据报道,全世界约有 1% 的成年人患有此病。它是一种破坏性疾病,会导致肺血管阻力逐渐发展,导致右心衰竭并最终死亡。PH是一种发病年龄早、潜在机制复杂的难治性疾病。由于这些原因,这种疾病作为世界范围内的研究课题引起了广泛的关注。PH 的特点是肺血管收缩和血管重塑。然而,目前的治疗仍侧重于血管舒张和长期补氧,未能阻止或逆转作为该疾病关键特征的持续血管重塑。
先前的研究已经证实,长期接触香烟烟雾 (CS) 是 PH 进展的重要危险因素。此外,一些研究表明,导致肺血管重构导致 PH 的初始事件可能是暴露于 CS 引起的肺血管内皮功能障碍。有趣的是,据报道,肺功能正常的年轻吸烟者存在血管内皮功能障碍。维持内皮细胞 (EC) 的功能完整性需要通过不同机制协调单个细胞之间的活动,其中与间隙连接相关的机制尤为重要 。间隙连接是结构上包含连接蛋白 (Cxs) 的细胞间通道,对于传输细胞信号至关重要。已经证明 Cx37、Cx40、Cx43 和 Cx45 在整个血管系统中表达。Cx 介导的细胞间通讯被认为在肺血管收缩和血管重塑中发挥重要作用。近年来,一些研究表明 Cxs 与 CS 诱导的内皮功能障碍有关。然而,尚未研究 Cx 与 CS 诱导的 PH 发展之间的关系。
Cx 在 CS 诱导的 PH 中的潜在作用
NO-sGC-cGMP 信号通路
暴露于 CS 可能会通过 NO-sGC-cGMP 信号通路降低 Cx43 的表达。已知该途径在肺血管生理学和病理生理学中起关键作用。众所周知,NO 是一种有效的肺血管扩张剂,可以激活可溶性鸟苷酸环化酶 (sGC)。sGC 由一个大亚基 (α) 和一个小的血红素结合亚基 (β) 组成;已检测到这两个亚基的几种异构体(称为 α1、α2、β1 和 β2)。NO 通过 sGC 的 β1 亚基与血红素结合,产生环状鸟苷一磷酸 (cGMP) 。许多研究表明,cGMP 不仅是平滑肌收缩的重要调节剂,也是平滑肌对慢性增殖信号反应的重要调节剂。
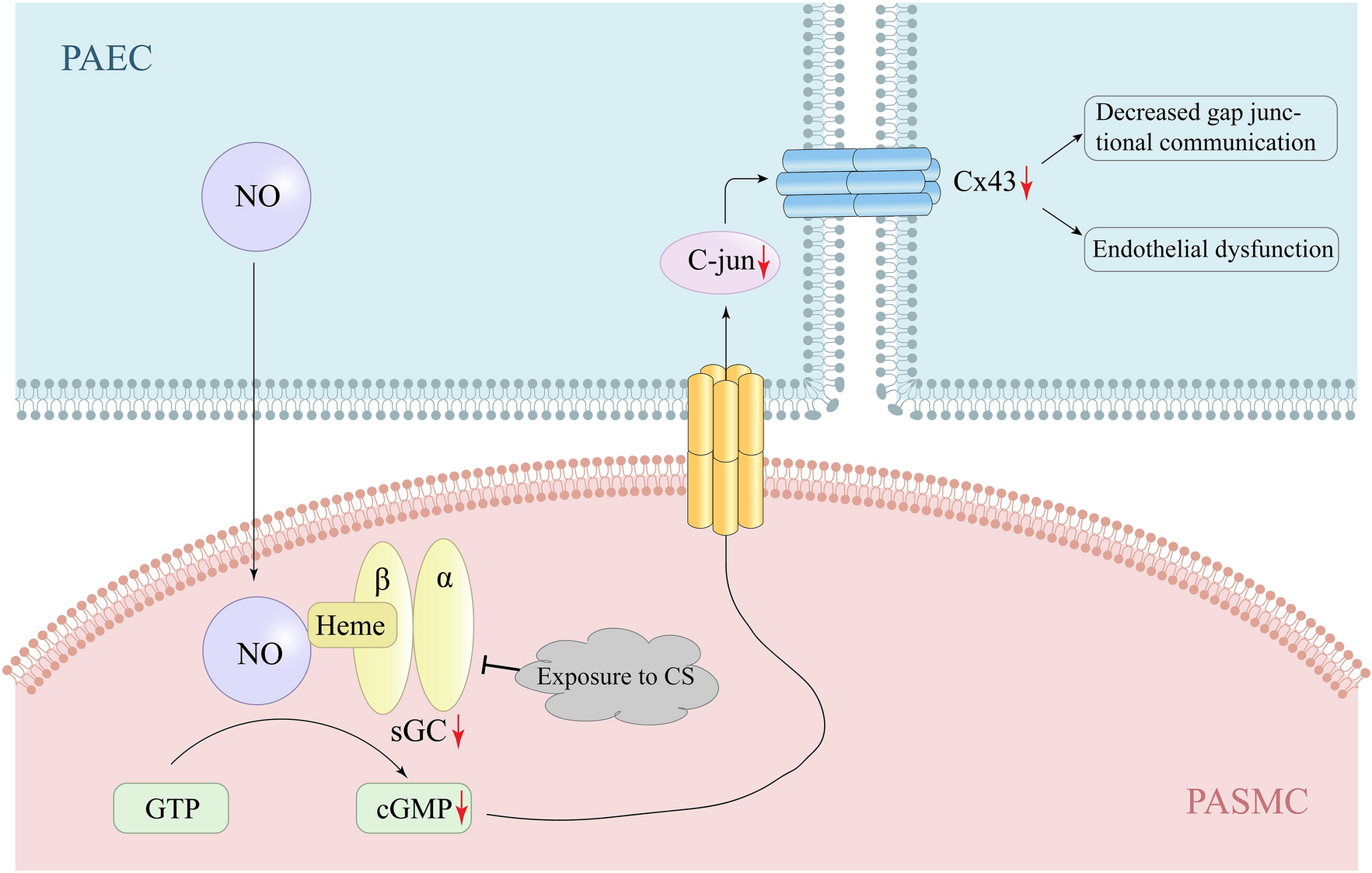
NO-sGC-cGMP 信号通路。PAEC 产生的 NO 可以与 PASMC 中与 sGC 结合的血红素结合,从而产生 cGMP。暴露于 CS 会下调 sGC 亚基,从而导致 cGMP 产生减少。cGMP 降低导致 c-jun 的表达和磷酸化水平降低,导致 Cx43 表达降低,最终导致内皮功能障碍和间隙连接通讯减少。
Ang II – PKC 信号通路
暴露于 CS 可能会通过增加 Ang II 的产生来增加 Cx43 的表达。糜蛋白酶是一种丝氨酸蛋白酶,主要存在于肥大细胞的分泌颗粒中;这种酶被认为与血管疾病有关。与血管紧张素转换酶 (ACE) 类似,糜酶催化血管紧张素 I (Ang I) 生成 Ang II。在人类中,动脉中超过 60% 的 Ang II 和心脏中超过 80% 的 Ang II 似乎是通过食糜酶的作用形成的,而食糜酶依赖性 Ang II 可能在其功能中发挥重要作用。
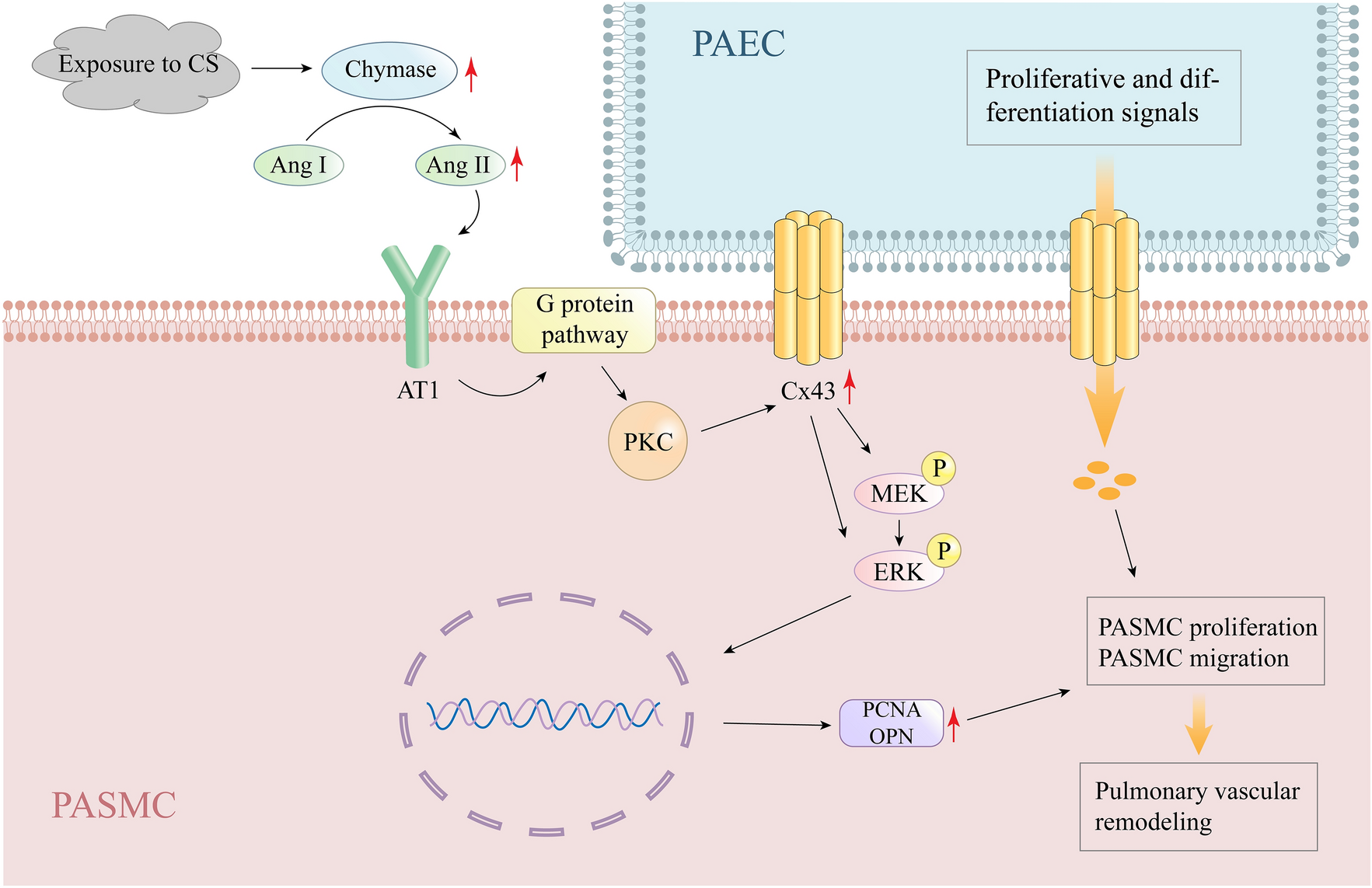
Ang II-PKC 信号通路。长期暴露于 CS 会增加糜酶的活性和表达,从而导致 Ang II 产生增加。增加的 Ang II 激活 AT1 受体,进而通过 G 蛋白途径激活 PKC,最终上调 Cx43 的表达。上调 Cx43 表达一方面促进 MEK/ERK 信号传导从而促进 OPN 和 PCNA 表达,另一方面增加 PAECs 向 PASMCs 传递的增殖和分化信号,从而导致 PASMCs 的增殖和迁移,最终导致肺血管重塑。
总结和未来方向
慢性接触 CS 是 PH 组 3 的一个已知和基本危险因素。然而,吸烟仍然很普遍,而且很难戒掉。目前对 PH 组 3 的治疗仍侧重于血管扩张和长期补氧,未能阻止或逆转持续的血管重塑。因此,吸烟者继续表现出 PH 和死亡风险增加。最近的研究表明,暴露于 CS 引起的肺血管内皮功能障碍可能是 PH 自然史中的初始事件。因此,如果可以靶向由 CS 引起的内皮功能障碍,则有可能在代偿期预防 PH 的发展。
参考文献:
Qin X, Gao A, Hou X, Xu X, Chen L, Sun L, Hao Y, Shi Y. Connexins may play a critical role in cigarette smoke-induced pulmonary hypertension. Arch Toxicol. 2022 Mar 27. doi: 10.1007/s00204-022-03274-6. Epub ahead of print. PMID: 35344070.
作者:刘少飞
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






#动脉高压#
69
关注肺动脉高压研究进展
85
#香烟#
74