Cell Host & Microbe:脑损伤的早产新生儿的肠道-微生物-免疫-脑轴发育异常
2021-09-04 haibei MedSci原创
最近,研究人员分析了60名极度早产婴儿的肠道微生物群、免疫学和神经生理学发展,这些婴儿接受了包括抗生素和益生菌在内的标准医院护理。
早产的发生率在世界范围内一直在上升,是围产期发病率和死亡率的主要原因之一。尽管最近新生儿重症监护的进展提高了极度早产儿(胎龄<28周)的存活率,但这些孩子中具有严重疾病和终身神经发育障碍的数量仍然很高。
怀孕的第三个月是人类大脑连接的建立、完善和成熟的关键时期,这决定了随后的认知潜力。极端早产儿在第三个月的边缘出生,因此他们的神经回路是在多种环境线索和宫外生活的共同刺激下建立的。

一个不可避免的环境线索是出生后身体立即被微生物定植,肠道微生物群将与肠道神经系统的多个神经元接触。越来越多的证据表明,在生命早期,肠道微生物参与了胃肠道(GIT)和大脑之间的双向信号传递。原核生物和人类中枢神经系统(CNS)之间的这种相互交流是通过肠脑轴建立的,其中来自迷走神经的副交感神经纤维直接暴露于细菌及其代谢产物中,而免疫和内分泌系统介导间接串联。
早产婴儿正在发育的大脑遭受围产期白质损伤(PWMI)的风险特别高,它可以表现为脑室内出血(IVH)、脑室周围白斑(PVL)或弥漫性白质损伤(DWMI)。现在人们普遍认为,围产期感染和相关炎症参与了PWMI的病理生理学,并能使脑损伤的结果恶化,导致终身发病,如认知和运动延迟、脑瘫、神经感觉障碍和行为异常。
发育中的免疫系统和肠道微生物群之间的平衡关系对防止过度炎症至关重要。然而,尽管许多新生儿重症监护室(NICU)每天都在使用益生菌,但在极度早产的婴儿中,肠道微生物群和其宿主之间的相互关系的建立似乎受到了损害。
目前,人们对早产新生儿的肠道-微生物群-免疫-脑轴还缺乏详细了解。
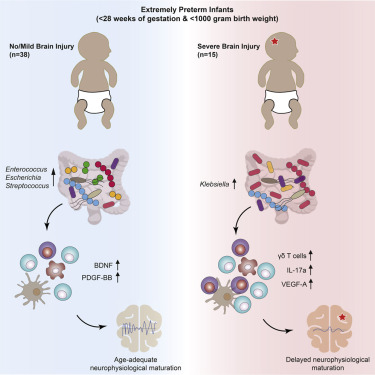
脑损伤的早产新生儿表现出肠道-微生物-免疫-脑轴的发育异常
最近,研究人员分析了60名极度早产婴儿的肠道微生物群、免疫学和神经生理学发展,这些婴儿接受了包括抗生素和益生菌在内的标准医院护理。研究人员发现,在有严重脑损伤的婴儿中,皮质电活动的成熟被抑制。这伴随着γδT细胞水平的升高和T细胞分泌的血管内皮生长因子的增加,以及神经保护因子的分泌减少。
值得注意的是,克雷伯氏菌在肠道的过度生长对脑损伤有很强的预测性,并与促炎症的免疫学基调有关。
这些结果表明,肠道-微生物-免疫-脑轴的异常发展可能驱动或加剧极早产新生儿的脑损伤,这也代表了一种有希望的全新干预策略。
原始出处:
David Seki et al. Aberrant gut-microbiota-immune-brain axis development in premature neonates with brain damage. Cell Host Microbe (2021).

作者:haibei
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#微生物#
0
#发育异常#
55
#CEL#
34
#CRO#
34
jkds
52