Alzheimer’s & Dementia: TREM2的多聚化受阿尔茨海默病相关变异影响
2024-07-28 xiongjy MedSci原创
TREM2三聚体的稳定性主要由D87和R76之间的盐桥驱动。AD相关变异R47H和R98W破坏了这一盐桥,D87N变异则导致其完全丧失,显著减少了TREM2多聚化。
触发受体表达在髓系细胞2型(TREM2)的杂合子遗传变异与多种神经退行性疾病有关,包括阿尔茨海默病(AD)。许多临床相关变异如R47H被认为直接损害TREM2的配体结合和信号传导能力,通过阻止TREM2的成熟和定位到细胞表面,减少R47周围的电势,或者全构性地破坏互补决定区(CDR)样环的稳定性。然而,一些AD相关变异仍保留表面表达,并显示一定的配体结合和信号传导能力。TREM2多聚化可能受到AD相关变异的影响。人TREM2免疫球蛋白结构域的晶体结构显示,TREM2分子以六聚体排列,内三聚体紧密结合,每个成员松散地与一个外TREM2分子关联。

本研究通过分子动力学(MD)模拟和结合能分析,探讨了AD相关变异对TREM2多聚化的影响,并进行了实验验证。我们生成了包含磷脂酰丝氨酸(PS)的CV人TREM2免疫球蛋白结构域的初始六聚体模型,并基于此模型构建了三聚体和二聚体模型。使用PyMOL中的诱变工具生成含R47H、D87N、R98W、P37D或G90D变异的三聚体结构,并使用AMBER软件进行能量最小化和MD模拟。此外,我们还生成了不同pH水平下的CV TREM2模型,并进行了结合自由能分析、盐桥占有率分析和聚类分析。实验验证包括在HEK-293T细胞中进行的共免疫沉淀和非变性PAGE分析。
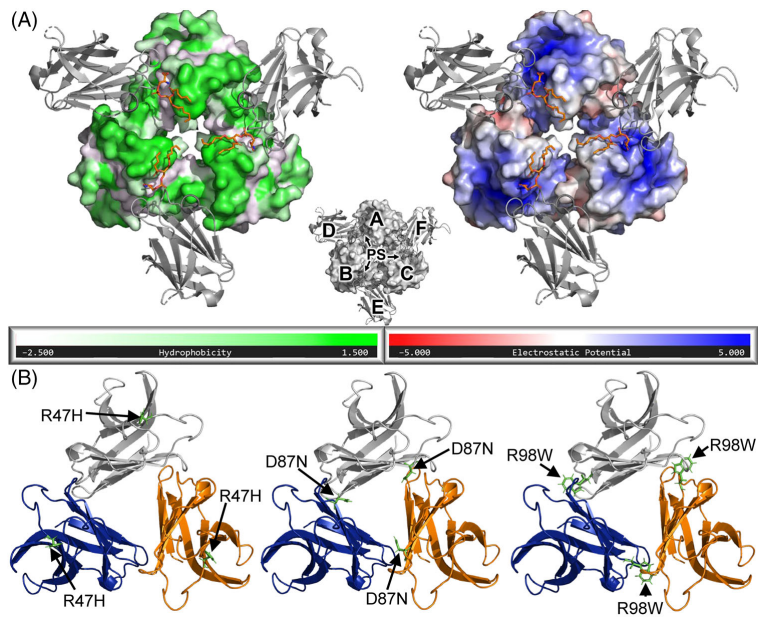
图1.分子动力学模拟的TREM2-R47H、TREM2-D87N和TREM2-R98W三聚体模型
在细胞裂解物中检测到TREM2多聚体。在非变性PAGE上,TREM2-CV转染的样品显示出三条明显的带,分别对应TREM2的单体、二聚体和三聚体。模拟结果表明,D87和R76之间的盐桥在TREM2单位的界面处驱动了稳定的TREM2二聚体和三聚体的形成。AD相关变异R47H和R98W破坏了D87-R76盐桥,D87N变异导致该盐桥完全丧失。进一步的分析显示,R47H和R98W变异通过降低盐桥占有率和结合自由能,削弱了TREM2三聚体的稳定性。D87N变异则通过直接破坏关键的D87-R76盐桥,导致三聚体解离。
实验验证结果与计算结果一致。在pH6.4下,TREM2多聚化减少,而在pH 8.4下,多聚化增加。这表明在老年和AD大脑中略酸性的环境中,TREM2多聚化可能更不利。

图2.AD相关的D87N变异对TREM2三聚体模型的影响
本研究揭示了TREM2形成稳定三聚体的分子基础,并提出了一种新机制,即AD相关变异通过破坏TREM2的多聚化来增加AD风险。这些发现为TREM2靶向治疗的开发提供了重要信息,强调了理解TREM2多聚化对于设计未来药物的重要性。
作者:xiongjy
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#阿尔茨海默病# #遗传变异# #分子动力学模拟算法#
61