Nature Cell Biology:单细胞分析揭示人类前列腺癌进展机制
2021-01-27 AlexYang MedSci原创
前列腺癌显示出明显的临床异质性,表现为空间和克隆基因组多样性。而前列腺肿瘤的转录组异质性却理解甚少。
前列腺癌显示出明显的临床异质性,表现为空间和克隆基因组多样性。而前列腺肿瘤的转录组异质性却理解甚少。

最近,有研究人员对来自13种前列腺肿瘤的36424个单细胞的转录组进行了剖析,并鉴定了上皮细胞来阐释潜在的疾病侵袭机制。结果表明,肿瘤微环境(TME)显示出多种进展相关的转录组程序的激活。值得注意的是,研究人员观察到了杂乱的KLK3表达,并验证了癌细胞改变T细胞转录组的能力。对一个原发肿瘤和两个匹配的淋巴结的剖析发现为KLK3的异位表达与微转移相关提供了证据。细胞之间存在密切的细胞-细胞通信。研究人员发现了一个内皮细胞亚群与肿瘤细胞有活跃的交流(活化的内皮细胞,aECs)。加上另外11个样本的测序,研究人员发现aECs在去势抵抗性前列腺癌中富集,并促进癌细胞的入侵。
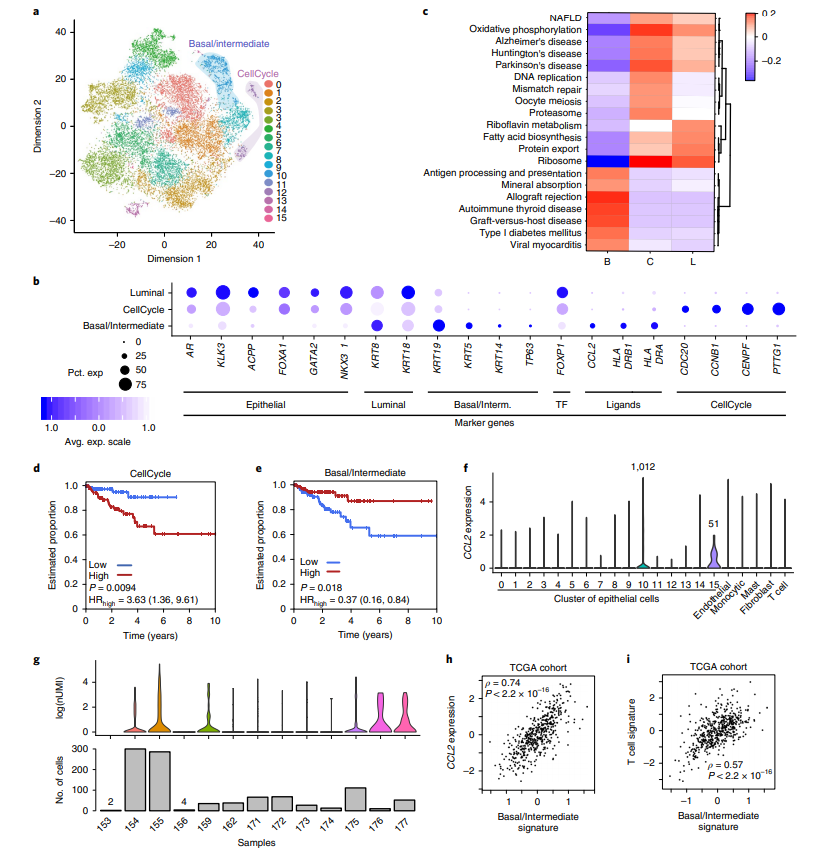
单细胞数据的特征以及与生存的关系
最后,研究人员还创建了一个用户友好的网络界面供使用者探索测序数据。
原始出处:
Sujun Chen, Guanghui Zhu, Yue Yang et al. Single-cell analysis reveals transcriptomic remodellings in distinct cell types that contribute to human prostate cancer progression. Nature Cell Biology. Jan 2021
作者:AlexYang
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#Biol#
55
#Nat#
64
#Cell#
64
#CEL#
64
#Bio#
56