STTT:派安普利单抗和安罗替尼联合白蛋白紫杉醇/吉西他滨(PAAG)治疗转移性胰腺癌:一项前瞻性、多中心、生物分子探索性Ⅱ期试验
2024-07-12 daikun MedSci原创
该研究旨在评估派安普利单抗和安罗替尼与白蛋白紫杉醇/吉西他滨(PAAG)方案在mPC一线治疗中的疗效和安全性,PAAG方案作为mPC一线治疗显示出良好的耐受性和有前景的临床疗效。
胰腺癌是一种常见的消化系统恶性肿瘤,其发病率和死亡率在全球范围内呈上升趋势,预计到2030年,胰腺癌将成为全球癌症相关死亡的第二大原因,目前,晚期转移性胰腺癌(mPC)的治疗仍然以全身化疗为主,但疗效有限,传统的化疗方案,如AG方案(白蛋白紫杉醇/吉西他滨)和FOLFIRINOX方案(奥沙利铂+伊立替康+亚叶酸钙+5-氟尿嘧啶),客观缓解率(ORR)仅为约20%,总生存期(OS)不超过一年,近年来,免疫检查点抑制剂(ICIs)在癌症治疗领域取得了突破性进展,但其临床效益在胰腺癌中尚未得到证实,CISPD3研究和PRINCE研究显示,化疗与ICIs的联合使用可以提高胰腺癌的ORR,达到约50%,表明化疗与免疫治疗的联合具有一定的临床意义。
然而,将ORR的获益转化为OS和PFS的改善仍然是未来研究的关键挑战,肿瘤微环境(TME)在肿瘤的发生发展中起着重要作用,血管生成信号通路激活和肿瘤免疫抑制之间的相互作用已被证实,抗血管生成药物可以通过直接抑制肿瘤生长和转移,并将肿瘤微环境从免疫抑制状态重编程为免疫耐受状态,从而提高免疫治疗的疗效,例如,晚期肝内胆管癌(ICC)患者接受特瑞普利单抗、仑伐替尼和GEMOX方案(吉西他滨+奥沙利铂)的联合治疗,ORR达到80%,DRAGON IV研究也证实了该多药联合方案在局部晚期胃癌中的安全性,并显著提高了病理完全缓解率,考虑到胃肠道肿瘤具有相似的肿瘤微环境,将抗血管生成药物与化疗和免疫治疗联合应用于mPC是合理的,该研究旨在评估派安普利单抗(抗PD-1抗体)和安罗替尼(抗血管生成药物)与白蛋白紫杉醇/吉西他滨(PAAG)方案在mPC一线治疗中的疗效和安全性。

方法
这是一项前瞻性、多中心、单臂、II期临床试验,旨在评估派安普利单抗和安罗替尼与白蛋白紫杉醇/吉西他滨(PAAG)方案在mPC一线治疗中的疗效和安全性,研究纳入了来自中国四家医院的66例mPC患者,纳入患者年龄≥18岁,ECOG体力状态评分为0-1,经组织学或细胞学证实为mPC,具有可测量病灶,患者接受派安普利单抗:200 mg,静脉注射,第1天;安罗替尼:12 mg,口服,每日1次,第1-14天;白蛋白紫杉醇:125 mg/m²,静脉注射,第1、8天;吉西他滨:1.0 g/m²,静脉注射,第1、8天,治疗周期为21天,患者接受8个周期的PAAG治疗,治疗后,完全缓解(CR)、部分缓解(PR)或稳定疾病(SD)的患者继续接受派安普利单抗和安罗替尼的维持治疗,疾病进展(PD)的患者停止治疗,主要终点为客观缓解率(ORR)和疾病控制率(DCR),次要终点为无进展生存期(PFS)、总生存期(OS)和安全性。
研究结果
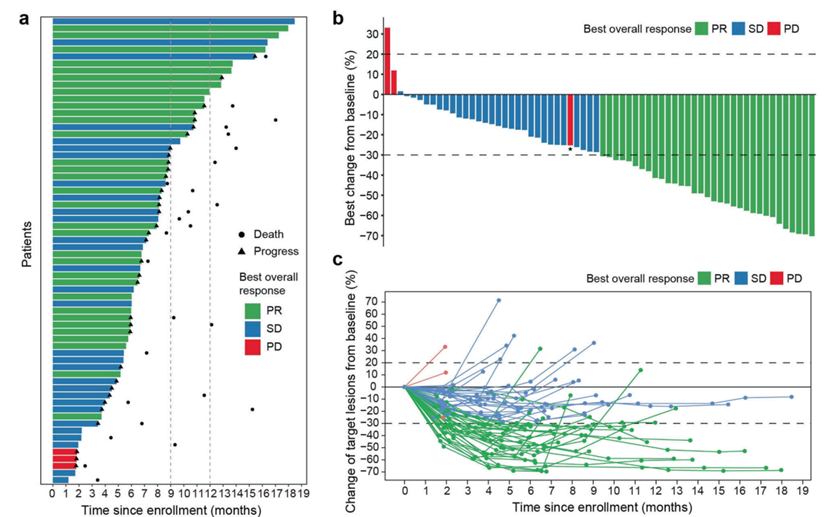
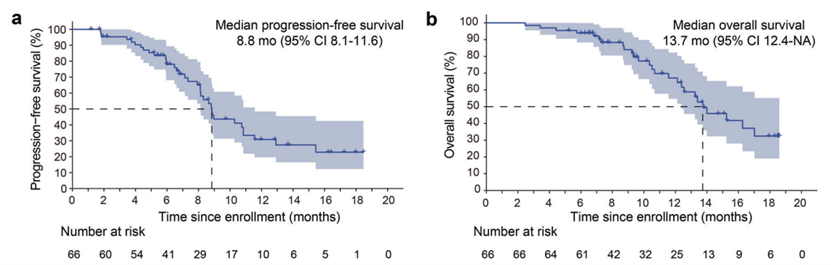
在66例接受疗效评估的患者中,ORR为50.0%(33/66)(95% CI,37.4–62.6%),其中33例患者获得部分缓解(PR),DCR为95.5%(63/66)(95% CI,87.3–99.1%),中位PFS为8.8个月(95% CI,8.1–11.6),中位OS为13.7个月(95% CI,12.4至未达到)。
安全性
所有患者均出现不良反应,最常见的不良反应包括贫血、白细胞减少、疲劳和皮疹,3/4级治疗相关不良事件(TRAEs)发生率为39.4%,其中最常见的是中性粒细胞减少和白细胞减少。
结论
该研究表明,PAAG方案作为mPC一线治疗显示出良好的耐受性和有前景的临床疗效,为mPC一线治疗提供了新的治疗选择,需要开展更大规模的临床研究,进一步验证PAAG方案的有效性和安全性。
原始出处
Sha, H., Tong, F., Ni, J. et al. First-line penpulimab (an anti-PD1 antibody) and anlotinib (an angiogenesis inhibitor) with nab-paclitaxel/gemcitabine (PAAG) in metastatic pancreatic cancer: a prospective, multicentre, biomolecular exploratory, phase II trial. Sig Transduct Target Ther 9, 143 (2024). https://doi.org/10.1038/s41392-024-01857-6.
作者:daikun
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#胰腺癌# #吉西他滨# #安罗替尼# #白蛋白紫杉醇# #派安普利单抗#
71