Hepatology:IL-17和TNF在NLRP3调节肝脏损伤和肝纤维化过程中的作用
2017-09-19 MedSci MedSci原创
研究揭示了TNF和一定程度上的IL-17,是炎症反应和肝纤维化的调节分子。这两种分子由骨髓源性细胞的NLRP3炎症体激活。通过激活NLRP3可阻止肝脏损伤和纤维化进展。
炎症小体-NLRP3,为半胱天冬酶-1的激活体,在调节肝脏炎症和纤维化过程中发挥重要作用。本研究的目的是探究白细胞介素17(IL-17)和肿瘤坏死因子(TNF)是否参与了NLRP3激活后肝脏炎症和纤维化的持续和放大。
该项研究通过IL-17和TNF基因敲除小鼠繁殖得到功能性的Nlrp3A350V基因敲除小鼠,确保Nlrp3A350V基因敲除小鼠的Nlrp3可以在IL-17和TNF基因敲除小鼠中的骨髓来源细胞中被激活。
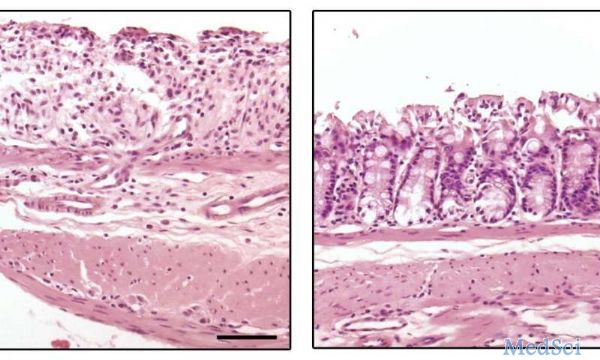
Nlrp3A350V基因敲除小鼠肝脏表现出严重的炎症改变,以中性粒细胞浸润,CXCL1和CXCL2等趋化因子表达增加,巨噬细胞激活,白细胞介素17(IL-17)和TNF表达水平增加为特征。相比完整的Nlrp3A350V突变体,切除IL-17a信号的突变体,中性粒细胞浸润减少;然而,相比未突变IL-17a信号的同窝小鼠,炎症改变仍然显著。与突变的Nlrp3相关的严重炎症变化,在TNF基因敲除后,几乎完全得到缓解,这与血循环IL-1β水平显著下降相关。完整的Nlrp3A350V突变体显示出肝纤维化改变,天狼猩红的形态测量及结缔组织生长因子(CTGF)、基质金属蛋白酶抑制剂-1(TIMP-1)等因子mRNA水平的增加,证明了这一点。相比同窝小鼠,IL-17a缺乏的突变体,肝纤维化得到改善;然而,TNF缺乏的突变体,没有出现纤维化的迹象。
研究揭示了TNF和一定程度上的IL-17,是炎症反应和肝纤维化的调节分子。这两种分子由骨髓源性细胞的NLRP3炎症体激活。通过激活NLRP3可阻止肝脏损伤和纤维化进展。
原始出处:
Wree A, McGeough MD, Inzaugarat ME, et al. NLRP3 inflammasome driven liver injury and fibrosis: Roles of IL- 17 and TNF. Hepatology, 2017, Sep 13. doi: 10.1002/hep.29523.
本文系梅斯医学(MedSci)原创编译整理,转载需授权!
作者:MedSci
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#肝纤维#
37
下载去看原文
84
#肝脏损伤#
47
#IL-17#
30
#损伤#
38