Nat Commun :艾滋病疫苗新理念,回输编程B细胞产生广谱中和抗体
2020-11-25 药学速览 Bio生物世界
艾滋病是一种危害性极大的传染病,它由感染了艾滋病病毒(HIV病毒)引起的。HIV专门攻击人体免疫系统的病毒,它结合于T淋巴细胞的CD4受体以及CCR5辅助受体,大量破坏该细胞,使人体丧失免疫功能。
艾滋病是一种危害性极大的传染病,它由感染了艾滋病病毒(HIV病毒)引起的。HIV专门攻击人体免疫系统的病毒,它结合于T淋巴细胞的CD4受体以及CCR5辅助受体,大量破坏该细胞,使人体丧失免疫功能。因此,患有该疾病的人易于感染各种疾病,并可发生恶性肿瘤,病死率较高。目前针对该疾病的治疗主要是服用抗病毒药物,但是药物不能根除这种病毒感染,因此必须终生服用。
有人可能会问了,既然没有药物来应对病毒感染,开发病毒疫苗不可以么?
为什么还没有HIV病毒疫苗?
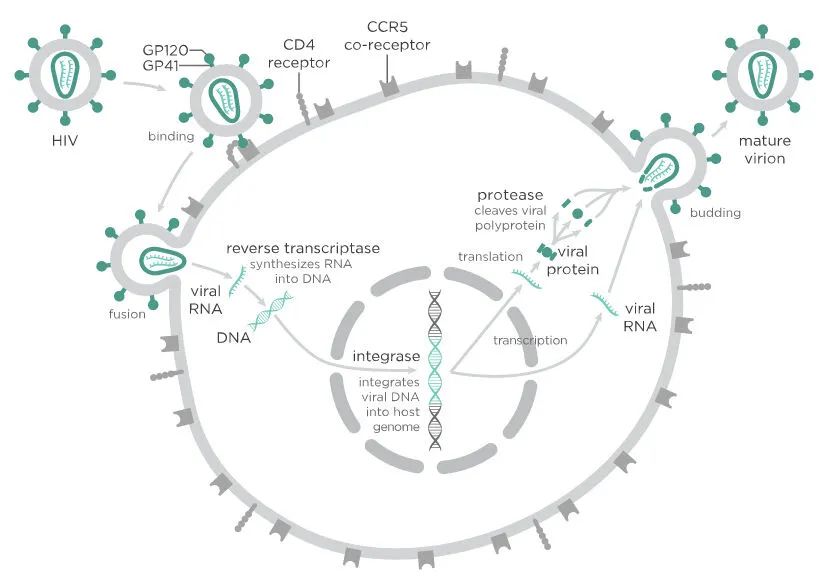
HIV病毒感染细胞过程
开发HIV疫苗难度很大,原因总结有5点:
1、HIV 病毒含有的RNA在被转录为DNA后,会整合到宿主细胞的基因组中,因为免疫系统无法扩展到细胞内部,因此无法识别并清除这段病毒DNA。
2、HIV是变异能力很强的病毒,病毒进入人体后,免疫系统刚刚建立对病毒的保护机制,病毒可能就已经发生了变异,且HIV表达的辅助蛋白Nef可帮助自身逃逸免疫系统的追踪,所以人体很难产生相对应的抗体。
3、HIV病毒外层的特异性刺突膜蛋白覆盖很高的糖基化修饰,即使在病毒感染宿主细胞后将这层蛋白外衣留在了细胞膜上,这些糖蛋白也会隐藏关键抗原决定基的缘故,导致不能有效的激活免疫反应。而且其中像Gp120的刺突蛋白很少,使得HIV能够绕开抗体发挥作用的二价效应(一个抗HIV抗体分子只有同时与两个刺突结合才能有效地发挥中和病毒的作用)。
4、缺少足够数量的非人灵长类动物模型。
5、不能像其他病毒疫苗一样直接使用活病毒作为疫苗成分,因为风险太大,容易造成更多的人感染。
天无绝人之路-HIV广谱中和抗体
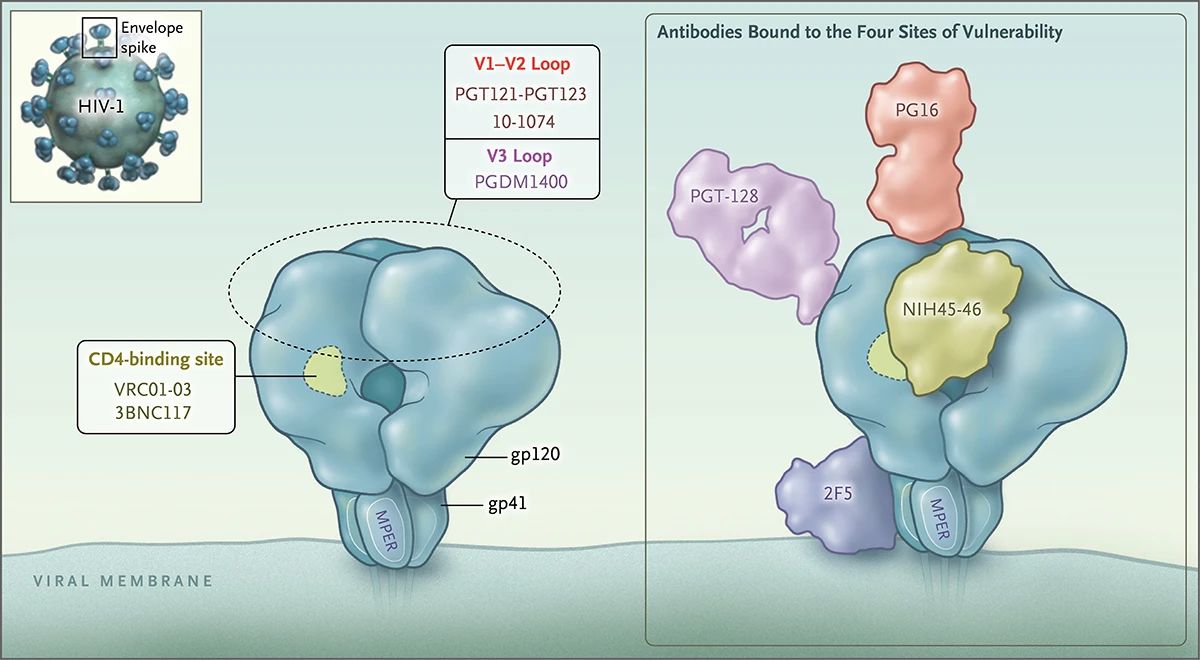
左图:临床开发中单克隆抗体的靶点。右图:四种不同的广谱中和抗体(与靶点)的结合。
研究发现,少量的HIV感染者会产生一些“无敌”抗体-HIV广谱中和抗体(anti-HIV broadly neutralizing antibodies),这些抗体不仅抵抗这些人体内自身携带的HIV毒株,而且也抵抗在全世界传播的不同HIV亚型,研究较多的如VRC01抗体。由于针对该抗体的BCR较少以及其复杂的成熟途径,该抗体的产出变得十分困难。
科学家们一直致力于寻找一种能引起HIV广谱中和抗体产生的HIV疫苗,比如之前有研究利用牛的免疫系统产生抵抗HIV病毒的抗体,这离我们开发一种能够促进人类免疫系统在体内抵抗病毒的疫苗相差甚远。
还有一些将HIV刺突蛋白作为研究对象,设计开发此类蛋白的蛋白疫苗,诱导机体产生抗体,结果显示要么只产生针对特定病毒的抗体,要么就是只产生结合,但没有实质保护作用的抗体,都很难产生较好的广谱中和抗体效果。
因此开发出一种疫苗来诱导可交叉反应的中和抗体被证实是一项相当困难的工作,但仍然是当前HIV-1疫苗研究人员的重要目标之一。
新思路-编程B细胞的活疫苗
最近发表在 Nature Communications 杂志的一项研究,来自Scripps研究所,加州大学圣地亚哥分校以及瑞典斯德哥尔摩大学团队合作开发了一种经体外编程的初代B细胞的过继疫苗,可诱导产生广谱中和抗体的HIV疫苗新策略。
研究团队利用CRISPR技术将HIV中和抗体的可变区整合到小鼠的B细胞基因组产生抗体的特定区域。该B细胞既能产生针对HIV的BCR受体,也能产生分泌型的广谱中和抗体。将编程好的B细胞回输到小鼠体内,丧失免疫的小鼠可产生持久的广谱中和抗体的记忆细胞以及长寿命的浆细胞。
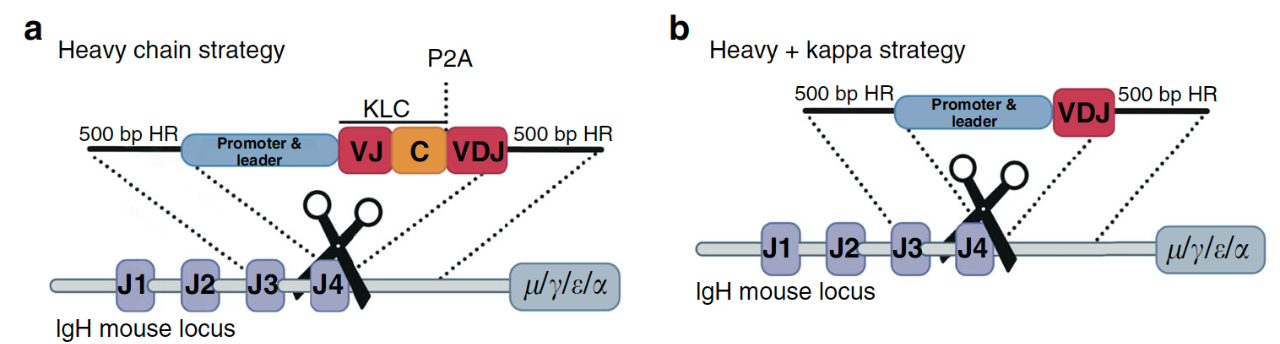
利用CRISPR技术将HIV中和抗体的可变区整合到小鼠的B细胞基因组
该文章的亮点在于能够使用编程的原代B细胞作为疫苗,该工程B细胞能够在体内扩增,且能够诱导产生持久性而且具有亲和力的HIV广谱中和抗体,更为重要的一点是免疫后体细胞超突变表明改造的B细胞有能力来响应一个不断发生突变的病原体。

编程B细胞免疫后产生广谱中和抗体的效果
本文也证实了确实可以被动的将遗传信息转移到适应性免疫系统,是可以编程免疫记忆的。癌症可以用T细胞过继疗法(CAR-T),疫苗免疫也可以用B细胞过继疗法(Engineered-B-vaccine),这将开启被动免疫发展的新篇章。
原始出处:
Deli Huang, Jenny Tuyet Tran, Alex Olson, et al.Vaccine elicitation of HIV broadly neutralizing antibodies from engineered B cells.Nat Commun. 2020 Nov 17;11(1):5850. doi: 10.1038/s41467-020-19650-8.
作者:药学速览
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#COMMUN#
68
#Nat#
74
#B细胞#
76
免疫后体细胞超突变表明改造的B细胞有能力来响应一个不断发生突变的病原体。
135