背景 已有研究证实四价HPV疫苗可以有效预防宫颈高级别上皮内病变,但四价HPV疫苗接种与浸润性宫颈癌患病风险的关系尚未得到充分论证。方法 通过瑞典全国人口和健康登记册随访调查了2006年~2017年间1672983名10~30岁的女性,评估接种HPV疫苗与浸润性宫颈癌患病风险之间的关系,对随访年龄,年限、居住地、父母特征(包括教育程度、家庭收入、母亲出生国、疾病史)等因素进行控制干预。结果19名接种四价HPV疫苗的女性和538名未接种疫苗的女性确诊为宫颈癌,接种疫苗的女性宫颈癌累积发病率为47/105,未接种人群为94/105,调整随访年龄后,接种疫苗组较未接种组宫颈癌发生率占比为0.51(95%CI 0.32-0.82),对其他协变量进行调整后发生率占比为0.37(95%CI 0.21-0.57),对所有协变量进行校正后,17岁之前接种疫苗者发病率占比为0.12(95%CI 0.00-0.34),17~30岁接种疫苗者为0.47(95%CI 0.27-0.75)。结论 接种四价HPV疫苗可显著降低人群中浸润性宫颈癌的发病风险。
HPV疫苗接种的根本目标是通过预防高危HPV感染预防浸润性宫颈癌的发生1。截至2019年12月,共有124个国家和地区将HPV疫苗接种纳入国家免疫计划2,而瑞典HPV四价疫苗接种始于2006年3。既往大量研究(包括功效评估4-6或有效性评价7-13)表明,HPV疫苗可预防HPV感染、生殖道疣以及宫颈高级别上皮内病变,另外,疫苗接种也可预防HPV相关癌症,且不仅仅限于子宫颈癌14,但由于研究周期较长(从HPV感染到临床确诊宫颈癌的时间较长)、接种疫苗后宫颈病变发生风险下降,既往随机对照试验难以评估疫苗对于宫颈癌发病风险的有效性。本研究旨在通过瑞典全国注册数据研究接种HPV疫苗与宫颈浸润癌风险之间的关系。
研究方法
研究人群
瑞典自2007年5月起为13~17岁女孩提供HPV疫苗接种补贴,2012年为13~18岁女孩实施HPV疫苗免费接种政策,为10~12岁女孩制定校园疫苗接种计划3,为23~64岁女性提供基础宫颈癌筛查,每3-7年会根据不同年龄阶段通知复查15。
本研究是通过调查2006年~2017年间瑞典人口登记册开展的队列研究,目标人群是10至30岁女性16,纳入标准是既往未接种HPV疫苗、非浸润性宫颈癌、非移民女性,对所有符合条件的女性进行随访,直到确诊、移民出国、死亡、登记失访、接种HPV二价疫苗。研究得到斯德哥尔摩地区伦理审查委员会的批准,不需要入组人员知情同意。
数据采集
研究使用瑞典全国人口登记册17、HPV疫苗接种登记簿18、处方药登记簿19、国家疫苗接种登记簿20,通过检索HPV疫苗接种记录确定是否接种HPV四价疫苗18。2007年~2012年期间政府四价HPV疫苗接种补贴计划在登记处使用J07BM01代码进行标识,国家疫苗接种登记处20始于2013年,几乎全部覆盖学校HPV疫苗接种计划,浸润性宫颈癌使用代码C53,诊断日期在瑞典癌症登记簿有详细记录21。通过户籍登记表(包含1932年以后在瑞典出生的人口家庭联系信息)22确定参与者的亲生父母和养父母,使用纵向整合数据库进行健康保险和劳动力市场调查父母特征信息23,包括母亲出生国、父母最高教育水平、家庭年收入、母亲CIN3+病史、除宫颈癌以外的其他癌症病史等。
HPV疫苗接种
四价HPV疫苗执行三剂疫苗接种计划,自2015年起学校采用两剂疫苗接种计划,如果研究期间没有接种疫苗,则归类为未接种疫苗人群。对疫苗接种年龄分为17岁以前接种和20岁以前接种两组,评估疫苗接种效果10-13。
敏感性分析
将HPV疫苗接种与出生队列纳入研究,检验是否存在群体效应,为排除HPV疫苗接种时存在宫颈癌的可能性,本研究在接种后1至5年设置的缓冲期(图S4和S5),通过多重插补来解决缺失的协变量数据。
统计分析
在进行分析之前,先评估了宫颈癌发病率的统计功效,设置中位功效为0.94(0.43~1.00),对应的疫苗覆盖率为30%,接种人群假定的发病风险降低70%,每年未接种疫苗人群宫颈癌发病率为4/105人。按照HPV疫苗接种情况,根据随访时的年龄绘制宫颈癌累积发病率曲线,使用泊松回归模型估计发病率占比,比较疫苗接种和未接种女性的宫颈癌发病率,使用SAS 9.4用于功效比较,Stata15.0和R 3.6.3用于所有其他统计分析。
结果
研究人群
本研究共包括1672983名10~30岁女性,其中527871名女性至少接种过一剂HPV疫苗,其中438939(83.2%)例为17岁之前接种,538例未接种疫苗的女性确诊为宫颈癌,疫苗接种者中有19例确诊。

HPV疫苗接种与宫颈癌
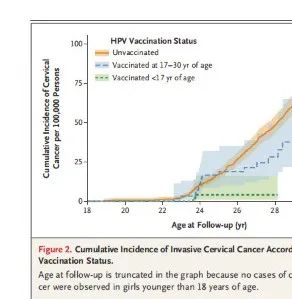
在瑞典,无论是否接种HPV疫苗,23岁后宫颈癌累积发病率迅速增加,故宫颈癌筛查推荐年龄为23岁,30岁时未接种疫苗组宫颈癌累积发病率急剧上升至94/105,疫苗接种组为47/105,17~30岁接种组为54/105人,而17岁前接种组28岁时宫颈癌累计发病率仅为4/105。调整随访年龄后,接种组与未接种组发病率占比为0.51(95%CI 0.32-0.82);按年历、居住地和父母特征进一步调整后,发生率占比为0.37(95%CI 0.21-0.57);按照疫苗接种时年龄分层,17岁前接种组和17-30岁接种组宫颈癌发病率占比分别是0.12(95%CI 0.00-0.34)vs 0.47(95%CI 0.27-0.75),完全校正后的发病率占比20岁前接种组为0.36(95%CI 0.18-0.61),20-30岁接种组为0.38(95%CI0.12-0.72)。
敏感性分析
本研究未发现出生队列与HPV疫苗接种相关宫颈癌发病风险有关联。随着缓冲期的引入,接种HPV疫苗组宫颈癌发病风险始终低于未接种组,接种疫苗组有8例宫颈癌确诊,未接种组有549例,经多次插补后分析,结论大致相同。
讨论
在这项以人群为基础的队列研究中,结果显示四价HPV疫苗接种可显著降低浸润性宫颈癌的发病风险,按接种年龄进行分层分析,小年龄接种组浸润性宫颈癌发病率降低更为明显。
既往研究肯定了HPV疫苗对于HPV感染、生殖器疣和宫颈高级别上皮内病变(CIN2+和CIN3+)的功效4-6和有效性7-13,本研究结果延伸了HPV疫苗的效力,显示HPV四价疫苗可显著降低浸润性宫颈癌的发生风险,这也是HPV疫苗接种的终极目标,疫苗接种的年龄越小,罹患宫颈癌的风险越低。另外,与之前的研究结论一致,接种HPV疫苗降低了尖锐湿疣感染和宫颈高级别上皮内病变的发生10-13。本研究结果还支持在HPV感染之前接种HPV四价疫苗有最大获益,但对接种之前已发生HPV感染没有治疗作用24,25。
一项来自芬兰癌症登记系统的随访研究报道,接种疫苗的女性未发现HPV相关癌症,未接种疫苗的女性中发生10例HPV相关癌症(包括8例宫颈癌),疫苗保护效力达100%(95%CI 16-100)14;来自美国的一项研究表明,15~34岁接种疫苗的女性宫颈癌发病率明显下降26。本研究结论与上述研究相同。
17岁前接种疫苗的女性比未接种者罹患宫颈癌的风险降低88%(66%-100%),在全球范围内HPV16和18型所致的宫颈癌约占70%27,既往观察发现30岁以下的女性中84.4%宫颈浸润癌与HPV16或18型感染有关28,疫苗也可能对其他HPV类型有交叉保护作用。29
如果人群中HPV疫苗接种覆盖率超过50%,未接种疫苗的女性将间接获益。7,有研究证实在瑞典人群中HPV疫苗接种对生殖器疣的群体效应30。本研究发现,1993年之后出生的女性疫苗接种覆盖率至少为50%,但敏感性分析并未观察到宫颈癌风险方面的群体获益,原因可能在于从HPV持续感染到子宫颈癌发生通常经历5到20年的时间31,且随访期间在相关出生队列中浸润性宫颈癌病例极少。
本研究的局限性 在本研究中小部分接种疫苗的女性被错误分类,但潜在更大的担忧是HPV疫苗接种与宫颈癌风险之间的关系存在其他混淆因素,如HPV疫苗接种者通常比未接种者更健康(即健康志愿者偏倚),于是对几个可能与疫苗接种和宫颈癌潜在风险相关的父母特征进行了调整,然而,不能排除生活方式和健康因素的影响(如吸烟、性活动、口服避孕药、肥胖等),这些因素与宫颈癌发病风险也有关联32-34,宫颈癌发生不是仅与HPV疫苗接种独立相关35,36,但对其父母教育水平和家庭年收入的调整也在某种程度上代表了生活方式因素的影响37,健康志愿者偏倚在付费接种疫苗的女性中可能更为突出。此外,接种HPV疫苗的妇女中宫颈癌筛查率较高[38,39],而HPV疫苗接种后CIN2+风险大大低于未接种女性,而对癌前病变的治疗,可能会低估宫颈癌的发病风险6,11,12。由于疫苗接种者观察到的宫颈癌病例很少,无法推断疫苗剂量的影响。
结论:在这项全国性大型研究中,10~30岁女性接种四价HPV疫苗可显著降低浸润性宫颈癌的发病风险。
Lei J, Ploner A, Elfström KM, et al. HPVVaccination and the Risk of Invasive Cervical Cancer. N Engl J Med.2020, 383(14):1340-8

作者:王晓娟 李爱华
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言



.JPG)






#HPV疫苗接种#
58
#疫苗接种#
61
#患病风险#
59
#宫颈#
63
受教
102