ft
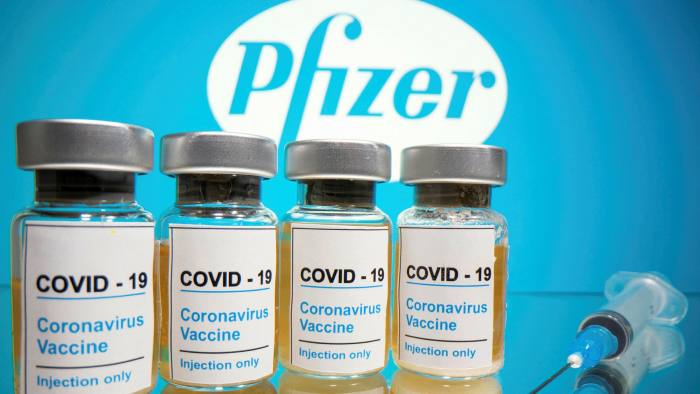
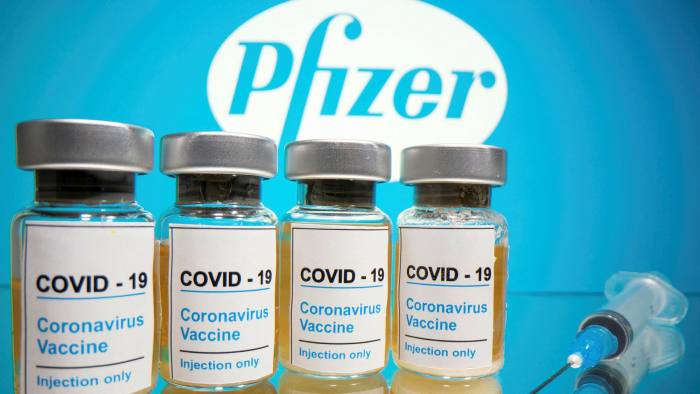
辉瑞公司和德国BioNTech公司共同开发的新冠疫苗被发现具有90%以上的有效性,这是一项重大突破,如果药监部门批准,该疫苗可在今年年底投入使用。

该发现是在第3阶段试验中对新冠疫苗进行首次独立分析的结果,这是商业许可之前的最后试验阶段。所谓的中期分析是在43000多名接受了两剂疫苗或安慰剂的志愿者中,对头94例确诊的Covid-19病例进行了研究。研究发现,只有不到10%的感染是接种疫苗的参与者。超过90%的病例发生在接受安慰剂治疗的患者中。
BNT162b2的3期临床试验于7月27日开始,迄今已招募了43538名参与者,截至2020年11月8日,其中38955名参与者已接受了第二剂候选疫苗。约42%的全球参与者和30%的美国参与者具有不同种族背景。该临床试验正在继续进行中,预计将在总共164例确诊的COVID-19病例中进行最终分析。
这项研究还将评估候选疫苗在先前接触过SARS-CoV-2的人群中提供针对COVID-19的保护的潜力,以及针对严重COVID-19疾病的疫苗预防。除了评估第二次给药后7天确认的COVID-19病例累积的主要功效终点外,现在的最终分析将包括经FDA批准的新的次要终点,其基于第二次给药14天后累积的病例来评估功效剂量也是如此。两家公司认为,增加这些次要终点将有助于使所有COVID-19疫苗研究中的数据保持一致,并允许在这些新型疫苗平台之间进行交叉试验学习和比较。
辉瑞公司表示,继续收集安全性和其他功效数据计划在达到所需的安全标准后不久向美国FDA提交紧急使用授权(EUA),目前预计将在11月的第三周进行。辉瑞发布的结果远远超出了美国食品和药物管理局批准新冠疫苗的标准,该疫苗要求在安慰剂对照试验中至少有50%的功效。根据世界卫生组织,没有一种疫苗是100%有效的。辉瑞股价在纽约盘前交易中上涨了近10%。
辉瑞和BioNTech表示,今年将生产多达5,000万剂这种新的mRNA技术的疫苗,到2021年将再生产13亿剂。
美国已经获得了1亿剂注射剂的订单,可以选择再购买5亿剂,而英国已经同意采购3000万剂。正在就向欧盟提供2亿剂疫苗的交易进行谈判。
作者:JACKZHAO
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#Bio#
76
#TEC#
65
虽然产品不太亲民 但是可喜可贺
120
曙光在前
126
学习了,谢谢分享
119