Cell:放疗,或将改变“癌症免疫疗法”
2016-07-17 生物探索 生物探索
近几年,癌症免疫疗法取得了惊人的发展,而免疫联合疗法已成为这一领域未来必然的发展方向之一。目前,全球制药巨头正积极开展各类免疫联合治疗项目。近日,BMS宣布开展其PD-1抗体Opdivo与PsiOxus公司溶瘤病毒疗法Enadenotucirev的联合用药研究,而“老对手”默沙东为其PD-1抗体Keytruda找的“新朋友”是一款mRNA癌症疫苗。事实上,癌症免疫疗法可找的“搭档”很多,包括化疗、
近几年,癌症免疫疗法取得了惊人的发展,而免疫联合疗法已成为这一领域未来必然的发展方向之一。目前,全球制药巨头正积极开展各类免疫联合治疗项目。近日,BMS宣布开展其PD-1抗体Opdivo与PsiOxus公司溶瘤病毒疗法Enadenotucirev的联合用药研究,而“老对手”默沙东为其PD-1抗体Keytruda找的“新朋友”是一款mRNA癌症疫苗。
事实上,癌症免疫疗法可找的“搭档”很多,包括化疗、放疗、靶向疗法、疫苗等。然而,究竟怎样的联合方案才能真正提高免疫疗法的疗效,扩大适用人群的范围依然在探索中。今年4月,发表在Nature Reviews Cancer上的一篇综述称,基于数以百计正在进行的免疫联合疗法临床试验,未来5-10年,将有一批新的能够提高临床疗效的组合治疗方案产生。
本月初,笔者与大家分享了Cell旗下Trends in Immunology上发表的题为“Targeted Therapy and Checkpoint Immunotherapy Combinations for the Treatment of Cancer”的综述。文章讨论了针对MAPK和VEGF信号通路的靶向疗法与免疫检查点阻断疗法的联合治疗策略。
作者们提出了靶向疗法与免疫疗法的联合框架。他们还指出,靶向疗法能够通过增强癌症-免疫循环中的一些环节(如肿瘤抗原性、T细胞启动/运输/浸润等)对免疫疗法起到协同增强的作用。他们认为,靶向疗法对宿主免疫力的影响可被用于指导和优化更多“靶向-免疫联合疗法”的开发。
放疗:改变免疫疗法这场“游戏”
近日,笔者注意到,Cell旗下Trends in Cancer上发表了题为“Radiotherapy: Changing the Game in Immunotherapy”的观点文章,讨论了放射疗法与免疫疗法的联合治疗策略。
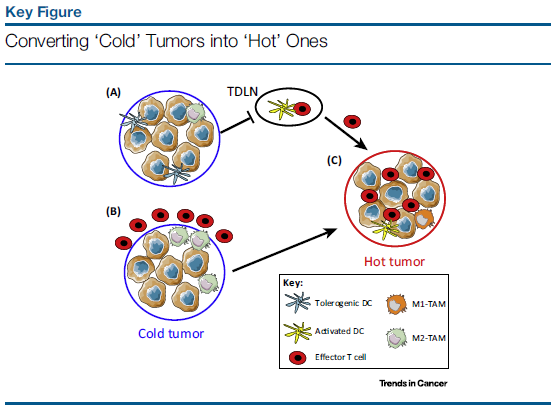
文章指出,免疫检查点抑制剂(Immune checkpoint inhibitors,ICI)在多种类型的癌症治疗中表现出了惊人的疗效。而事实上,预先存在的免疫响应(有效的肿瘤淋巴细胞浸润)是患者对ICI产生响应的先决条件。
在浸润型肿瘤中(被称为“热”肿瘤),ICI能够恢复抗肿瘤T细胞的活性。相反,“冷”肿瘤缺乏淋巴细胞浸润,免疫疗法对此类肿瘤不能发挥作用。临床前数据表明,放疗可以通过招募抗肿瘤T细胞使这些“冷”肿瘤变得对ICI敏感。
尽管越来越多的临床研究开始检测放疗对免疫疗法的增强作用,但借助放疗将“冷”肿瘤变成“热”肿瘤的临床证据依然难以捉摸。在这一文章中,作者们汇总了一些新证据。这些证据表明,放射治疗不仅是免疫疗法疗效的强化剂,而且是“游戏的改变者”。
文章总结了五大趋势(Trends):
1) 免疫疗法的出现使癌症治疗发生了革命性的变化。在转移性癌症患者中,免疫疗法通过阻断免疫抑制通路表现出了显著、持久的响应。
2) 在大多数患者中,如果不预先利用治疗诱导产生新的抗肿瘤免疫响应,阻断免疫抑制是无效的。
3) 在响应免疫疗法的患者中,T细胞会识别独特的neoantigens,这意味着肿瘤疫苗需要高度的个性化。
4)一些新数据表明,放疗能够将病人的自身肿瘤转变为原位疫苗(in situ vaccine),为开发放疗-免疫联合疗法提供了依据。
5) 研究发现,通过对癌症患者进行局部放疗可产生成功的个体化免疫。这为增强患者对免疫疗法的响应提供了一种简单的、具有成本效益的方法。
文章正文部分讨论了放疗剂量和分级(Fractionation)的影响,汇总了从临床试验中获得的经验教训,探讨了如何将临床前模型整合到临床研究中,以及如何通过临床试验设计证明放疗在免疫治疗响应中的贡献。
结论
利用放疗增强免疫疗法的疗效是一个令人兴奋的、革命性的概念。但是,在真正将这种联合疗法应用到患者治疗中之前还有许多问题需要进一步研究。作者们相信,癌症免疫治疗领域的进步需要这种创新的研究。
他们还指出,近阶段,联合免疫疗法与放疗的临床研究快速增长,但如果缺乏严格的试验设计,可能会无法探索出这一联合治疗方案的真正潜力,并影响这一领域的发展。此外,随着新型的免疫疗法快速加入到临床实践中,探索如何将放疗生物学和肿瘤免疫学进行最好的整合依然非常紧迫。
原始出处
Sandra Demariacorrespondenceemail, C. Norman Coleman, Silvia C. Formenti.Radiotherapy: Changing the Game in Immunotherapy.cell.2016
作者:生物探索
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#Cell#
65
#CEL#
88
不要以为有T就行,有效针对或的癌细胞的T才行!
91
进去的T细胞到处寻找释放新抗原的细胞,原来是死亡中的癌细胞,一口吞下去。边上的正常癌细胞表面没有这个新抗原,T们是“诚心诚意”的视而不见。期待中的生力军只是吃死尸的食腐动物,是收尸队。我不知道何喜之有??
99
进去的T细胞到处寻找释放新抗原的细胞,原来是死亡中的癌细胞,一口吞下去。边上的正常癌细胞表面没有这个新抗原,T们是“诚心诚意”的视而不见。期待中的生力军只是吃死尸的食腐动物,是收尸队。我不知道何喜之有??
4