FDA延长法布雷病治疗药物长效α-半乳糖苷酶A产品pegunigalsidase alfa审查周期
2020-12-02 网络 网络
Protalix BioTherapeutics是一家致力于开发、生产和商业化由其专有的ProCellEx®植物细胞蛋白表达系统生产的重组治疗蛋白的生物制药公司。近日,该公司与合作伙Chies
Protalix BioTherapeutics是一家致力于开发、生产和商业化由其专有的ProCellEx®植物细胞蛋白表达系统生产的重组治疗蛋白的生物制药公司。近日,该公司与合作伙Chiesi Group旗下公司Chiesi Global Rare Diseases联合宣布,美国食品和药物管理局(FDA)已将pegunigalsidase alfa(PRX–102)生物制品许可申请(BLA)的《处方药用户收费法》(PDUFA)目标日期延长3个月,由2021年1月27日延长至2021年4月27日。
pegunigalsidase alfa是一种长效、重组、聚乙二醇化、交联α-半乳糖苷酶A,用于治疗法布雷病(Fabry disease)成人患者。在2018年1月,FDA已授予了pegunigalsidase alfa快速通道资格(FTD)。
正如之前所宣布的那样,FDA受理了BLA并根据加速审批程序授予了优先审查。FDA表示,目前不打算召开咨询委员会会议来讨论申请。
BLA提交材料包括了来自临床前、临床和制造的一套完整数据,包括已完成pegunigalsidase alfa的I/II期临床试验、继I/II期临床试验之后的相关扩展研究,III期BRIDGE转换研究的中期临床数据、正在进行的评估pegunigalsidase alfa每隔一周1mg/kg的治疗研究。
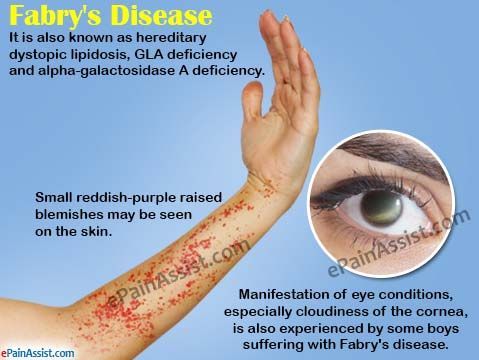
法布雷病(Fabry disease)是一种X连锁遗传性疾病,缺陷基因位于X染色体长臂上。该病是由于α-半乳糖甘酶基因缺陷,造成溶酶体中α半乳糖苷酶(α–Galactosidase)活性缺陷,导致一种名为酰基鞘鞍醇三己糖 (globotriaosylceramide, Gb3)的脂肪物质在全身血管壁上不断累积。
法布雷病是一种罕见病,每4万-6万人中有一人患病。患者α-半乳糖苷酶存在缺陷,该酶通常负责Gb3的分解。Gb3的异常蓄积随时间的推移而增加,因此,Gb3主要在血液和血管壁中积聚。Gb3沉积的最终后果包括从疼痛和周围感觉受损,到器官衰竭,尤其是肾脏,也包括心脏和脑血管系统。
pegunigalsidase alfa(PRX-102)是一种植物细胞培养表达的、化学修饰的稳定版本的重组α-半乳糖苷酶-A酶。蛋白质亚基之间利用短的PEG进行化学交联进行共价结合,形成具有独特药代动力学参数的分子。在临床研究中,pegunigalsidase alfa的循环半衰期约为80小时。pegunigalsidase alfa的开发,旨在解决法布里患者群体中持续未满足的临床需求。
Protalix公司专注于通过其专有的植物细胞表达系统ProCellEx®开发和商业化重组治疗蛋白。Protalix是第一家获得美国食品和药物管理局(FDA)批准通过植物细胞悬浮表达系统生产蛋白质的公司。Protalix独特的表达系统代表了一种以工业规模的方式开发重组蛋白的新方法。
该公司生产的第一个产品,taliglucerase alfa(Elelyso),于2012年5月被美国FDA批准上市,随后也被其他国家的监管机构批准上市,作为一种长期的酶替代疗法(ERT),用于治疗1型戈谢病成人及儿科患者。Protalix已向辉瑞公司授予了taliglucerase alfa的全球开发和商业化权利,Protalix在巴西保留全部权利。
目前,Protalix公司管线中包括针对现有医药市场重组治疗蛋白的专有版本,包括:(1)pegunigalsidase alfa,重组人α-半乳糖苷酶的改良版本,用于治疗法布里病;(2)OPRX–106,一种用于治疗法布里病的蛋白质口服抗炎疗法;(3)alidornase alfa,治疗囊性纤维化;(4)PRX–115,一种植物细胞表达的重组聚乙二醇尿酸酶,治疗痛风。Protalix与Chiesi在美国和美国以外地区合作开发和商业化pegunigalsidase alfa。
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






#治疗药物#
38
#ALF#
50
#PE#
30
#IgA#
38
#PEG#
41