知临集团用于治疗神经母细胞瘤的再利用药物 SACT-1 获得FDA孤儿药资格
2022-01-21 国际文传 网络
知临集团计划提交一份试研究药物申请(IND),于 2022 年开始 SACT-1 的 1b/2a 期临床试验,在神经母细胞瘤患者中测试该药物。
临床阶段生物制药公司知临集团有限公司(纳斯达克代码:APM,巴黎泛欧证券交易所代码:APM)(“知临集团”或“知临”)欣然宣布,美国食品药品监督管理局 (FDA) 办公室已授予 SACT-1 孤儿药资格。SACT-1是一种再利用小分子混合物,用于治疗神经母细胞瘤患者。知临集团计划提交一份试研究药物申请(IND),于 2022 年开始 SACT-1 的 1b/2a 期临床试验,在神经母细胞瘤患者中测试该药物。
知临集团总裁兼执行董事雷宏业先生表示:“授予 SACT-1 用于治疗神经母细胞瘤的孤儿药资格是我们候选药物开发过程中向前迈出的重要一步, FDA 和知临皆显示出对解决神经母细胞瘤患者未解决的临床需求的承诺。继我们最近宣布完成 SACT-1 的 1 期临床试验和专利授权之后,我们目前正专注于IND 准备工作,以在美国展开令人兴奋的 SACT-1 的 1b/2a 期临床试验。”
关于SACT-1
SACT-1 是一种用于治疗神经母细胞瘤的口服改用小分子药物。我们的临床前研究已经研究了 SACT-1 的机制,以增强肿瘤细胞死亡和抑制 MYCN 表达(这是通常观察到 MYCN 扩增的高风险或复发性神经母细胞瘤患者的常见临床诊断)。 SACT-1 特别被设计用于与标准护理化疗结合使用。
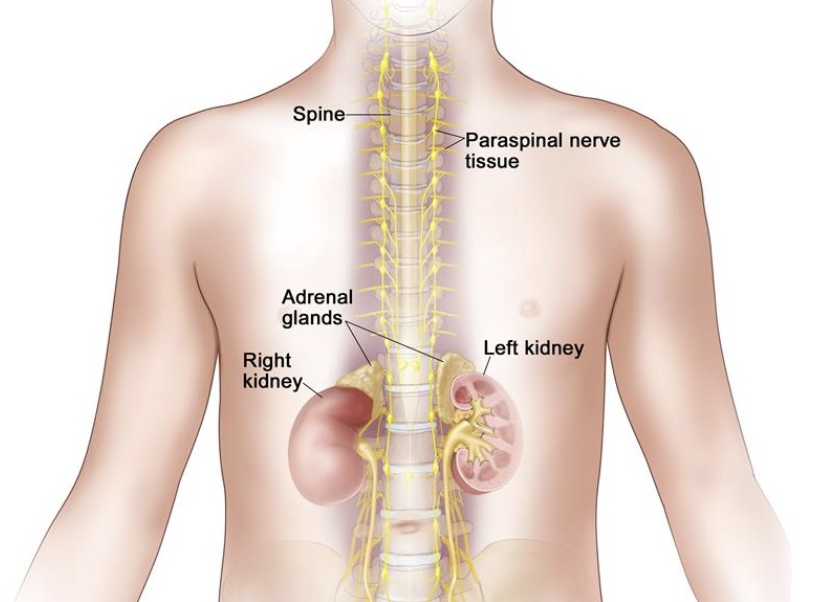
关于神经母细胞瘤
神经母细胞瘤是儿童中最常见的实体瘤之一,占所有儿童肿瘤的 8% - 10%,占儿科人群中所有癌症相关死亡的 15%1。对于高危患者群体,根据美国癌症协会2基于现有治疗的观察,这种疾病的 5 年生存率约为 40-50%。
2 https://www.cancer.org/cancer/neuroblastoma/detection-diagnosis-staging/survival-rates.html
作者:国际文传
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#母细胞瘤#
68
#细胞瘤#
74
好文章,谢谢分享。
118
统性红斑狼疮(Systemic lupus erythematosus, SLE)是一种慢性自身免
83