JCO | FDA批准摘要:elacestrant 用于治疗ER阳性、HER2阴性、ESR1突变晚期或转移性乳腺癌
2024-03-18 daikun MedSci原创
基于Ⅲ期EMERALD研究,FDA批准了Elacestrant用于存在ESR1突变的ER阳性、HER2阴性晚期或转移性乳腺癌患者,成为该类患者的新口服内分泌治疗选择。
ER阳性、HER2阴性晚期或转移性乳腺癌是一种不可治愈的严重疾病,当前治疗选择有限,通常采用内分泌治疗,约20-40%的患者在接受一线内分泌治疗后会出现ESR1突变,这会导致对内分泌治疗产生耐药,在Elacestrant出现之前,尚无针对ER阳性、HER2阴性、ESR1突变晚期或转移性乳腺癌的获批口服雌激素受体拮抗剂,Elacestrant是一种口服雌激素受体拮抗剂,可以降解ERα,具有抗肿瘤活性,初步研究显示,Elacestrant可能对存在ESR1突变的乳腺癌患者更有效,EMERALD是一项随机对照试验,结果显示,Elacestrant可以显著延长存在ESR1突变患者的PFS,且安全性可接受,因此,FDA批准了Elacestrant用于存在ESR1突变的ER阳性、HER2阴性晚期或转移性乳腺癌患者,成为该类患者的新口服内分泌治疗选择。

方法
EMERALD一项随机、开放标签、活性对照、多中心的临床试验,共纳入478例ER阳性、HER2阴性晚期或转移性乳腺癌患者,包括228例存在ESR1突变的患者,患者按1:1比例随机分配至Elacestrant组(345mg口服,每日一次,n=239)或研究者选择的内分泌治疗(SOC, n=239),研究的主要终点是无进展生存期(PFS),在存在ESR1突变患者组和所有患者组(意向治疗人群)进行评估。

研究结果
存在ESR1突变的患者:Elacestrant显著改善了该亚组患者的PFS,危险比(HR)为0.55 (95% CI 0.39-0.77),中位PFS为3.8个月,而SOC为1.9个月。总生存期(OS)趋势:该亚组患者的OS没有显著改善,但也没有发现潜在的损害趋势,HR为0.90 (95% CI 0.63-1.30)。所有患者(意向治疗人群):Elacestrant也显著改善了所有患者的PFS,HR为0.70 (95% CI 0.55-0.88),但主要归因于存在ESR1突变的患者。无ESR1突变的患者:Elacestrant在该亚组患者的PFS改善较小,HR为0.86 (95% CI 0.63-1.19),中位PFS为1.9个月,而SOC为2.0个月。总体响应率:Elacestrant和SOC的总体响应率较低,存在ESR1突变的患者中Elacestrant略高。

安全性
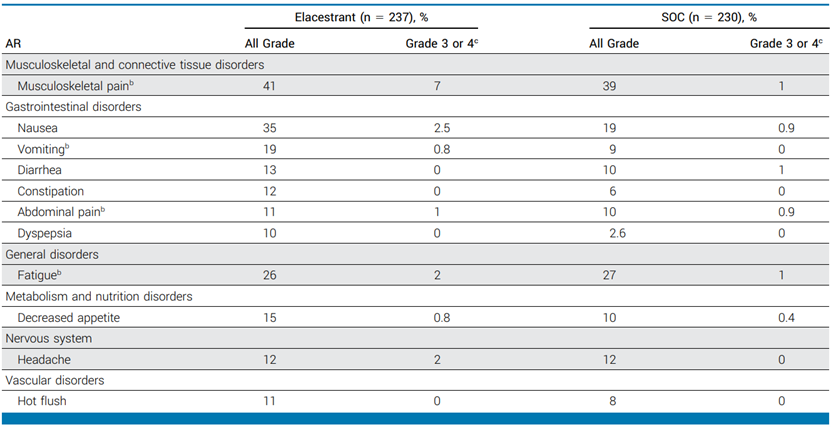
在EMERALD临床试验中,467例患者接受了至少一剂Elacestrant,大多数不良事件为1-2级,符合内分泌治疗的预期,Elacestrant组较对照组的不良事件发生率更高,包括恶心(35% vs 19%)、呕吐(19% vs 9%)、食欲减退(15% vs 10%)和消化不良(10% vs 2.6%),Elacestrant组中更常使用血清素受体拮抗剂(17% vs 10%),Elacestrant组较对照组更常出现血脂异常,包括高甘油三酯血症(30% vs 17%)和高胆固醇血症(27% vs 15%),Elacestrant组中只有1例4级不良事件,即血脂异常,Elacestrant组的剂量中断(15%)、剂量降低(3%)和药物停用(6%)发生率略高于对照组,动物重复给药毒性试验显示,Elacestrant可引起生殖器官毒性,包括卵巢囊肿、生殖器萎缩等,可能影响生育能力,胚胎发育毒性试验表明,Elacestrant具有致畸作用,因此在标签中增加了胚胎毒性的警告,Elacestrant的安全性总体可接受,可通过标签中的警告和注意事项进行管理。
结论
Elacestrant显著改善了存在ESR1突变患者的PFS,而总生存期趋势也良好,Elacestrant的毒性可接受,可以通过标签管理,Elacestrant提供了口服给药的新选择,为患者带来便利。对于无ESR1突变的患者,Elacestrant的PFS改善较小,安全性也不确定,因此FDA未批准该亚组使用。尽管Elacestrant的PFS改善幅度不大,但作为存在ESR1突变患者的新口服内分泌治疗选择,具有临床意义,Elacestrant还需要进行进一步研究,以确定其在不同人群中的效果。基于该临床研究,FDA批准Elacestrant用于存在ESR1突变的ER阳性、HER2阴性晚期或转移性乳腺癌患者,标志着该类患者的新口服内分泌治疗选择。
原始出处
Mirat Shah et al., US Food and Drug Administration Approval Summary: Elacestrant for Estrogen Receptor–Positive, Human Epidermal Growth Factor Receptor 2–Negative, ESR1-Mutated Advanced or Metastatic Breast Cancer. JCO 0, JCO.23.02112.DOI:10.1200/JCO.23.02112.
作者:daikun
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






#Elacestrant# #ESR1突变# #乳腺癌#
23