病例简介
一般情况
老年男性,78岁,体重55 kg。
主诉
活动后胸骨后烧灼感1年,加重1个月。
既往史
入院检查
血红蛋白100 g/L;血肌酐117.2 μmol/L;估计肾小球滤过率37 ml/min。超声心动图:主动脉瓣硬化、二尖瓣反流(少量),射血分数63%。
入院诊断
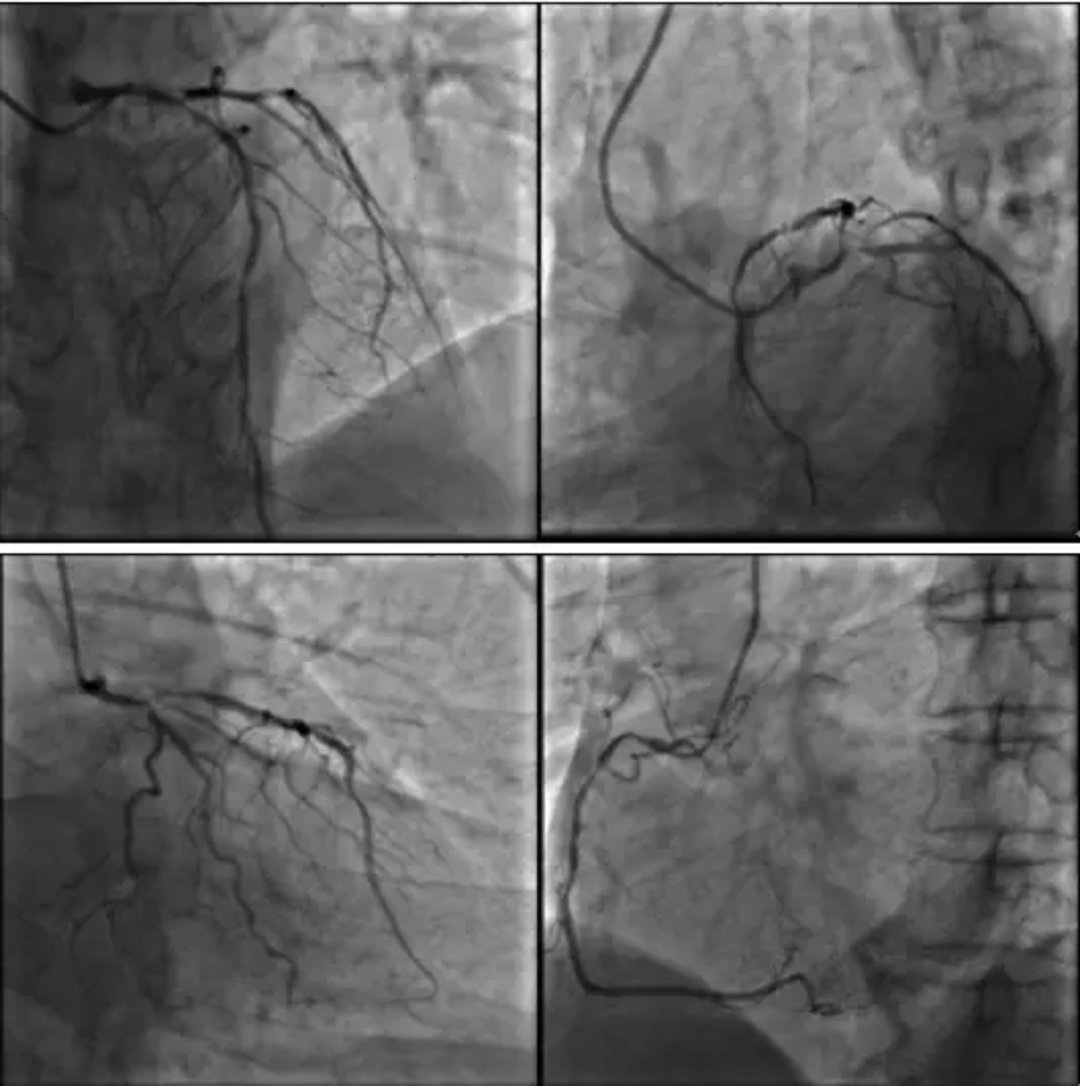
冠脉造影
左主干(LM):体部可见外膜钙化;
左前降支(LAD):开口-近段重度狭窄,伴有严重钙化;
回旋支(LCX):开口重度狭窄,伴有严重钙化;
钝缘支(OM):开口、近段重度狭窄;
右冠状动脉(RCA):近段、中段弥漫长病变,重度狭窄。
治疗过程
治疗策略
(1)对该患者进行冠脉病变评估,SYNTAX 评分38分;

(2)外科搭桥 or内科介入治疗? 建议首选外科搭桥,但患者及家属拒绝;
(3)内科介入治疗策略:术中体外膜肺氧合(ECMO)循环支持下,旋磨处理钙化病变, LM、LAD、LCX分叉病变采用DK-CRUSH术式。

根据术前超声评估血管情况选择入路
ECMO 入路:右侧股动脉置入17F导管,右侧股静脉置入21F导管,ECMO起始转速为2700转/分,泵流量为2.5 L/min。
介入治疗入路:右侧桡动脉置入7F鞘管;使用7F EBU 3.0。
PCI过程
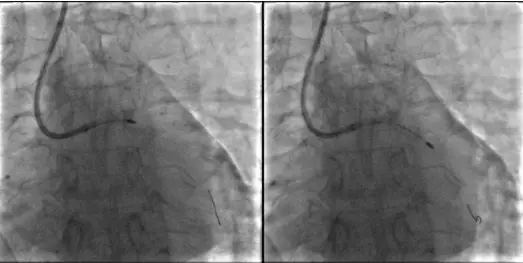
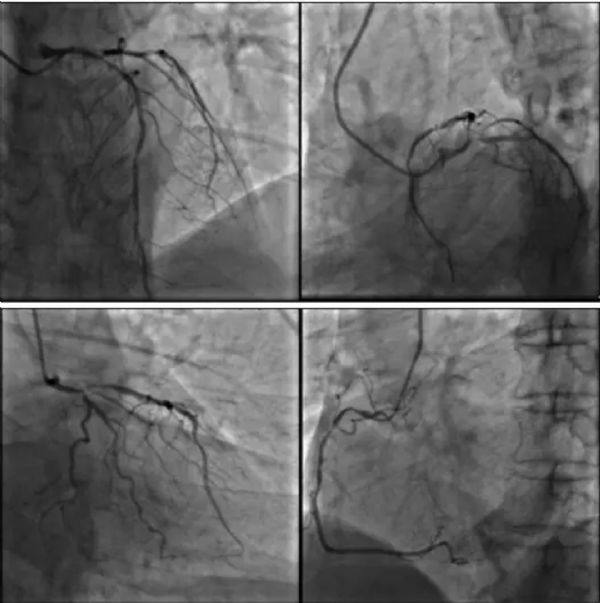
首先对LM-LAD严重钙化病变进行旋磨治疗
(1)导丝、微导管通过:将Runthrough NS导丝送至LAD血管远端,Finecross微导管难以通过病变段。使用球囊Tazuna(1.25×15 mm)预扩张后,微导管艰难通过病变段,送至LAD远端,交换为旋磨导丝。
(2)旋磨:先使用直径1.25 mm旋磨头进行旋磨5次,但旋磨头始终无法通过LAD近段重度狭窄段,提示该处病变的钙化、狭窄严重。在旋磨10次时,最终通过LAD近段重度狭窄段。之后继续使用1.5 mm的旋磨头进行旋磨5次。
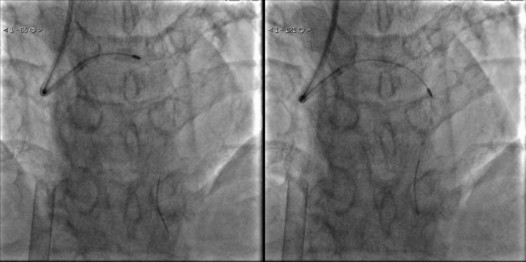
(3)血管内超声(IVUS)评估病变:使用IVUS评估LM-LAD病变发现,钙化环消减不完全。
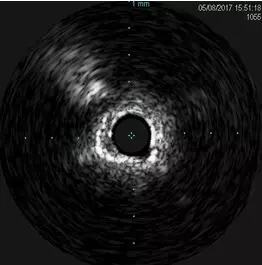
(4)更换更大直径旋磨头(1.75 mm)进行旋磨治疗5次。
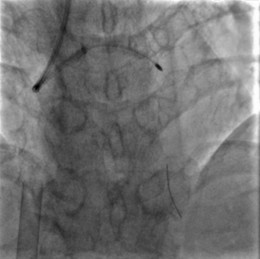
随后对LM-LCX严重钙化病变进行旋磨治疗
(5)预扩张OM开口病变:考虑到OM开口重度狭窄,首先以Tazuna球囊(1.25×15 mm,14 atm),Sprinter球囊(2.0×15 mm,10 atm)对LCX开口-OM近段进行扩张。球囊于LCX开口处无法完全膨胀,IVUS亦无法通过LCX开口,提示LCX开口严重钙化。
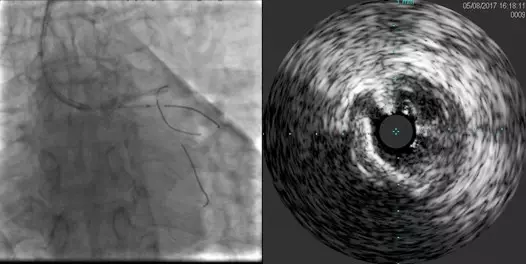
(6)使用直径1.25 mm的旋磨头对LCX开口、近段进行旋磨。
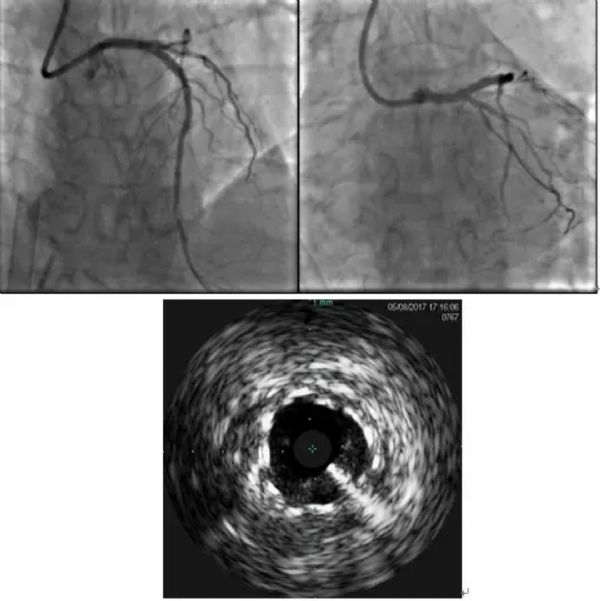
(7)植入支架:LAD中段植入支架1 Xience Xpedition(2.5×38 mm);
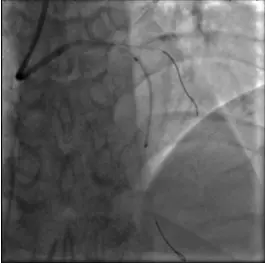
使用DK-CRUSH术式处理LM分叉病变,于LCX开口、近段植入支架2 Endeavor Resolute(2.25×14 mm);
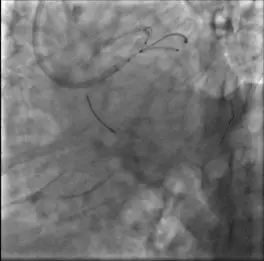
于LAD近段至LM体部植入支架3 Endeavor Resolute(3.5×30 mm);
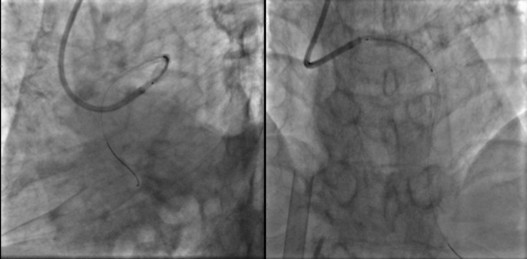
DK-CRUSH过程中对吻2次。

(8)最终造影结果并复查IVUS,提示支架均贴壁良好。
术后评估
术中患者循环平稳,未诉特殊不适。术后观察患者2小时,生命体征平稳,即刻拔除股动脉、股静脉置管,减少ECMO相关血管并发症。冠心病重症监护室(CCU)病房观察2日后,患者情况稳定,转入普通病房,拟择期行RCA介入治疗。
小结
本例患者高龄(78岁)、低体重(55 kg),基础疾病复杂(高血压、糖尿病、贫血、肾功能不全),且冠脉病变弥漫,对介入治疗的技术要求高。尤其是治疗中需要分别对LAD、LCX的严重钙化病变进行旋磨,这意味着旋磨的同时,LCX和LAD会先后在一段时间内处于无导丝保护状态,存在术中发生急性闭塞并进而导致患者循环崩溃的风险。
针对这一类复杂、高危但有介入治疗指征(CHIP)的患者, 目前国内外指南推荐机械循环辅助支持下完成介入治疗。因此,本中心选择在ECMO支持下完成介入治疗,可以有效降低CHIP术中风险,提高手术成功率,改善患者预后。
专家简介:
作者:郑金刚 董哲
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
小提示:本篇资讯需要登录阅读,点击跳转登录









#左主干#
78
#CMO#
86
左主干分叉病变的介入治疗,厉害!
126
#分叉病变#
104
好文章学习了
118