AACR 2022:度伐利尤单抗和和曲美木单抗联合一线新辅助化疗治疗晚期卵巢癌患者的结果公布 (KGOG 3046/TRU-D)
2022-04-11 网络 网络
2020年1月,美国食品药品监督管理局(FDA)授予阿斯利康的PD-L1抑制剂度伐利尤单抗(Durvalumab,Imfinzi)和CTLA-4抑制剂曲美木单抗(tremelimumab)一线治疗肝细
2020年1月,美国食品药品监督管理局(FDA)授予阿斯利康的PD-L1抑制剂度伐利尤单抗(Durvalumab,Imfinzi)和CTLA-4抑制剂曲美木单抗(tremelimumab)一线治疗肝细胞癌(HCC)的孤儿药资格。从此,二药联合应用在多种瘤种中取得不错的效果。这一次是挑战晚期卵巢癌。
KGOG 3046是一项评估双重免疫检查点抑制(度伐利尤单抗 [D]和曲美木单抗 [T])与新辅助化疗(NAC)联合治疗晚期前上皮性卵巢癌(aEOC)的单臂2期研究。该研究招募了FIGO IIIC-IV期上皮卵巢癌患者,旨在评估双免疫治疗+化疗用于晚期上皮性卵巢癌新辅助治疗的疗效和安全性。
合格患者被分配到以下新辅助化学免疫疗法(NACI):原始队列1组(度伐利尤单抗 1500 mg q3w + 曲美木单抗 75 mg q3w + 紫杉醇175 mg/㎡ + 卡铂AUC 5 [3个周期])或扩展队列2组(度伐利尤单抗 1500 mg q3w + 曲美木单抗 300 mg [1个剂量] + 原始化疗),组2在组1完成后再开始。在新辅助化疗之后,所有患者都接受了间歇性肿瘤细胞减灭术(IDS)。手术后再接受3周期辅助治疗:度伐利尤单抗(1120mg)+化疗,序贯度伐利尤单抗维持治疗(1120mg)。主要终点为12个月PFS率。
在治疗期间,通过进行一系列的活组织检查探究肿瘤微环境(TME)的免疫学变化。该研究主要终点是12个月的无进展生存期。在所有患者接受间歇性肿瘤细胞减灭术治疗后,对他们进行中期分析来评估新辅助化疗后的效果。
去年公布的是期中分析结果,显示:共23例患者纳入研究,中位年龄为60岁.大多数(87.0%)患者为高级别浆液性卵巢癌,60.9%患者为IV期。新辅助治疗后,3例(13%)患者达到完全缓解(CR),20例患者达到部分缓解(PR)。IDS期间,17例(73.9%)患者实现RO切除。4例(17.4%)患者达到病理完全缓解。
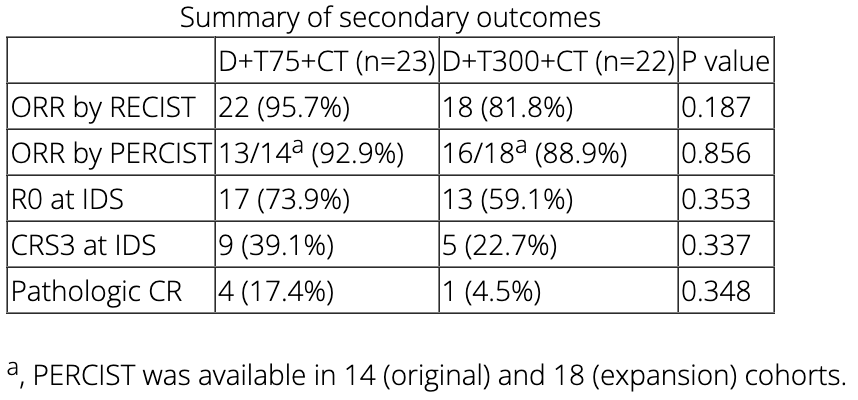
本次公布的是45名患者,具体如下:组1(n=23)和组2(n=22)。大多数患者表现为高级别浆液性癌(91.1%)和四期疾病(77.8%)。在新辅助化疗之后,根据实体瘤的疗效评价标准(RECIST 1.1),客观缓解率为86.7%(第一组为95.7%,第二组为81.8%,P=0.17)。在间歇性肿瘤细胞减灭术中,30名患者(66.7%)为完整切除(第一组73.9%,第二组59.1%,P=0.353)。14名患者(31.1%)的化疗反应评分为3级(1组为39.1%,2组为22.7%,P=0.337),5名患者(11.1%)病理缓解。皮疹是这其中最常见的不良事件(51.1%),3名患者(15.6%)发生≥3级事件,但在使用类固醇后症状完全缓解。
新辅助免疫联合化疗后,免疫组化结果显示间质肿瘤浸润淋巴细胞(P=0.0335)、CD8(P<0.001)、CD8/Foxp3比例(P<0.001)明显增加。使用流式详细分析肿瘤浸润免疫细胞发现,新辅助免疫联合化疗后两组的抑制性瘤内调节性T细胞(Treg)都明显减少(P<0.05)。有趣的是,新辅助免疫联合化疗后肿瘤内Treg的比率组1比组2低(P<0.05)。
目前这些数据突出显示了在晚期上皮性卵巢癌的新辅助化疗中加入度伐利尤单抗和曲美木单抗的临床活性和可控毒性。其他的转化医学研究数据将在会议上公布。
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言





#新辅助#
93
#结果公布#
95
#晚期卵巢癌#
92
#ACR#
112
#AACR#
68