【BJH】全口服诱导方案治疗高危APL的回顾性研究:口服依托泊苷替代静脉化疗
2024-05-06 聊聊血液 聊聊血液
北京大学人民医院学者开展一项纳入60例高危APL患者的回顾性研究,探讨了口服VP16替代静脉化疗的有效性和安全性。
高危APL全口服诱导方案
随着全反式维甲酸(ATRA)和砷剂的使用,急性早幼粒细胞白血病(APL)已成为一种可治愈的疾病,但其中约有20%为高危(白细胞计数[WBC] >10×109/L)。ATRA +三氧化二砷(ATO)+细胞毒性化疗是高危APL患者的一线治疗方法,此外ATRA联合口服砷剂(复方黄黛片[RIF])的全口服方案对APL患者也能达到类似的治疗效果。因此,在中国APL诊疗指南(2018)中,口服砷剂(RIF) +ATRA+细胞毒化疗也是高危APL的一线治疗。
数年前由于COVID-19大流行,迫切需要一种口服、高效、安全的高危APL治疗方案。鉴于口服依托泊苷(VP16) 在高危APL中的个案报道,证明其替代细胞毒化疗作为诱导治疗的有效性、安全性和便捷性。因此,北京大学人民医院学者开展一项纳入60例高危APL患者的回顾性研究,探讨了口服VP16替代静脉化疗的有效性和安全性。研究结果近日发表于《British Journal of Haematology》。

研究方法
根据中国APL诊断和治疗指南,根据形态学特征怀疑APL时立即给予ATRA (25 mg/m2/d)。确认PML-RARA融合基因或t(15;17)易位后给予RIF (60 mg/kg/d)。由于APL诊断的遗传或染色体确认通常需要5-7天,砷剂应用的开始时间大约比ATRA晚5-7天。ATRA加RIF继续使用,直到达到血液学完全缓解(CR)。
当根据形态学特征怀疑为高危APL时立即给予口服VP16 (治疗前WBC计数为10-20×109/L患者 为50mg/bid;治疗前WBC计数>20×109/L患者为50mg tid),WBC下降到≤10×109/L时停止治疗。
在历史对照组,立即使用蒽环类药物(柔红霉素45mg /m2/d或伊达比星8mg /m2/d, d1-3)和/或阿糖胞苷100mg/d进行静脉化疗,WBC降至≤10×109/L时停用。
研究结果
患者
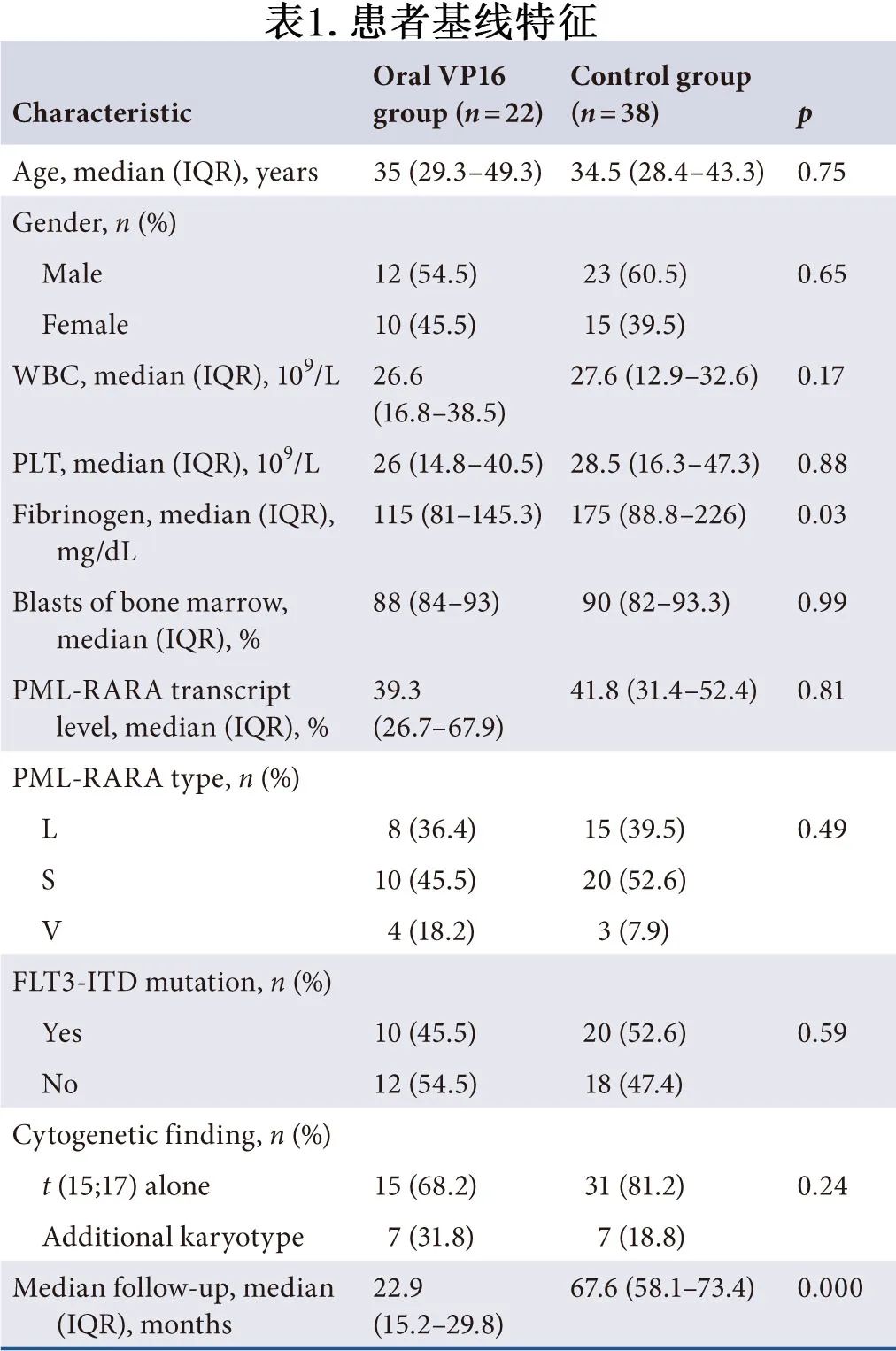
研究共纳入60例高危APL患者;22例患者于2020年2月至2022年7月接受口服VP16作为细胞减灭化疗联合ATRA和RIF诱导治疗,另外38例患者于2017年1月至2019年12月接受静脉细胞减灭化疗联合ATRA和RIF诱导治疗作为历史对照组。患者的基本特征见表1。口服VP16组患者的中位年龄为35岁,对照组为35岁(p=0.75)。除了口服VP16组基线纤维蛋白原中位数水平较低[115 mg/dL vs 175 mg/dL;P=0.03)],两组其他基线特征相似。截至2023年5月,中位随访56.6个月。口服VP16组和对照组的中位随访时间分别为22.9个月和67.4个月。
诱导治疗
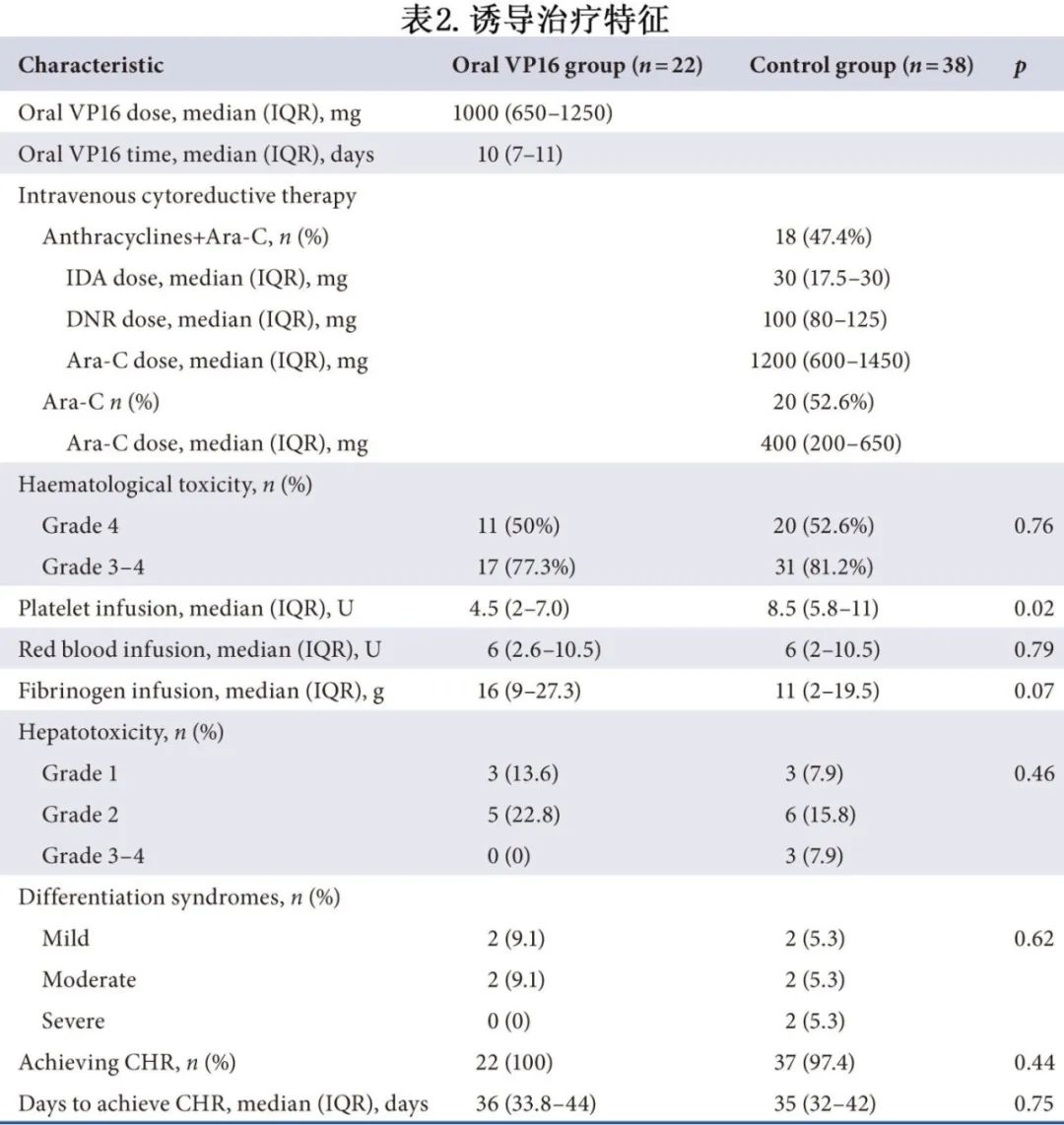
诱导治疗的基本特征见表2。口服VP16的中位时间为10天,中位剂量为1000mg。诱导治疗期间两组的4级血液学毒性、分化综合征无差异,无致死性感染。口服VP16组8例(36.4%)患者在诱导过程中出现1-2级肝毒性,无3-4级肝毒性。口服VP16组0例和对照组1例患者在诱导治疗中早期死亡。
血液学缓解和分子学缓解率
除1例患者在诱导治疗中早期死亡外,两组患者均在诱导治疗后达到完全血液学缓解(CHR)(100%);至CHR的中位时间为36天和35天(P=0.75)。
除1例患者在诱导治疗中早期死亡外,两组患者均进行巩固治疗并完成巩固治疗,巩固治疗后均达到完全分子学反应(CMR)。口服VP16组诊断后中位至CMR时间为3个月,对照组为3.3个月 (p=0.58)。
复发和生存
口服VP16组2例(9.1%)患者分别在随访5.3个月和6.2个月出现分子学复发;无血液学复发。1例患者接受ATRA+RIF作为的挽救治疗后(未进行干细胞移植)再次达到CMR并保持持续CR至今,另1例患者在达到第二次CMR仅1周后再次复发为中枢神经系统白血病,接受ATRA+RIF +鞘内化疗。2例患者均保持CR且存活。此外,巩固治疗期间无患者死亡。
对照组3例(7.9%)患者分别在随访5.2、14和18个月出现分子学复发。2例患者在接受ATRA和RIF挽救治疗后(未进行干细胞移植)再次获得CMR,持续CR并存活至今,1例患者随后出现血液学复发,最终因血液学复发死亡。
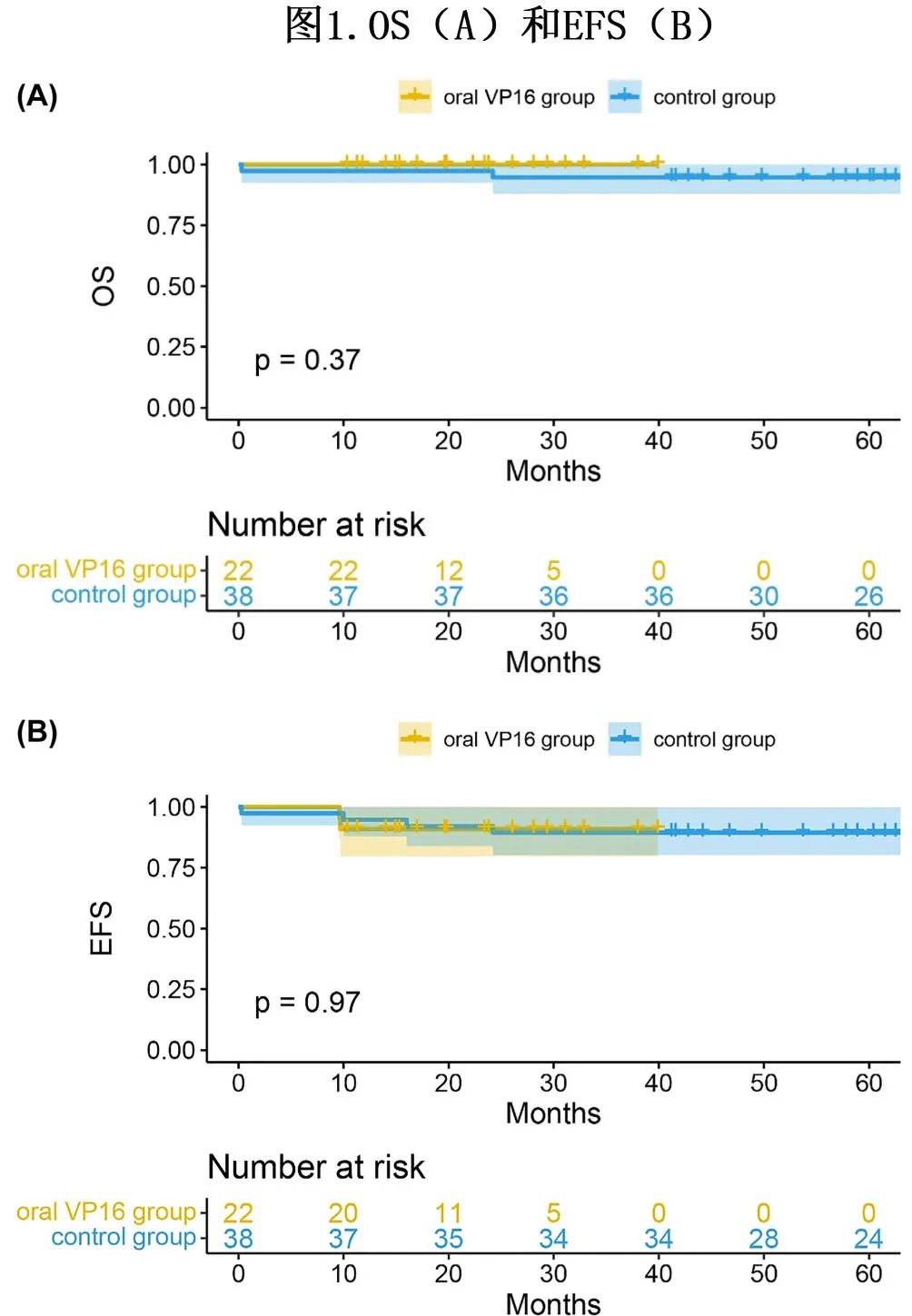
截至末次随访,除1例患者在诱导治疗期间早期死亡外,其余患者均存活。口服VP16组和对照组的2年OS和EFS分别为100% vs 94.7% (p=0.37)和90.9% vs 89.5% (p=0.97)(图1)。
总结
该回顾性研究分析了60例高危APL患者。诱导治疗中,除全反式维甲酸(ATRA)和口服砷(RIF)外,22例患者接受口服依托泊苷(VP16)作为细胞毒化疗(CC);38例患者接受静脉CC作为历史对照组。口服VP16的中位剂量为1000mg。对照组1例患者在诱导治疗期间死亡,59例可评估患者(100%)在IT后均达到完全血液学缓解(CHR),在巩固治疗后均达到完全分子学反应(CMR)。至CHR的中位时间为36天和35天(P=0.75),至CMR的中位时间为3个月和3.3个月(p=0.58)。两组患者分子复发分别为2例(9.1%)和3例(7.9%)。2年估计总生存率和无事件生存率分别为100% vs 94.7% (p=0.37)和90.9% vs 89.5% (p=0.97)。
口服VP16作为细胞减灭化疗联合ATRA和RIF的全口服诱导方案高效、安全、方便,可作为高危APL患者的备选方案。
参考文献
Tang F-F, Duan W-B, Liu X-H, Lu S-Y, Zhao X-S, Qin Y-Z, et al. A complete oral regimen for induction therapy of patients with high-risk APL: An oral etoposide instead of intravenous infusion for cytoreductive chemotherapy.Br J Haematol. 2024;00:1–7. https://doi.org/10.1111/ bjh.19464
作者:聊聊血液
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








真是方便的好办法
54
#依托泊苷# #急性早幼粒细胞白血病# #APL#
72