Nature Communications:PD-1/CD137双抗效果优异,安全性良好
2021-11-15 “ E药世界”公众号 “ E药世界”公众号
临床前研究显示,IBI319具有明显优于PD-1单抗的药效,且安全性良好,无肝毒性等副作用。
以PD-1/PD-L1为代表的免疫检查点疗法显着改变了部分癌症的治疗前景,但对许多癌症患者来说还不够。T 细胞共刺激受体已被作为下一代免疫疗法的靶点。CD137(又名4-1BB)是一种T细胞共刺激受体,它属于肿瘤坏死因子受体超家族(TNFRSF),广泛表达于各种细胞中。4-1BBL是CD137的天然配体,介导CD137的三聚化和随后特定TNF受体相关因子的募集以及下游信号级联反应的启动,这会导致细胞毒性T细胞的激活。
几种抗CD137的激动性抗体让人们看到了新的希望,但它们的肝毒性很强,无法应用于临床。事实上,抗CD137的激动性抗体如何诱导受体三聚化和下游信号传导的机制以及肝毒性的原因都没有得到充分解决。
近日,信达生物的研究团队在 Nature Communications 期刊上发表了题为:Cancer immune therapy with PD-1-dependent CD137 co-stimulation provides localized tumour killing without systemic toxicity 的研究论文。
该研究报告了一种CD137/PD-1双特异性抗体——IBI319 ,能够优先富集于PD-1高表达的肿瘤浸润性T细胞和NK细胞,临床前研究显示,IBI319具有明显优于PD-1单抗的药效,且安全性良好,无肝毒性等副作用。食蟹猴的毒理实验中,IBI319显示安全性良好,无肝毒性等副作用。将在人体临床试验中开展进一步评估研究。

IBI319被设计为完全人源化的IgG1分子,包含一个二价Fab片段,该片段分别与PD-1和CD137结合。抗PD-1区来自优化的信迪利单抗(αPD-1)——一种经批准的PD-1抑制剂。抗CD137区由优化的抗CD137抗体(αCD137 mAb)结合。这种设计使IBI319保持对PD-1的高亲和力和对CD137的低亲和力,以实现对PD-1的强阻断和对CD137的适当激动作用。
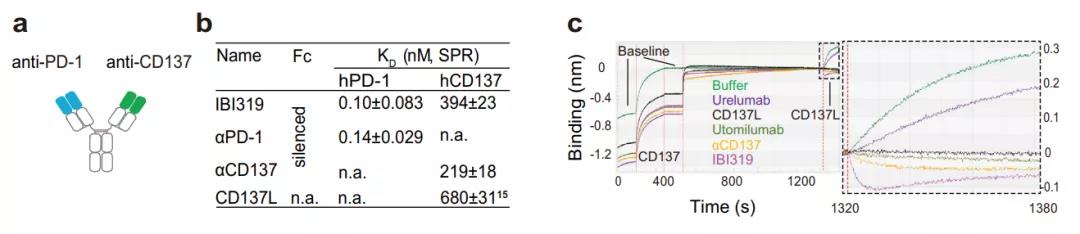
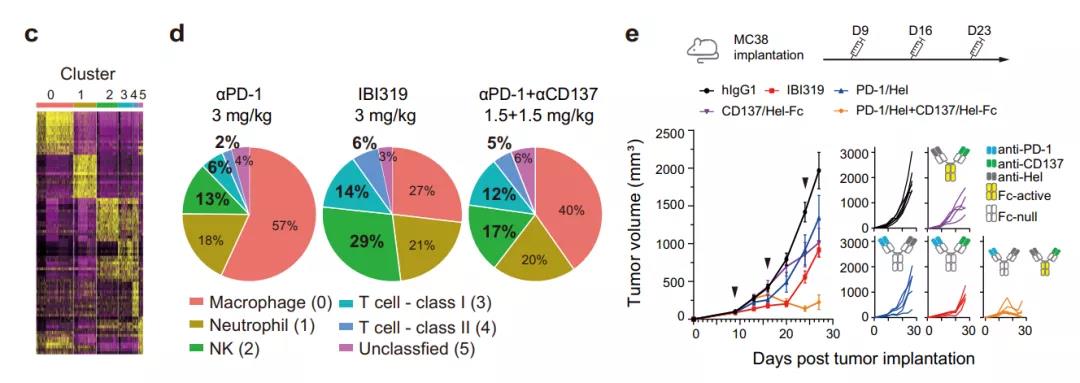
接下来,研究团队试图探索IBI319的体内功效和安全性。先前的研究表明通过结合检查点阻断和CD137刺激可以实现协同抗肿瘤效应。因此,除了确认IBI319保留这种协同作用外,他们还专注于解决靶向CD137诱导的潜在肝毒性。他们建立了两种过表达人PD-L1的结直肠癌细胞系小鼠模型。在第三次抗体注射后7天,与αPD-1 mAb和αCD137 mAb直接联用相比,IBI319显示出明显的剂量依赖性抗肿瘤功效,并抑制肿瘤生长,同时避免肝毒性。
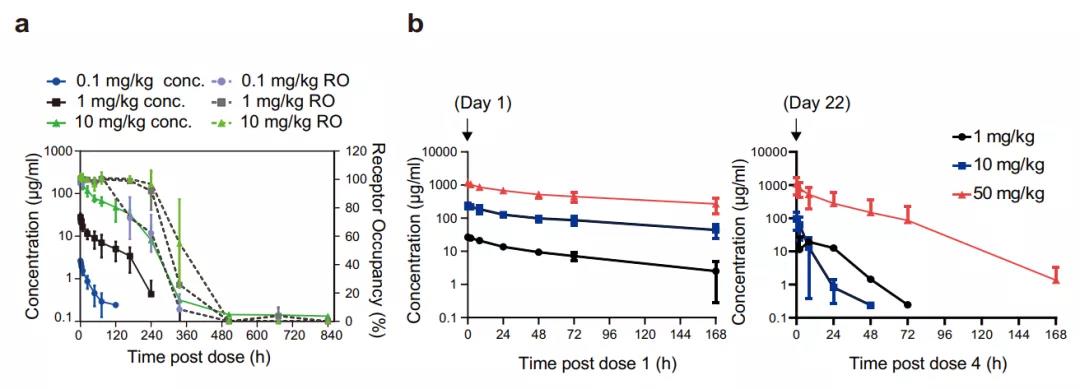
最后,研究团队通过食蟹猴确定了IBI319的药代动力学和安全性特征。IBI319药物浓度在给药后240-360小时下降,这种下降可能与抗药抗体的出现有关。在第360小时经常检测到抗药抗体的发生并持续到第864小时。
此外,在所有剂量组中,PD-1占有率在给药后5分钟达到饱和,并表现出结合耐久性和药物浓度之间的相关性。未观察到药物蓄积,未发现肝脏炎症和血液ALT/AST水平升高等毒副作用,表明IBI319在食蟹猴中具有可控的安全性。
综上,该研究评估了PD-1/CD137双特异性抗体IBI319,该双抗能够优先富集于PD-1高表达的肿瘤浸润性T细胞和NK细胞,临床前研究显示,IBI319具有明显优于PD-1单抗的药效,且安全性良好,无肝毒性等副作用。食蟹猴的毒理实验中,IBI319显示安全性良好,无肝毒性等副作用。
据悉,IBI319的1期临床试验已由广东省人民医院终身主任、广东省肺癌研究所名誉所长吴一龙教授牵头开展。
原始出处:
Qiao, Y., Qiu, Y., Ding, J. et al. Cancer immune therapy with PD-1-dependent CD137 co-stimulation provides localized tumour killing without systemic toxicity. Nat Commun 12, 6360 (2021). https://doi.org/10.1038/s41467-021-26645-6.
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#CD137#
50
#Nat#
46
#CD13#
48
#COMMUN#
45
#双抗#
54