Autophagy:湖南大学谭拥军团队发现转录因子FOXM1将染色质DNA定位到细胞外囊泡
2023-11-23 医药加学习班 医药加学习班
该研究发现转录因子FOXM1是将染色质基因或DNA片段定向到细胞外囊泡(EVs)的介质。
细胞外囊泡DNA(evDNAs)在各种疾病的诊断中具有重要价值,并促进遗传物质的跨细胞传递。
2023年11月16日,湖南大学谭拥军团队在Autophagy 在线发表题为“Transcription factor FOXM1 specifies chromatin DNA to extracellular vesicles”的研究论文,该研究发现转录因子FOXM1是将染色质基因或DNA片段(称为FOXM1-chDNAs)定向到细胞外囊泡(EVs)的介质。FOXM1与细胞核中的MAP1LC3/LC3结合,而FOXM1-chDNAs(如DUX4基因和端粒DNA)通过FOXM1结合并在溶酶体抑制期间通过分泌性自噬过程(SALI)被定向到细胞质,然后释放到EVs中。
破坏FOXM1表达或SALI过程会影响FOXM1-chDNAs纳入EVs中。FOXM1-chDNAs可以通过EVs传递到受体细胞,并在它们携带功能基因时在受体细胞中表达。这一发现提供了一个示例,说明转录因子FOXM1如何将染色质DNA片段指定到EVs中,揭示了其对形成来自细胞核的evDNAs的贡献。这为进一步探讨evDNAs在生物过程中的作用提供了基础,如水平基因转移。

细胞外囊泡(EVs)是各种细胞释放到细胞外微环境的膜囊泡,包含DNA、RNA和蛋白质,作为细胞间信使在细胞之间交换物质。由于细胞外囊泡DNA(evDNAs)在特定的生理或病理条件下携带来自其母细胞的基因物质的部分,广泛的研究已经集中在evDNAs对多种疾病的诊断价值上,而其生物学功能则没有像EV的RNA或蛋白质那样深入探讨。
evDNAs被认为在所谓的水平基因转移(HGT)中发挥作用,促进了功能基因和DNA片段在细胞之间的交换。越来越多的证据表明,EVs包含功能基因或染色体DNA片段作为evDNAs,并将它们转移到受体细胞。例如,作为evDNA的LINE-1逆转录子在人类癌细胞之间发生水平转移。另一个例子是由抗原呈递细胞(APCs)携带的EVs中的端粒DNA水平转移到主要是初级T细胞和中央记忆T细胞。因此,了解染色质DNA片段是如何选择到EVs的对于推动evDNAs在诊断中的应用以及澄清它们在水平基因转移等重要生物过程中的功能至关重要。
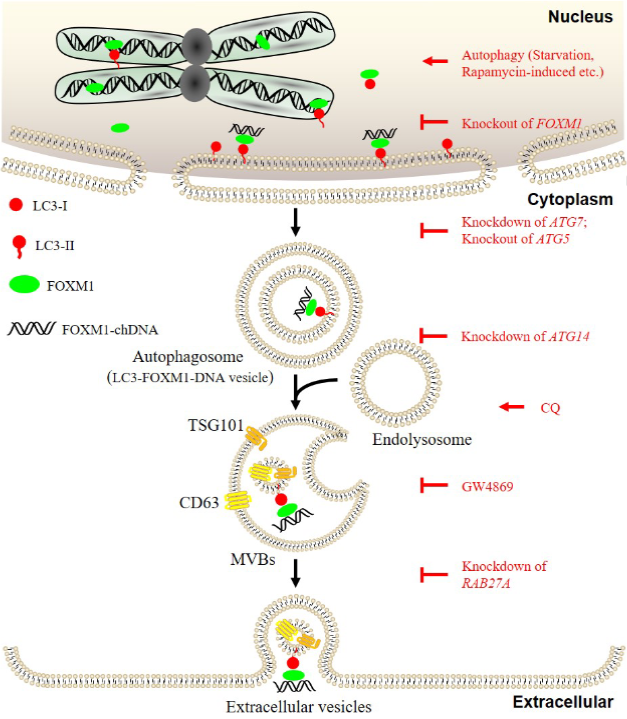
模式机理图(图片源自Autophagy )
最近,发现在自噬过程中LMNB1(Lamin B1)与细胞核中的LC3之间相互作用,染色质DNA可以转位到细胞质,为探索evDNAs起源提供了线索。LC3是Atg8家族蛋白的关键成员,负责自噬货物的选择。除了存在于细胞质中,LC3还存在于细胞核中,并与染色质结合的LMNB1(核小体蛋白)相互作用。在巨自噬/自噬过程中,正常LC3的一部分(LC3-I)需要与磷脂酰乙醇胺(PE)结合形成LC3–PE(LC3-II),这被称为LC3脂化,允许LC3蛋白嵌入膜中,然后将货物装载到自噬体中。
尽管自噬体经典上与溶酶体途径融合以进行降解,但累积的证据显示,自噬体可以通过释放细胞外囊泡和颗粒来分泌其成分。近来已经描述了两个主要的分泌性自噬途径:LC3依赖的EV装载和分泌(LDELS),该途径在晚期内体捕获货物,以及在溶酶体抑制期间进行的分泌性自噬(SALI),当降解受阻时,该途径分泌货物。在SALI过程中,ATG14(自噬相关14)促进自噬体和内体溶酶体融合形成含有LC3阳性内腔泡(ILVs)的多囊体体(MVBs)。ILVs可以通过MVBs与细胞膜的融合而作为EVs释放到细胞外环境。众所周知,LC3确定将蛋白质和RNA装载到EVs。然而,由于LMNB1对其DNA结合没有序列特异性,仅基于LMNB1-LC3介导的染色质DNA细胞质转位机制很难理解某些染色质DNA片段如何被选择并装载到EVs中。
该研究展示了一个涉及转录因子-LC3的机制,该机制在自噬过程中将某些染色质基因或DNA片段指定给EVs。FOXM1是forkhead box转录因子家族的成员,参与通过刺激细胞核中的基因转录来调控细胞proliferation、DNA损伤修复、细胞干性和新陈代谢。FOXM1可以通过直接与其DNA结合一致性序列或间接通过与其他转录因子如MYBL2/B-Myb、MuvB和NFY等相互作用来直接定向其染色质结合区域。
该研究证实FOXM1在细胞核中与LC3相互作用,并在自噬过程中介导特定的染色质DNA片段(称为FOXM1-chDNAs)到EVs的过程。FOXM1与LC3的相互作用由FOXM1的LC3相互作用区(LIR)基序(FOXM1 317-320aa)介导,并且在LC3脂化的促进下进行,而FOXM1与LC3的相互作用并不破坏FOXM1的DNA结合能力。通过分析FOXM1特异ChIP-seq、LC3特异ChIP-seq和evDNA-seq的测序数据,确认了FOXM1-chDNAs,包括DUX4基因和端粒DNA。
通过DNA-FISH实验证实了FOXM1-chDNAs到EVs的转位,通过使用TetO-TetR-GFP方法追踪选择的染色质位点的移动,以及对来自MVBs和EVs的DNA样本进行PCR分析。作者确认FOXM1表达和SALI过程对于FOXM1-chDNAs到EVs是至关重要的。本研究首次展示了由转录因子指定的EVs中的染色质DNA片段的情况,为进一步研究evDNAs在水平基因转移等重要生物过程中的功能提供了基础。
原文链接:
https://doi.org/10.1080/15548627.2023.2284523
作者:医药加学习班
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#FOXM1# #水平基因转移# #细胞外囊泡DNA#
87