新冠大流行转折点?辉瑞,BioNTech正式向美国FDA提交申请以批准新冠疫苗
2020-11-21 JACKZHAO MedSci原创
或将成为遏制全球大流行的转折点,这是美国首例寻求监管当局批准的新冠疫苗
 SPENCER PLATT/GETTY IMAGES
SPENCER PLATT/GETTY IMAGES
辉瑞公司及其德国合作伙伴BioNTech上周五向美国食品药品管理局(FDA)正式提交申请了其针对SARS-CoV-2的BNT162b2疫苗的紧急使用授权(EUA),预计到2020年12月中旬至年底,将有可能在美国高危人群中使用该疫苗,或将成为遏制全球大流行的转折点。
这是美国首例寻求监管当局批准的新冠病毒疫苗。辉瑞公司首席执行官阿尔伯特•布尔拉(Albert Bourla)在周五的视频中说道:我感到非常自豪和喜悦,甚至有些放心,我们现在已经可以将我们对新冠疫苗的紧急使用授权的请求交给了FDA。这是一个历史性的日子,对于科学和我们所有人来说都是一个历史性的日子。从我们宣布与BioNTech合作的计划到FDA提交之日,仅用了248天的时间。
BioNTech首席执行官兼联合创始人医学博士Ugur Sahin表示,在美国,为紧急用途提交申请是向全球人群尽快提供我们的候选疫苗的关键一步。“我们打算继续与世界各地的监管机构合作,以实现我们疫苗在全球的快速分销。两家公司已经开始与包括EMA和英国药品和保健产品监管局(MHRA)在内的全球多个监管机构进行滚动提交,并打算在未来几天内向全球其他监管机构提交申请。在某些情况下,政府可能具有类似于EUA的监管途径。两家公司将准备在授权后数小时内分发候选疫苗。

美国FDA官方推特
数小时后,FDA宣布由外部专家组成的小组,即疫苗和相关生物产品咨询委员会或VRBPAC,将于12月10日开会审查数据,并就是否批准紧急使用请求以及在何种条件下(如果有的话)向该机构提供建议,以使用疫苗。例如,它尚未授权在12岁以下的儿童中使用,因为它尚未在未成年人中进行过试验。
人们普遍期望FDA随后将发布两剂疫苗的紧急使用授权,这种疫苗已被证明在预防新冠感染方面非常有效。官员们表示,他们希望在授权后的几天内,开始在某些地方为卫生工作者进行疫苗接种,他们将在有限的首批疫苗用于一线工作人员。
在10月下旬举行的VRBPAC的较早会议上,FDA官员似乎暗示他们正在重新考虑使用EUA允许早期使用新冠疫苗的想法,这表明这样做可能会破坏其他正在进行的临床试验并限制其产生足够数据。作为替代,官员表示他们正在考虑使用扩展访问协议以允许使用疫苗。
但据美国科技新闻STAT报道,这并未启动,不过援引FDA疫苗研究与审查办公室主任马里恩·格鲁伯(Marion Gruber)在本周的一次公开论坛上表示,扩大访问范围已成为现实。她在论坛上指的是辉瑞-BioNTech产品,她说:“疫苗制造商可能会……提出紧急使用授权请求。” “而且如果有数据支持,FDA可能会为此疫苗签发EUA。”
辉瑞疫苗的3期试验招募了43661名志愿者,其中170人出现了有症状的新冠病毒感染。这其中有162人是来自安慰剂组,只有8人接受了疫苗。该试验中有10例严重感染病例,其中9例属于安慰剂组,这表明该疫苗可预防严重疾病和轻度疾病。总体而言,该疫苗在预防有症状的新滚病毒感染方面显示出95%的有效率。迄今为止,该研究的数据监控委员会(DMC)尚未报告与疫苗有关的任何严重的安全隐患。
美国政府已同意购买1亿剂疫苗,并可以选择另外购买5亿剂。据辉瑞公司预测,它将在12月提供2500万剂疫苗,足以为1250万人接种疫苗。
另一新冠疫苗竞赛领先者Moderna,在本周一宣布,对其疫苗的初步分析表明,它在预防症状性感染方面的有效率为94.5%。在分析的95例病例中,有90例接受了安慰剂注射。到目前为止,在试验中发现的11例严重病例(仍在进行中)均在安慰剂组中。美国政府预计将在12月从Moderna那里再接收1500万剂疫苗,这足以为另外750万人接种疫苗。
预计未来几天Moderna也将向FDA提出正式申请要求以紧急授权使用其疫苗。
两种疫苗均采用一种mRNA新技术开发的mRNA疫苗。mRNA疫苗是近年来新兴的一种疫苗形式,mRNA疫苗是将外源目的基因序列通过转录、合成等工艺制备的mRNA通过特定的递送系统导入机体细胞并表达目的蛋白、刺激机体产生特异性免疫学反应,从而使机体获得免疫保护的一种核酸制剂,从而使机体获得免疫保护。mRNA疫苗研发存在较高的技术门槛,目前仅有美国和德国研发的少数几个mRNA疫苗品种进入临床研究阶段,并取得重要进展。
中国国内首个获批开展临床试验的新冠mRNA疫苗是由中国人民解放军军事科学院军事医学研究院与地方企业共同研究、开发形成的新型冠状病毒mRNA候选疫苗(ARCoV)已于6月19日正式通过国家药品监督管理局临床试验批准。据悉,该新冠mRNA疫苗已经按照临床试验要求完成了多批次生产,将在树兰(杭州)医院正式启动I期临床试验。

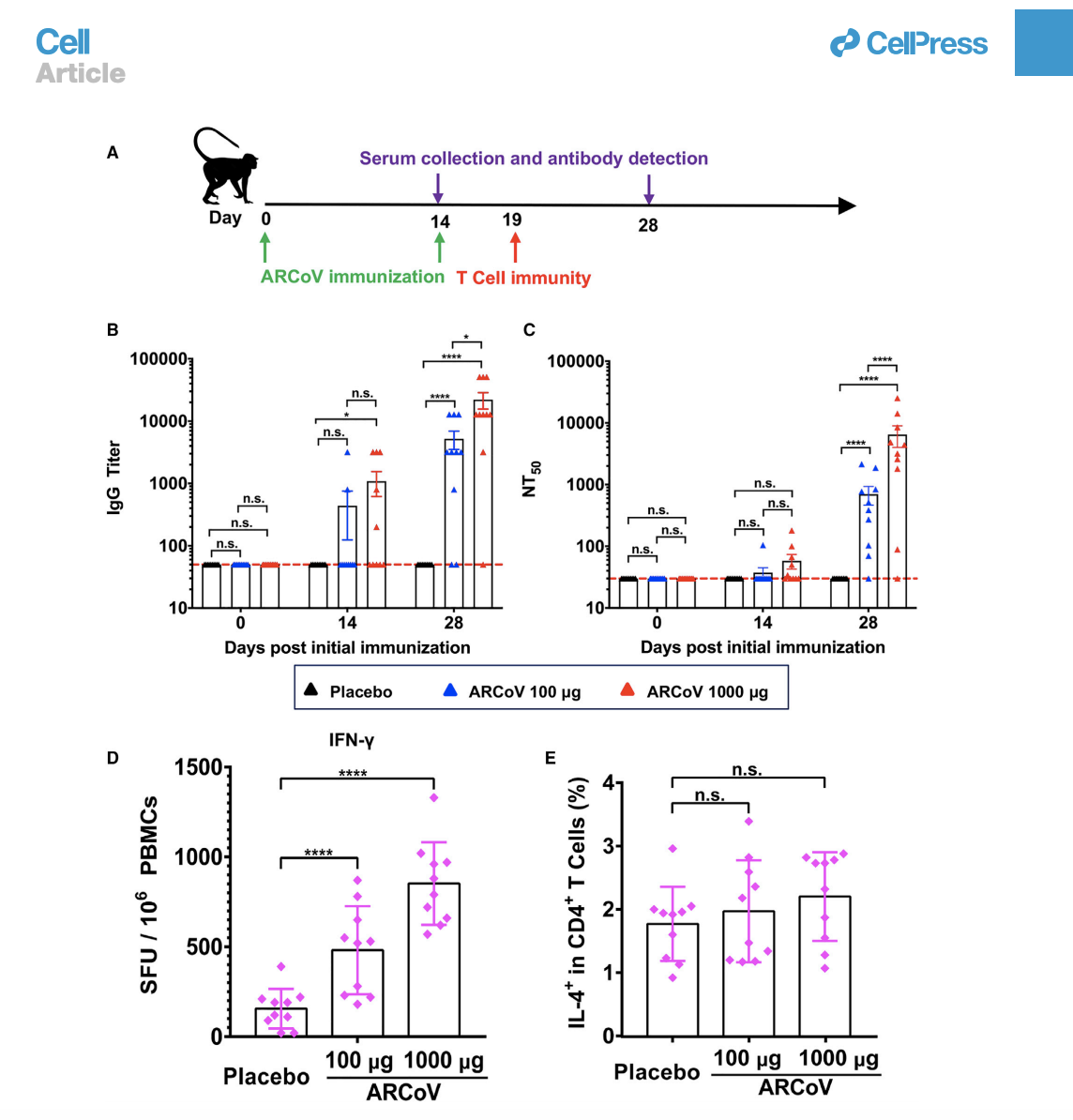
Zhang, Na-Na et al. “A Thermostable mRNA Vaccine against COVID-19.” Cell vol. 182,5 (2020): 1271-1283.e16. doi:10.1016/j.cell.2020.07.024
该疫苗项目负责人、军事科学院军事医学研究院研究员秦成峰团队于7月23日在《Cell》发表研究称,一种基于信使核糖核酸(mRNA)的实验性疫苗可在小鼠和非人灵长类动物中引起保护性免疫反应。两次注射疫苗足以诱导小鼠产生强大的免疫力,完全防止小鼠感染SARS-CoV-2。
研究人员目前正在评估ARCoV的长期稳定性。此外,ARCoV诱导的中和抗体的持续时间尚待确定,因为其他人类冠状病毒的经验表明,由于抗体反应减弱,可能再次感染,需要进一步的研究来评估动物模型的长期免疫反应以及ARCoV在人类中的有效性。
尽管mRNA疫苗在巨细胞病毒(CMV)、流感病毒、埃博拉病毒和寨卡病毒等多种传染病临床研究中取得了一定的研究进展,但尚存在待确证的诸多问题,如,mRNA本身具有的潜在免疫原性;递送系统(如,脂质纳米颗粒)的稳定性、纳米剂型安全性及所使用阳离子聚合物/脂质体安全性、递送靶向性及递送效力等诸多问题,影响疫苗的有效性、安全性和质量可控性。
美国国家过敏和传染病研究所所长安东尼·福西(Anthony Fauci)也承认,迄今为止进行的研究并未表明对疫苗的保护将持续多长时间,但是高效率令人惊讶。他甚至并没有期望其疗效能超过90%。
作者:JACKZHAO
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#Bio#
62
#FDA提交申请#
68
#TEC#
58
好
121
期待转折点的早日到来#新冠肺炎#
119