“绘”解读真报告丨从CSCO指南出发,带您更多地了解卵巢癌HRD检测!
2024-01-20 苏州绘真医学 苏州绘真医学
CSCO指南对HRD指标的升级和细化,也论证了卵巢癌HRD检测受到临床的进一步重视!
我们关注到2023年CSCO卵巢癌诊疗指南的更新,将“同源重组修复缺陷(HRD)”的检测从III级推荐提升至II级推荐;在一线维持治疗方案的推荐上,对于一线化疗中联合贝伐珠单抗且化疗后评价为CR/PR(完全/部分缓解)的患者,将先前“无BRCA突变”类型又细分为“HRD”和“HRP(同源重组修复正常)”,并做相应维持治疗的推荐:HRD阳性患者推荐尼拉帕利维持治疗或奥拉帕利+贝伐珠单抗维持治疗,阴性患者推荐尼拉帕利或贝伐珠单抗维持治疗。CSCO指南对HRD指标的升级和细化,也论证了卵巢癌HRD检测受到临床的进一步重视!
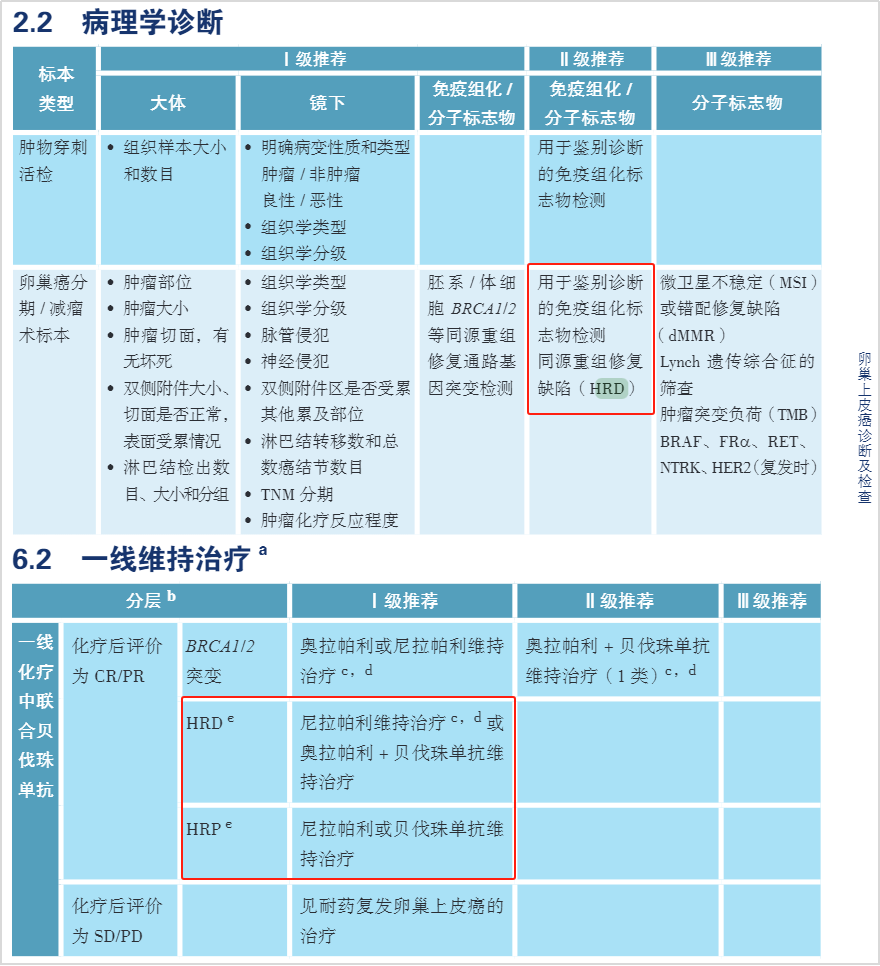
图1 摘自2023年新版卵巢癌CSCO指南
众所周知,HRD在卵巢癌、乳腺癌、胰腺导管癌、前列腺癌等肿瘤中尤其突出,并逐渐发展成一种新型标志物指导实体肿瘤的诊治!这里我们就从上述CSCO指南出发,结合我司既往HRD阳性检测报告(图2),解读HRD检测中的那些关键问题。
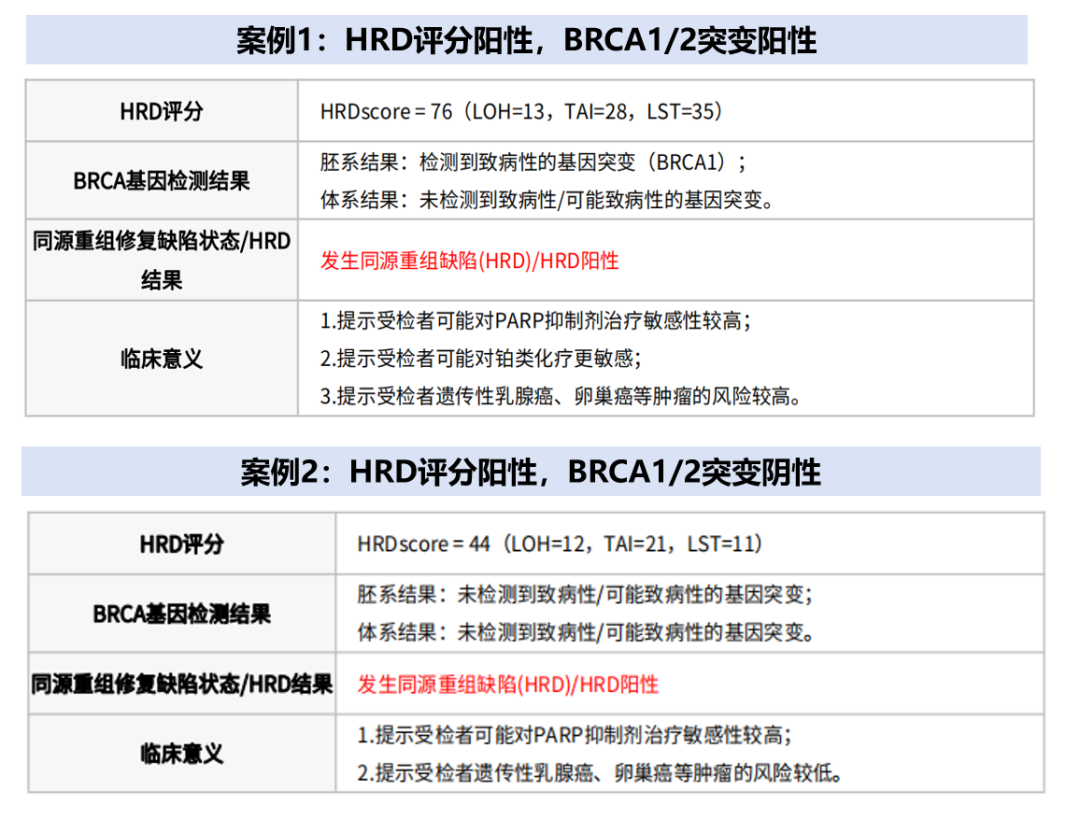
图2 报告案例展示
知其然,知其所以然,HRD检测是什么?
HRD检测要从细胞基因组上的DNA损伤说起:细胞中双链DNA由两条DNA单链组成,如若发生损伤断裂,可分为DNA单链断裂(SSB)和双链断裂(DSB),导致DNA的功能受损。当DNA损伤出现后,机体必然有补救的修复机制。于是,出现SSB的细胞会启动依赖于PARP酶的内在机制完成DNA单链修复;而出现更严重的DSB时,包含BRCA1/2在内的“同源重组修复”(HRR)通路基因就会发挥修复功能[1]。
如若DSB的修复过程出问题,即HRR基因发生变异等因素,细胞便失去了同源重组修复DNA损伤的能力,称为“同源重组缺陷”(HRD)。那么,对于肿瘤细胞存在HRD的患者来说,再使用PARP抑制剂阻碍SSB修复,使肿瘤细胞DNA单链损伤修复失败,发展成DNA双链损伤且得不到修复,就促进肿瘤细胞的凋亡,达到抗肿瘤的作用,即“合成致死”(图3)。
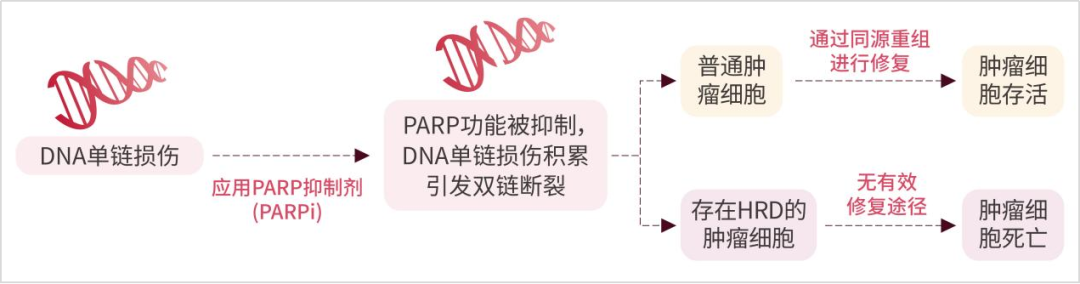
图3 HRD的合成致死原理图
HRD检测是什么?表现为HRD的肿瘤DNA由于基因修复缺陷,损伤积累后会在基因组上留下特定的、可量化的基因组改变,称为“基因组瘢痕”,形式体现为杂合性缺失(LOH)、端粒等位基因不平衡(TAI)、大片段迁移(LST),综合三者计算基因组不稳定评分(genomic instability score,GIS)就能更全面地反映基因组瘢痕状态,也就是所谓的HRD评分(图4)。研究表明,瘢痕状态越严重,HRD评分高的患者,可能更容易从PARP抑制剂中获益。
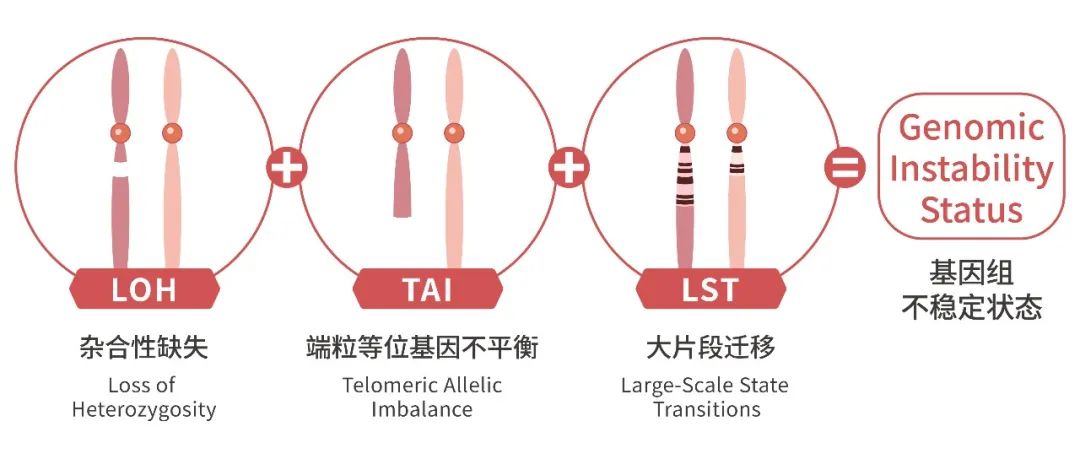
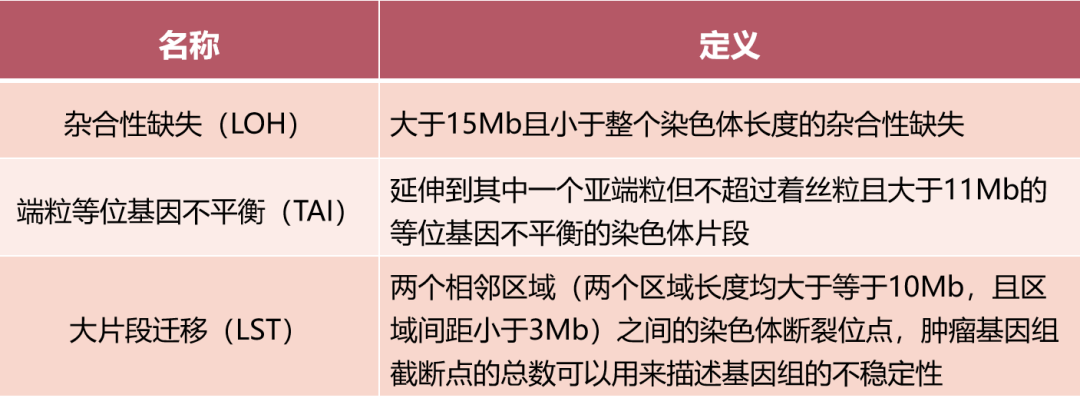
图4 HRD GIS评分方式
BRCA1/2突变的患者,HRD评分一定为阳性吗?
《同源重组修复缺陷临床检测与应用专家共识》中提到[2],HRD状态评估分为两方面:①HRD评分阳性:GIS评分≥42分,②BRCA1/2基因的致病性变异状态。二者至少有一个阳性,即为HRD阳性,只有当GIS评分<42(评分阴性)且BRCA1/2未发生致病性变异时,HRD状态为阴性。因此,在拿到HRD和BRCA1/2的检测结果后,不要单一地认为HRD评分阴性或者BRCA1/2未突变就是HRD阴性,需要同时把握两个指标,综合评估HRD状态。
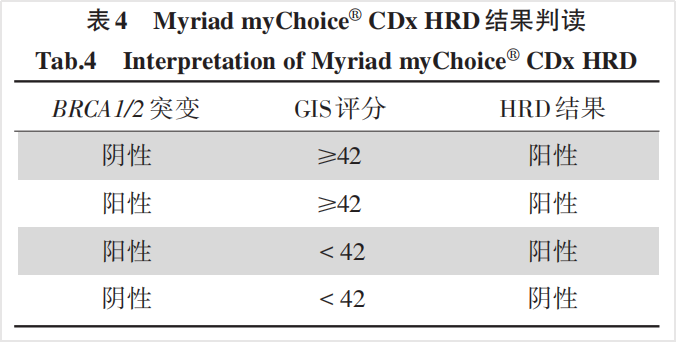
图5 共识推荐的HRD结果判读标准
从BRCA1/2和HRD的关系上来说,BRCA1/2突变是HRD形成的原因之一。那么,携带BRCA1/2突变的患者就一定会表现为HRD评分阳性吗?其实不然。我们从Mychoice CDX®关于HRD检测的技术信息中找到答案。在测试的总共209个FFPE肿瘤样品中,有5例样本检出为tBRCA1/2状态阳性而GIS评分为阴性的案例。

图6 Mychoice CDX®关于HRD检测的技术信息
调研相关文献,2016年发表在Clin Cancer Res.上的研究中也有体现[3]。该研究训练集纳入了561例卵巢癌和497例乳腺癌样本,分别检测HRD评分(LOH,TAI和LST)和BRCA1/2缺陷(含突变和甲基化)状态。结果如图7所示,分析看出,从BRCA基因缺陷出发,多数比例的缺陷及少数比例的正常的情况,都会匹配在HRD评分阳性(≥42)的患者中。然而,在HRD评分<40的患者中,也出现了少部分BRCA1/2缺陷的患者,且即便HRD评分≤15,也有BRCA1/2缺陷的案例。
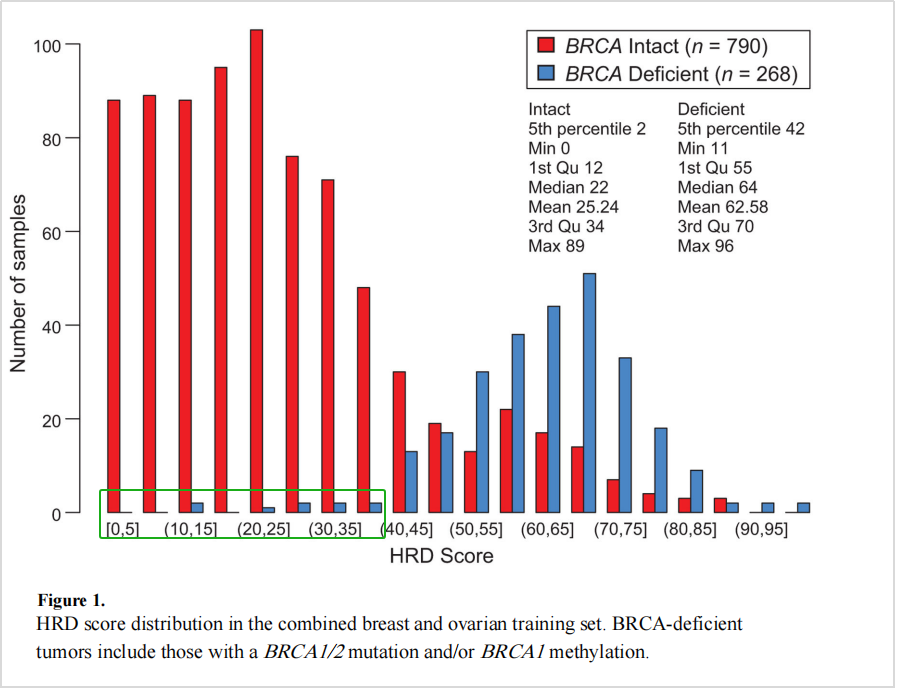
图7 在乳腺癌和卵巢癌中的HRD状态评估
西安交通大学附属第二医院今年发表的一篇研究[4],纳入147名乳腺癌患者,HRD通过基因组瘢痕评分(GSS)评估。若GSS≥50或BRCA1/2变异,则评估为HRD阳性。结果在乳腺癌中评估HRD阳性率为34.7%,并且在HRD阳性队列中,报道一位携带BRCA1/2突变且GSS<50的患者,占比仅占0.7%,比较罕见!
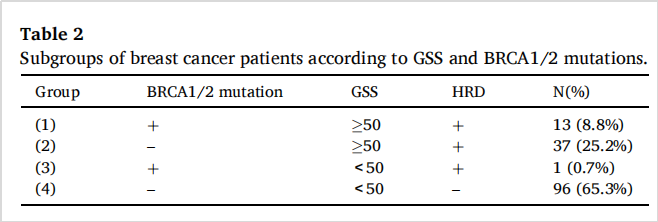
图8 根据GSS和BRCA1/2突变评估HRD状态
这可以说明表明,无论在卵巢癌还是在乳腺癌中,BRCA1/2缺陷的患者并非绝对导致HRD评分阳性。而且,从图5中共识标准的角度来说,HRD阳性判读条件也存在BRCA1/2突变阳性,GIS评分阴性这一栏,也是HRD阳性条件的评估标准之一!所以,HRD评分和BRCA1/2变异存在因果关系的同时又相互独立,均能各自评估HRD阳性,只是BRCA阳性,HRD阴性的患者实属罕见!
同为HRD阳性的患者,PARP抑制剂疗效是否有差异?
回到主题,关注我们报告中综合评估为HRD阳性的两位患者:案例1为HRD评分阳性,携带BRCA1致病性胚系变异;案例2为HRD评分阳性,BRCA1/2未发生致病性突变。那么针对这两种类型以及HRD阴性的患者,使用PARPi治疗疗效是否有差异呢?我们开展广泛调研。
2022年,MSKCC(纪念斯隆凯特琳癌症中心)发布II期LIGHT研究最新结果[5],研究入组272名既往接受过一线及以上含铂化疗的铂敏感复发性卵巢癌患者,接受奥拉帕利治疗。将患者分四组评估疗效:胚系(g)BRCAm、体系(s)BRCAm、HRD+(BRCA-)以及HRD-。结果表明,在客观缓解率(ORR)上,gBRCAm、sBRCAm、HRD+(BRCA-)、HRD-四个队列的ORR为69%、64%、30%、10%。在18个月总生存(OS)率上,四个队列OS率分别为:86%、88%、79%和60%;并且患者的疗效并不受患者既往治疗线数的影响。表明在奥拉帕利单药疗效上,BRCA突变/HRD阳性患者比BRCA阴性/HRD阳性患者疗效更好,两者均比HRD阴性患者疗效好!
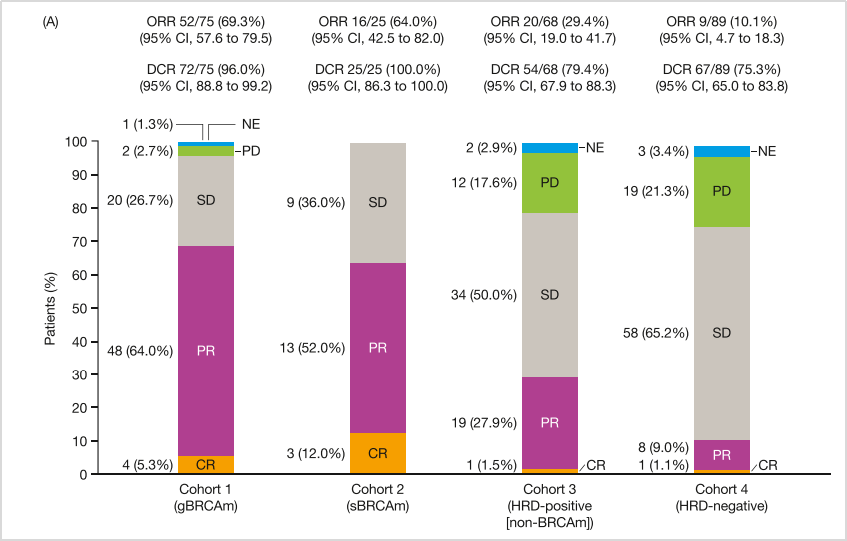
图9 LIGHT临床研究数据
另外,在奥拉帕利+贝伐珠单抗的二线治疗上,多中心、随机、双盲、III期PAOLA-1/ENGOT-ov25研究在Annals of Oncology上更新了长期随访数据[6]。该研究纳入806例二线治疗的卵巢癌患者,给予奥拉帕利+贝伐珠单抗或安慰剂+贝伐珠单抗维持治疗。结果在整体HRD阳性的人群中,奥拉帕利+贝伐珠单抗组的中位OS延长了近18个月(75.2 vs 57.3);5年OS率提升17%,死亡风险降低38%(HR=0.62)。
进一步细分BRCA突变和HRD评分状态的亚组显示,无论在无进展生存期(PFS)还是风险的降低(HR)上,与LIGHT研究结论高度一致,BRCA突变患者疗效最好,风险比59%,HRD阳性BRCA阴性患者疗效次之,风险比降低55%,HRD阴性患者疗效最差。
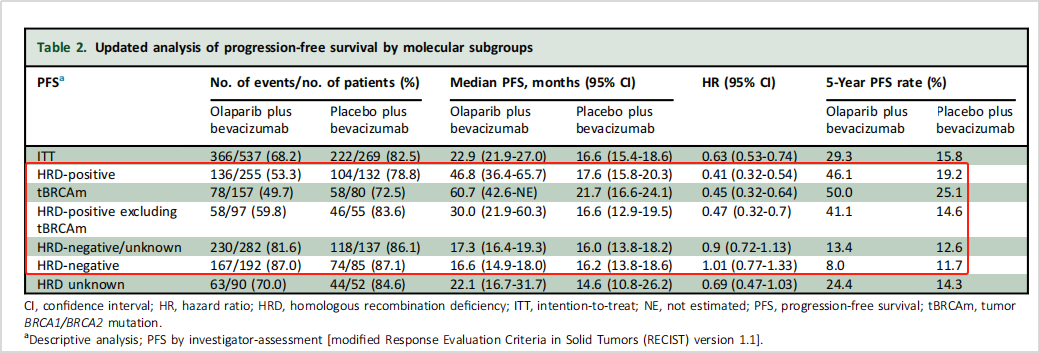
图10 PAOLA-1/ENGOT-ov25研究结果
总的来说,通过HRD评分和BRCA1/2基因突变的同步检测,可能对PARP抑制剂疗效提供更好的依据。本次报道的两位HRD阳性的卵巢癌患者,从检测结果层面来看,案例1患者用PARPi疗效可能会优于案例2患者,当然,这不能成为治疗疗效评估的唯一因素。
事实上,于卵巢癌患者而言,HRD和BRCA1/2的检测为首要推荐,且指导意义不止体现在PARPi的治疗上。根据国家医保局最近公布的2023年医保药品目录来看,多种PARPi用于HRD阳性/BRCA突变的卵巢癌适应症成功纳入医保目录。这也说明基因检测也会为实现医保报销、减轻经济负担提供依据,无疑为患者治疗锦上添花!
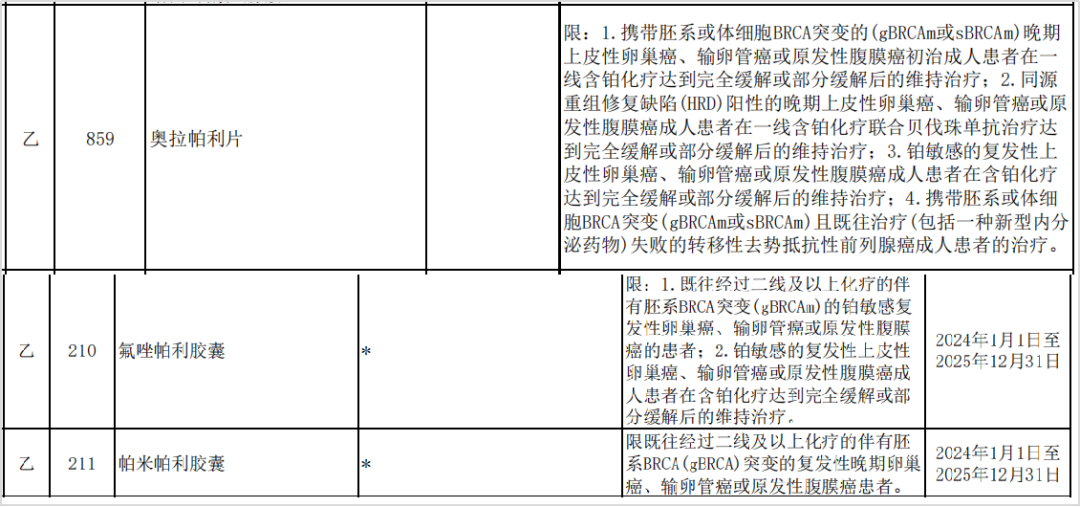
图11 摘自《国家基本医疗保险、工伤保险和生育保险药品目录(2023 年)》
为啥要选择绘真医学的HRD检测项目?
专家共识指出[7],除BRCA1/2基因突变外,其他HRR基因,如RAD51、ATM、PALB2、MRE11等损伤或缺失也会导致HRD,HRD检测可以使PARP抑制剂敏感人群从约占25%的BRCA突变人群扩大到超过50%的HRD阳性人群。基于SNPs的“基因组瘢痕”分析是当前最具应用前景的HRD临床检测方法,通过NGS检测SNPs是目前HRD评分检测的主流方案。
我司提供的同源重组修复缺陷(HRD)评分检测正是参考专家共识,采用SNPs检测,覆盖了约5万个SNP位点,能够一次性检测HRD评分(LOH+TAI+LST),并依据指南综合评估HRD状态。在检测性能上,其一,我司使用商业化的HRD标准品验证,在标准品梯度试验中(近30组数据),对于肿瘤细胞含量≥20%的样本,我司HRD检测项目检测准确性为100%。其二,某合作医疗机构同时送检我司及友商HRD检测项目27例,进行「头对头」比较性分析。结果显示,存在2例标本的HRD评分结论不一致。后来经WGS检测验证,两例标本完全符合我司检测结果。基于我司HRD产品的优异表现,获得了机构认可。其三,我司SNPs方法学产品通过与WGS方法学进行比较,结果显示,两者HRD阳性检出一致性高于95%,SNPs的整体阳性率在64%。又回顾我司近期近百例HRD临床样本检测结果,统计阳性率也为64%,数据吻合。这从不同角度,表明我司HRD检测的准确可靠性。
除了HRD评分之外,BRCA1/2基因检测也应追求更全面地检测,尤其关注到罕见的BRCA1/2基因大片段重排(LGR)。指南指出[8],BRCA1/2大片段重排检测除了MLPA外,部分经过特殊设计并严格验证的NGS方法也可用于LGR的检测。我司单项BRCA1/2检测能够覆盖BRCA1/2全部变异类型的检测,并经过真实报告验证。
目前,HRD和HRR基因作为PARP抑制剂重要的疗效预测标志物,已经呈现出面向整个实体瘤领域的治疗指导,相关检测也受到临床重视。我司在HRD评分和BRCA1/2基因检测的基础上,面向卵巢癌、乳腺癌、前列腺癌和胰腺癌患者,又推出HRD+HRR 61基因检测项目,形成了HRD系列产品线:HRD评分、HRDpro(包括HRD评分和BRCA1/2基因胚系和体系突变检测)、HRD+HRR 61基因(包括HRD评分+61个基因突变)。
介绍下HRD+HRR 61基因项目,它是包含了HRD评分和61个HRR等基因的全部编码区,即覆盖43个PARP抑制剂相关HRR基因变异,以及其他18个指南推荐基因变异。该项目分别从HRD评分,HRR基因突变和其他实体瘤的靶向指导的角度,全面地评估患者从PARP抑制剂或铂类药物治疗获益的可能性,同时预测其他靶药、化疗药疗效,辅助遗传风险评估和预后评估。
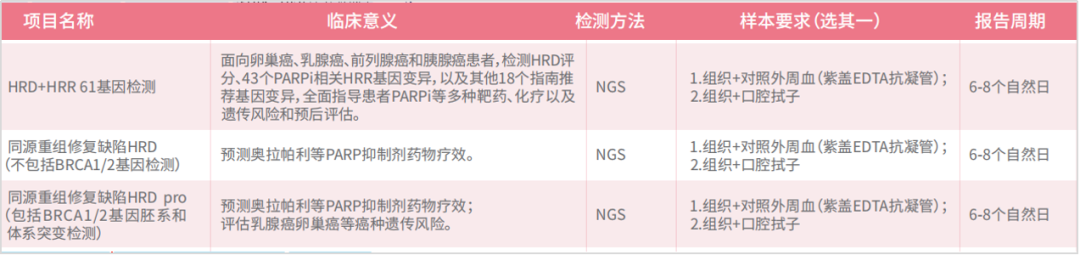
图12 绘真医学HRD相关检测产品线
参考文献:
[1]Murai J, Pommier Y. BRCAness, Homologous Recombination Deficiencies, and Synthetic Lethality. Cancer Res. 2023 Apr 14;83(8):1173-1174. doi: 10.1158/0008-5472.CAN-23-0628. PMID: 37057596.
[2]中国抗癌协会肿瘤标志专业委员会遗传性肿瘤标志物协作组,中华医学会病理学分会分子病理学组,辇伟奇,等.同源重组修复缺陷临床检测与应用专家共识(2021版)[J].中国癌症防治杂志 2021年13卷4期, 329-338页, 2021.DOI:10.3969/j.issn.1674-5671.2021.04.01.
[3]Telli M L , Timms K M , Reid J E ,et al.Homologous Recombination Deficiency (HRD) Score Predicts Response to Platinum-Containing Neoadjuvant Chemotherapy in Patients with Triple-Negative Breast Cancer[J].Clinical Cancer Research An Official Journal of the American Association for Cancer Research, 2016, 22(15):3764.DOI:10.1158/1078-0432.CCR-15-2477.
[4]Feng C, Zhang Y, Wu F, Li J, Liu M, Lv W, Li C, Wang W, Tan Q, Xue X, Ma X, Zhang S. Relationship between homologous recombination deficiency and clinical features of breast cancer based on genomic scar score. Breast. 2023 Jun;69:392-400. doi: 10.1016/j.breast.2023.04.002. Epub 2023 Apr 21. PMID: 37116400; PMCID: PMC10165146.
[5]Cadoo K, Simpkins F, Mathews C, Liu YL, Provencher D, McCormick C, ElNaggar AC, Altman AD, Gilbert L, Black D, Kabil N, Bennett J, Munley J, Aghajanian C. Olaparib treatment for platinum-sensitive relapsed ovarian cancer by BRCA mutation and homologous recombination deficiency status: Phase II LIGHT study primary analysis. Gynecol Oncol. 2022 Sep;166(3):425-431. doi: 10.1016/j.ygyno.2022.06.017. Epub 2022 Jul 5. PMID: 35803835; PMCID: PMC9909678.
[6]Ray-Coquard, et al. Olaparib plus bevacizumab first-line maintenance in ovarian cancer: final overall survival results from the PAOLA-1/ENGOT-ov25 trial. Annals of Oncology May 19, 2023. DOI: https://doi.org/10.1016/j.annonc.2023.05.005.
[7]中华医学会妇科肿瘤学分会孔北华刘继红谢幸马丁黄鹤王新宇鹿欣李宁姜洁张瑜高庆蕾张国楠梁志清向阳崔恒.卵巢癌PARP抑制剂临床应用指南(2022版)[J].现代妇产科进展, 2022, 31(8):561-572.
[8]中华医学会病理学分会, 国家病理质控中心. BRCA1/2数据解读中国专家共识(2021版) [J] . 中华病理学杂志, 2021, 50(6) : 565-571. DOI: 10.3760/cma.j.cn112151-20201027-00809.

作者:苏州绘真医学
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#卵巢癌# #HRD检测#
30