Lancet Oncol:Pembrolizumab获批一线联合化疗治疗晚期NSCLC(KEYNOTE-021)
2017-05-20 佚名 肿瘤前沿
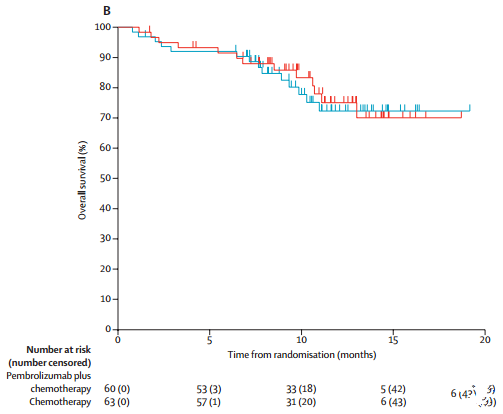
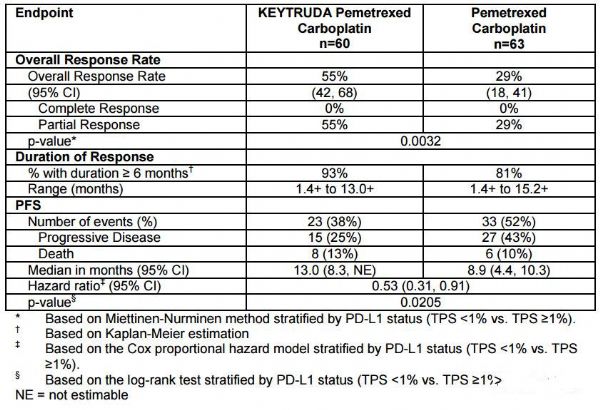
2017年5月10日,美国FDA加速批准了Pembrolizumab(Keytruda)联合培美曲塞+卡铂用于既往未经治疗的无突变的晚期NSCLC患者(非鳞癌)的治疗。这项适应症的获批使得Keytruda的说明书再次更新(之前的一次是2017年02月份的更新),而且把免疫单抗对于肺癌的治疗带入了一个新阶段,即联合化疗的全新治疗模式。该适应症的批准是基于一项名为KEYNOTE-021的多中心、开放、
作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#Lancet#
36
#Oncol#
46
#KEYNOTE#
42
#mAb#
29
#Pembro#
48