FDA批准赛诺菲和再生元的PD-1单抗Libtayo用于治疗晚期皮肤鳞状细胞癌
2018-09-29 MedSci MedSci原创
9月29日,FDA批准赛诺菲和再生元联合开发的PD-1单抗Libtayo(cemiplimab-rwlc)用于治疗不适合进行手术或放射治疗的转移性或局部晚期的皮肤鳞状细胞癌(CSCC) 患者。Libtayo是美国第一个批准用于晚期CSCC的治疗药物。
9月29日,FDA批准赛诺菲和再生元联合开发的PD-1单抗Libtayo(cemiplimab-rwlc)用于治疗不适合进行手术或放射治疗的转移性或局部晚期的皮肤鳞状细胞癌(CSCC) 患者。Libtayo是美国第一个批准用于晚期CSCC的治疗药物。
CSCC在美国占所有皮肤癌的1/5,每年有约70万名新病例,新诊断的患者数量还在不断增加。CSCC通常在暴露在阳光或紫外线照射下的皮肤中发生。虽然大多数CSCC患者可以通过手术切除来治愈,但是少数患者的癌症会进入晚期,它们不再对局部疗法产生应答。晚期CSCC会导致出血和感染的并发症,而且它们可以转移到局部淋巴结或身体的其它组织和器官中,可能危及生命。
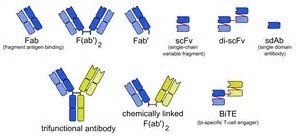
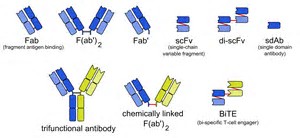
Libtayo是赛诺菲和再生元公司研发的全人源化抗PD-1单克隆抗体,以前称为REGN281。通过阻断PD-1信号通路,它可以帮助人体的免疫系统杀伤肿瘤细胞。它已经获得了FDA"突破性治疗"认证。
此次批准是基于中期EMPOWER-CSCC 1试验和I期研究1423的数据。EMPOWER-CSCC 1结果已经在今年6月发表在NEJM杂志上,结果显示Libtayo治疗的患者有47.5%的响应率。
该疗法也正在欧洲监管机构进行审核,用于治疗不能手术的转移性或局部晚期CSCC患者。
原始出处:
本文系梅斯医学(MedSci)原创编译整理,转载需授权!
作者:MedSci
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






#细胞癌#
27
#PD-1单抗Libtayo#
26
#PD-1单抗#
40
#Libtayo#
31
#FDA批准#
28