J Thorac Oncol:OAK研究再分析:NSCLC进展后继续阿替利珠单抗治疗仍可获益
2018-12-17 月下荷花 肿瘤资讯
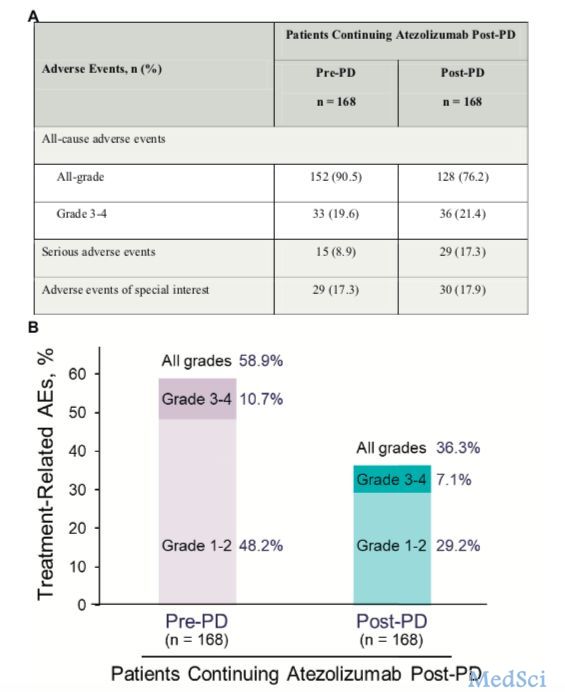
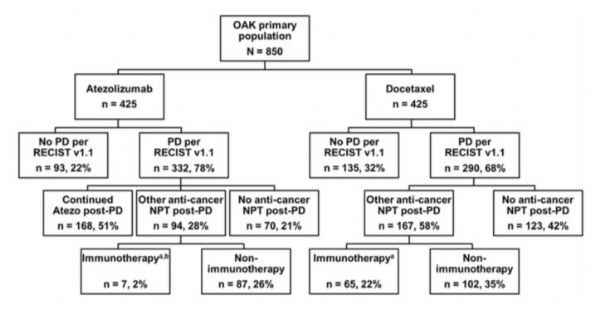
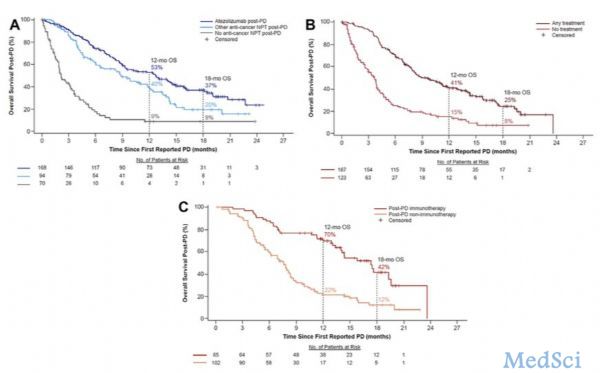
癌症免疫治疗可以改变肿瘤生物学,即便影像学进展时,治疗仍可能发挥作用。随机III期OAK研究中,进展期NSCLC接受阿替利珠单抗或多西他赛治疗,阿替利珠单抗治疗患者总生存(OS)获益,但客观反应率(ORR)或无进展生存(PFS)无改善。美国Gandara教授在J Thorac Oncol杂志上发文,对OAK研究进一步分析,结果表明进展后继续阿替利珠单抗治疗有良好的获益-风险比。
作者:月下荷花
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#THORAC#
34
#OAK研究#
31
#替利珠单抗#
50
#Oncol#
32
学习了
88