点击查看文中指南原文:
点击查看引用文献期刊专区:
质子泵抑制剂(PPIs)是用于治疗消化性溃疡常用的药物,在肿瘤患者中有20%~33% 的患者使用 PPIs 来缓解胃食管反流的症状,而在胃肠道癌症、胰腺癌、胶质母细胞瘤、胃肠道间质瘤中的使用频率更高(35%~50%)。目前临床常用的PPI包括奥美拉唑、雷贝拉唑、埃索美拉唑等等。
然而,目前众多的临床试验研究结论指出,PPI的“滥用”会影响抗肿瘤治疗的疗效。无论是在化疗、靶向治疗及免疫治疗方面均有体现。下面就PPI对于抗肿瘤治疗的疗效影响做一下梳理。
最新研究表明,抗生素和PPI的使用可能与接受 ICI 治疗的癌症患者的不良预后有关。抗生素(ATB)和质子泵抑制剂(PPI)的使用会改变肠道微生物群的组成和多样性,从而影响免疫系统,进而干扰对抗PD1免疫检查点抑制剂(ICI)的反应。
发表在Front Immunol上的这篇文章会对我们有部分启示。该文章回顾性纳入了212例用ICI治疗非小细胞肺癌、黑色素瘤、消化道肿瘤或肾细胞癌的患者。

在ICI开始前60天内接受ATB治疗的患者被纳入ATB+组。在ICI开始前30天内接受PPI的患者被纳入PPI +组。将最终符合标准的患者分为4组,即:ATB-/PPI-,ATB+/PPI-,ATB-/PPI+,ATB+/PPI+。
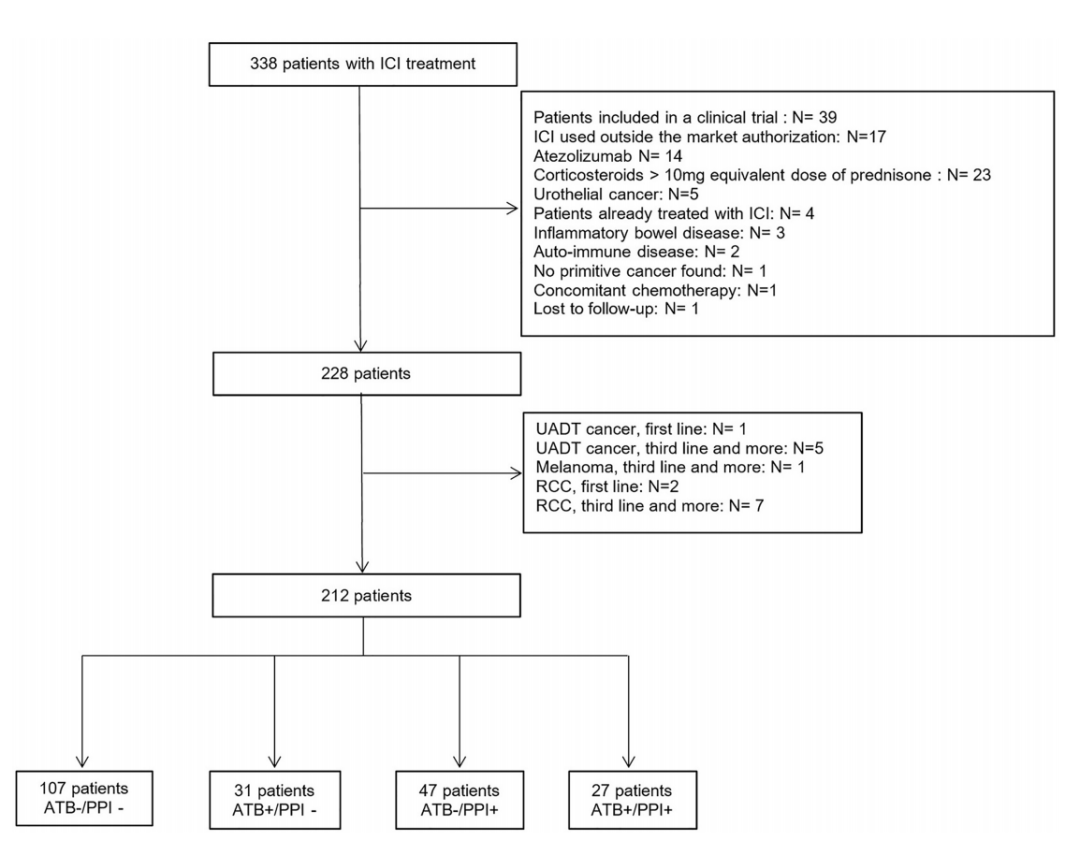
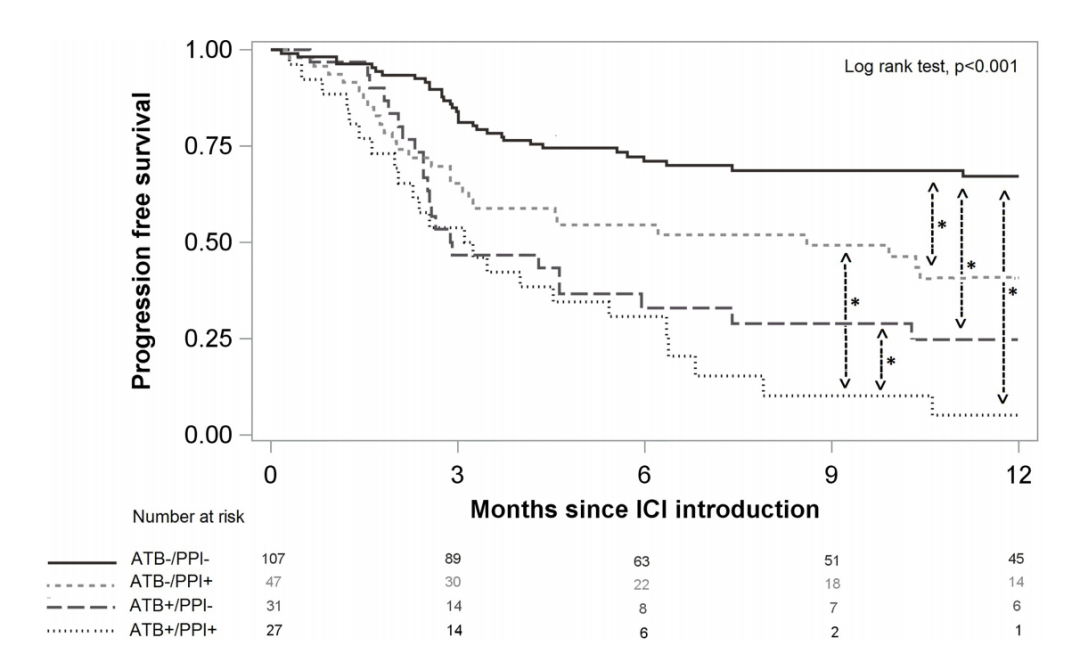
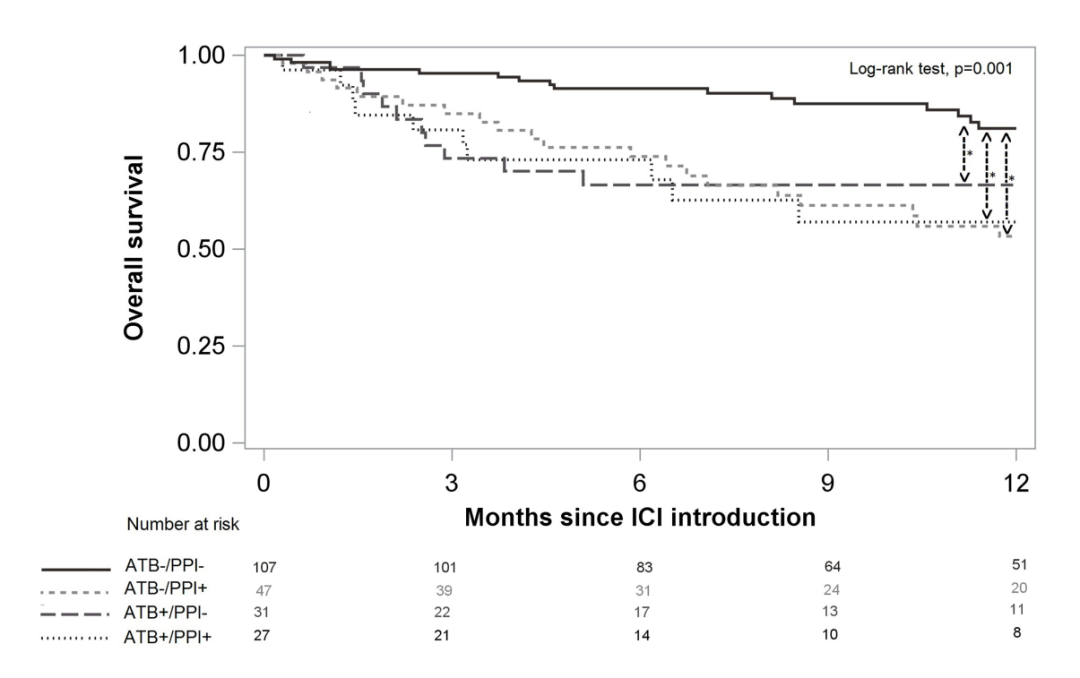 最终结果:6个月时的PFS为56.7%,95% CI(49.6%;63.2%),12个月时为47.2%,95%CI(39.8%;54.1%)。OS在6个月时为81.6%,95%CI(75.6%;86.2%),在12个月时为69.4%,95%CI(61.9%;75.7%)。与ATB-/PPI-组相比,ATB+/PPI-组的PFS较低[危险比(HR)1.90,95%CI(1.41;2.57)]和ATB-/PPI+组[HR 1.51,95%CI(1.11;2.05)],ATB+/PPI+组最低[HR 3.65,95%CI(2.75;4.84)]。对于OS而言,无论是单独使用ATB或PPI,亦或是联合使用ATB和PPI都是导致死亡的一个危险因素,并且ATB和PPI的组合不会进一步增加风险。在观察到78例(36.8%)中不良事件中,ATB或PPI的使用没有显著影响。
最终结果:6个月时的PFS为56.7%,95% CI(49.6%;63.2%),12个月时为47.2%,95%CI(39.8%;54.1%)。OS在6个月时为81.6%,95%CI(75.6%;86.2%),在12个月时为69.4%,95%CI(61.9%;75.7%)。与ATB-/PPI-组相比,ATB+/PPI-组的PFS较低[危险比(HR)1.90,95%CI(1.41;2.57)]和ATB-/PPI+组[HR 1.51,95%CI(1.11;2.05)],ATB+/PPI+组最低[HR 3.65,95%CI(2.75;4.84)]。对于OS而言,无论是单独使用ATB或PPI,亦或是联合使用ATB和PPI都是导致死亡的一个危险因素,并且ATB和PPI的组合不会进一步增加风险。在观察到78例(36.8%)中不良事件中,ATB或PPI的使用没有显著影响。
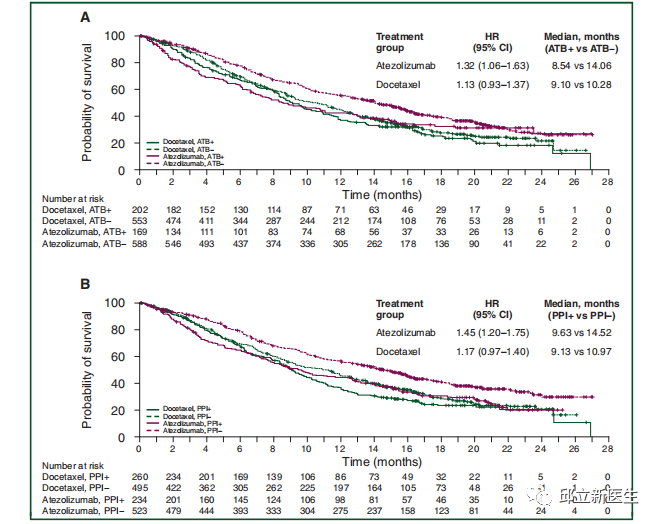
发表在Annals Of Oncology上的一篇关于抗生素、质子泵抑制剂与免疫治疗的疗效的文章,研究回顾性分析使用了来自II期POPLAR(NCT 01903993)和III期OAK(NCT 02008227)试验的汇总数据,其中包括1512名先前治疗过的非小细胞肺癌(NSCLC)患者,随机分配接受阿特珠单抗(n/757)或多西他赛(n/755)。主要目的是评估ATB和PPI的使用对总生存率(OS)和无进展生存率(PFS)的影响。


本研究回顾性分析使用了来自II期POPLAR(NCT 01903993)和III期OAK(NCT 02008227)试验的汇总数据,其中包括1512名先前治疗过的非小细胞肺癌(NSCLC)患者,随机分配接受阿特珠单抗(n/757)或多西他赛(n/755)。主要目的是评估ATB和PPI的使用对总生存率(OS)和无进展生存率(PFS)的影响。
结果显示,阿特珠单抗组169例(22.3%)和多西紫杉醇组202例(26.8%)分别给予ATB和PPI,分别为234例(30.9%)和260例(34.4%)。所有患者的多变量分析显示,ATB与较短的OS相关[危险比(HR)1.20,95%可信区间(CI)1.04e1.39],与PPI相关(HR 1.26,95%可信区间1.10e1.44)。在阿特珠单抗组中,接受ATB(8.5对14.1个月,HR 1.32,95%CI 1.06e1.63,P/4 0.01)或PPI(9.6对14.5个月,HR 1.45,95%CI 1.20e1.75,P/4 0.0001)的患者的OS显著缩短。使用PPI与阿特珠单抗PFS较短相关(1.9个月与2.8个月,HR为1.30,95%CI为1.10?1.53分,P 0.001)。在多西紫杉醇人群中,ATB和PPI的使用与多西他赛之间没有关联。数据表明,转移性NSCLC患者使用ATB或PPI与预后不良相关,并可能影响ICI的疗效。
一项基于SEER数据库的研究显示对于≥65岁的老年肿瘤患者, TKIs治疗期间联合应用质子泵抑制剂(PPIs)的比例高达22%。厄洛替尼联合PPIs治疗的肺癌患者90天内死亡风险增加21%, 1年内死亡风险增加11%。

Chu 等回顾性分析抑酸剂对厄洛替尼疗效的影响,共纳入507 例NSCLC 患者,抗酸组中115 例服用PPIs,9 例服用H2RA。研究结果显示联合组(抑酸药物+ 厄洛替尼)和单药组(厄洛替尼)的无进展生存期(progress free survival,PFS)分别为1.4 和2.3 月(P<0.001),总生存期(overall survival, OS)分别为12.9 和16.8 月(P=0.003),差异均有统计学意义。

Niho 等进行了一项回顾性研究,纳入分析了117例服用吉非替尼 250 mg/d 的晚期 NSCLC 患者,分为抗酸组和非抗酸组进行治疗,研究结果显示抗酸组(PPIs/H2RA)和非抗酸组的中位 PFS 分别为 8.7和 10.7月( P=0.13),客观缓解率(objective responserate, ORR)分别为 64% 和 63%( P=0.92),OS 分别为 20.1 和 24.3 月( P=0.07),两组 ORR、PFS 无明显差异,但OS有统计学差异。

此外,关于吉非替尼的另外一项研究同样也提示联合PPIs治疗会增加患者的死亡风险。

一项评估 PPIs 对达可替尼生物利用度影响的临床研究,24名健康男性志愿者被纳入该项研究,结果显示雷贝拉唑可使达可替尼中位 tmax 延迟,AUCinf 和 Cmax 分别下降 71.1% 和49.5%,这表明与雷贝拉唑联用时,达克替尼的血药浓度显著降低,提示应避免将达可替尼与 PPIs 联用。在《新型抗肿瘤药物临床应用指导原则 2020 版》中,对于治疗晚期 EGFR 突变的非小细胞肺癌的二代 EGFR 抑制剂达可替尼的合理用药要点中也明确指出:在服用达可替尼时,避免同时使用质子泵抑制剂;可使用局部作用的抗酸剂或 H2 受体拮抗剂代替质子泵抑制剂;必须临时服用 H2 受体拮抗剂的情况下,至少提前6小时或滞后10小时后给予本品。
2016 年在《JAMA Oncology》上了一项研究,目的在于确定质子泵抑制剂会不会降低卡培他滨的疗效。该研究对 545 例晚期 Her-2 阳性的胃食管癌患者接受卡培他滨和奥沙利铂(CapeOx)联合或不联合拉帕替尼(TRIO-013/LOGiC)再分析。

通过药物记录确定质子泵抑制剂的使用情况,比较接受 PPI 治疗的患者与未接受 PPI 治疗的患者的无进展生存期(PFS)和总体生存期(OS)。
结果显示:纳入分析的 545 例患者中(中位年龄 60 岁,男性 406 例)其中接受 PPI 的患者 229 名(拉帕替尼,n=110;对照组,n=119),平均分布在两组之间。接受 CapeOx 方案的患者中,使用质子泵抑制和未使用质子泵抑制剂两组的中位 PFS(4.2 个月 vs.5.7 个月;HR=1.55;95%CI 1.29-1.81,P<0.01)和中位 OS(9.2 个月 vs.11.3 个月;HR=1.34;95%CI,1.06-1.62,P=0.04),疾病控制率为(72% vs. 83%;P=0.02)。在多因素分析中也显示接受 PPI 的患者有更短的 PFS(P<0.01)。
结论:质子泵抑制剂可能会提高胃的 pH 值,从而降低了对卡培他滨疗效。然而,该研究并没有检验药代动力学和循环药物水平,因此这个分析并不能直接与潜在降低卡培他滨的吸收相联系。同样在酪氨酸激酶抑制剂厄洛替尼、舒尼替尼的肿瘤靶向治疗中也观察到了同样的现象。
那么肿瘤患者到底能不能用PPI呢?
为进一步规范质子泵抑制剂(PPI)的临床应用,促进合理用药,国家制定了《质子泵抑制剂临床应用指导原则(2020 年版)》。文中明确指出:由于化疗药及糖皮质激素可引起患者黏膜损伤、消化不良、应激性溃疡的发生。在肿瘤化疗过程中可考虑应用质子泵抑制剂改善患者烧心、恶心的症状,改善肿瘤患者的生活质量。但是,不建议常规化疗前的预防性使用质子泵抑制剂。
对于预防性使用PPI以下指南也做出明确的限定
《质子泵抑制剂预防性应用专家共识 2018》中指出,肿瘤患者在静脉使用存在致吐风险的化疗药物时,可以短程静脉应用 PPIs。
在 2019 年《预防性使用质子泵抑制剂及处方精简专家指导意见 2019》中指出:①尽管国内外多个肿瘤化疗止吐指南共识提及 PPI 可用于化疗呕吐的防治,但基于目前的证据,不建议在常规化疗中使用 PPI 进行预防呕吐或可能发生的上消化道症状。②若患者并发消化道症状可予短期 PPI 对症处理,且应尽量给予口服剂型。③若继发消化道出血应在专科医生指导下治疗性用药。
2020 年 5 月《质子泵抑制剂优化应用专家共识 2020》指出,对于肿瘤化疗致胃黏膜损伤的预防的优化建议是:不推荐在化疗期间常规使用 PPIs 预防胃黏膜损伤;肿瘤患者使用存在致吐风险的化疗药物时,如果伴有胃部不适,可在止吐方案中短程应用 PPIs 对症处理至化疗结束。
基于上述循证医学证据,在肿瘤治疗过程中,务必慎用质子泵抑制剂。
参考文献
1.Giordan Q, Salleron J, Vallance C, et al. Impact of Antibiotics and Proton Pump Inhibitors on Efficacy and Tolerance of Anti-PD-1 Immune Checkpoint Inhibitors. Front Immunol. 2021 Oct 27;12:716317.
2.Pinato DJ, Howlett S, Ottaviani D, et al. Association of Prior Antibiotic Treatment With Survival and Response to Immune Checkpoint Inhibitor Therapy in Patients With Cancer. JAMA Oncol. 2019 Dec 1;5(12):1774-1778.
3.Chalabi M, Cardona A, Nagarkar DR, et al. Efficacy of chemotherapy and atezolizumab in patients with non-small-cell lung cancer receiving antibiotics and proton pump inhibitors: pooled post hoc analyses of the OAK and POPLAR trials. Ann Oncol, 2020, 31(4): 525-531.
4. Sharma M, Holmes HM, Mehta HB, et al. The concomitant use of tyrosine kinase inhibitors and proton pump inhibitors: Prevalence, predictors, and impact on survival and discontinuation of therapy in older adults with cancer. Cancer, 2019, 125(7): 1155-1162. doi:10.1002/cncr.31917
5. Chu MP, Ghosh S, Chambers CR, et al. Gastric acid suppression isassociated with decreased erlotinib efficacy in non–small-cell lung cancer[J]. Clinical Lung Cancer, 2015, 16(1): 33-39
6. Niho S, You Y, Zenke k, et al. Clinical impact of gastric acidsuppressing medication use on the efficacy of erlotinib and gefitinib in patients with advanced non-small-cell lung cancer harboring EGFR mutations[J] . Clin Lung Cancer, 2016, 17(5), 412-418.
7. Fang YH, Yang YH. Concurrent proton-pump inhibitors increase risk of death for lung cancer patients receiving 1st-line gefitinib treatment-a nationwide population-based study. Cancer Manag Res, 2019, 11: 8539-8546. doi: 10.2147/cmar.s222278
8. Ruiz-Garcia A, Masters JC, Laure MDC, et al. Effect of food orproton pump inhibitor treatment on the bioavailability of dacomitinib in healthy volunteers[J]. The Journal of Clinical Pharmacology, 2016, 56(2): 223-230.
10. Capecitabine Efficacy in Advanced Gastroesophageal Cancer.JAMA Oncology.June 2017 doi:10.1001/jamaoncol.2016.3358.
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#抑制剂#
75
学习了
40
#质子泵#
61
#质子泵抑制剂##肿瘤##癌症#
82
#肿瘤治疗#
58