急性肺栓塞的诊治策略,流程图清晰总结!
2023-08-03 白静 薛亚军 中国医学论坛报今日循环
对怀疑急性PE的患者采取“三步走”策略,首先进行临床可能性评估,再进行初始危险分层,然后逐级选择检查手段以明确诊断。
诊断
肺栓塞(PE)不仅临床表现不特异,常规检查如胸片、心电图、血气分析、超声心动图等也缺乏特异性。多排螺旋CT、放射性核素肺通气灌注扫描、肺动脉造影常能明确诊断,但费用高,尤其肺动脉造影具有侵入性,许多基层医院尚不具备检查条件。结合我国实际情况,参照欧洲心脏病学会(ESC)2014年急性PE诊疗指南,我们推荐对怀疑急性PE的患者采取“三步走”策略,首先进行临床可能性评估,再进行初始危险分层,然后逐级选择检查手段以明确诊断。
1. 临床可能性评估
常用的临床评估标准有加拿大Wells评分和修正的Geneva评分。这两种评分标准简单易懂,所需的临床资料易于获得,适合在基层医院普及。最近,Wells和Geneva法则都进行了简化,更增加了临床实用性,其有效性也得到了证实(表2、表3)。
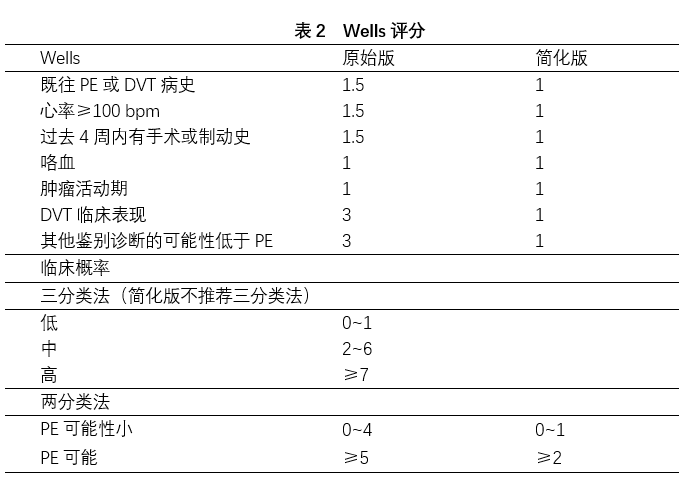
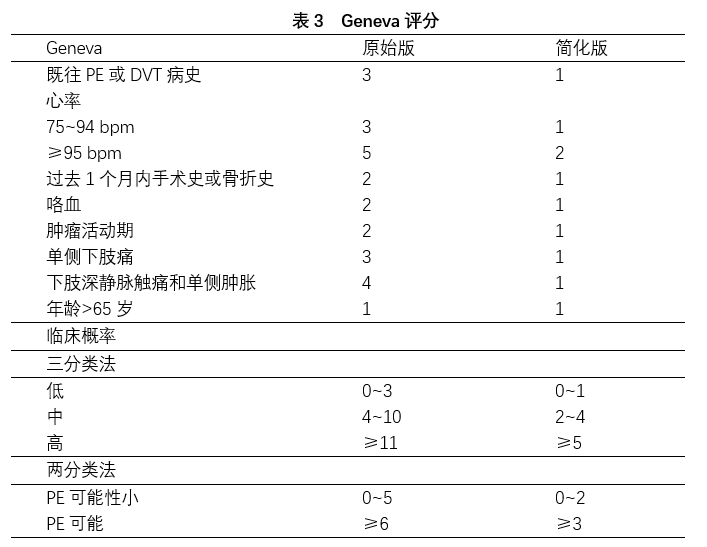
2.初始危险分层
对急性PE的严重程度进行初始危险分层(图1)以评估PE的早期死亡风险(包括住院死亡率或30天死亡率)。初始危险分层主要根据患者当前的临床状态,只要存在休克或者持续低血压即为高危PE,休克或者持续低血压是指收缩压<90 mmHg,或收缩压下降≥ 40 mmHg并持续15分钟以上,排除新发心律失常、血容量下降、脓毒血症。如无则为非高危PE。此分层方法对诊断和治疗策略都具有非常重要意义,由此决定下一步诊疗策略。
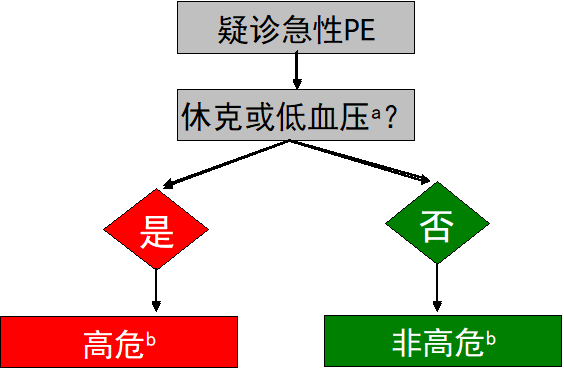
PE=肺栓塞
a.排除新发心律失常、血容量下降、脓毒血症后,收缩压<90 mmHg,或收缩压下降≥ 40 mmHg并持续15分钟以上
b.基于住院或30天死亡率
图1 急性PE初始危险分层
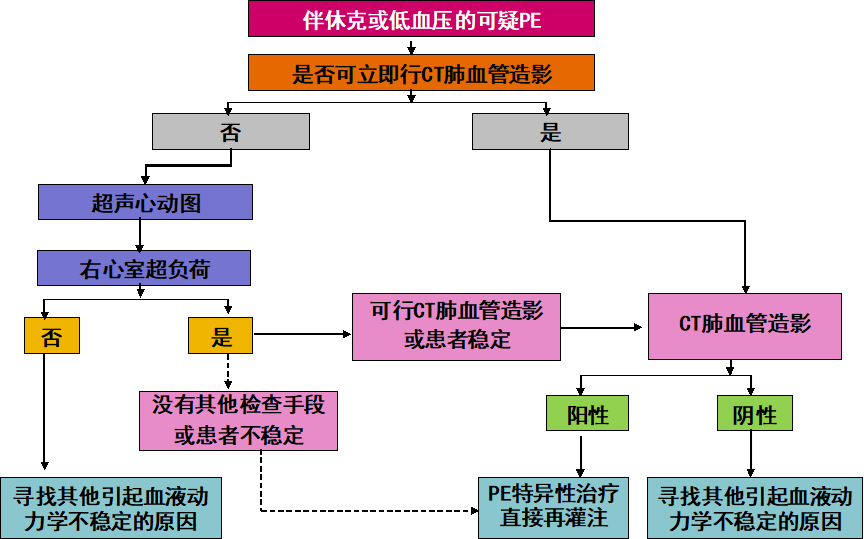
图2 可疑高危PE患者诊断流程图
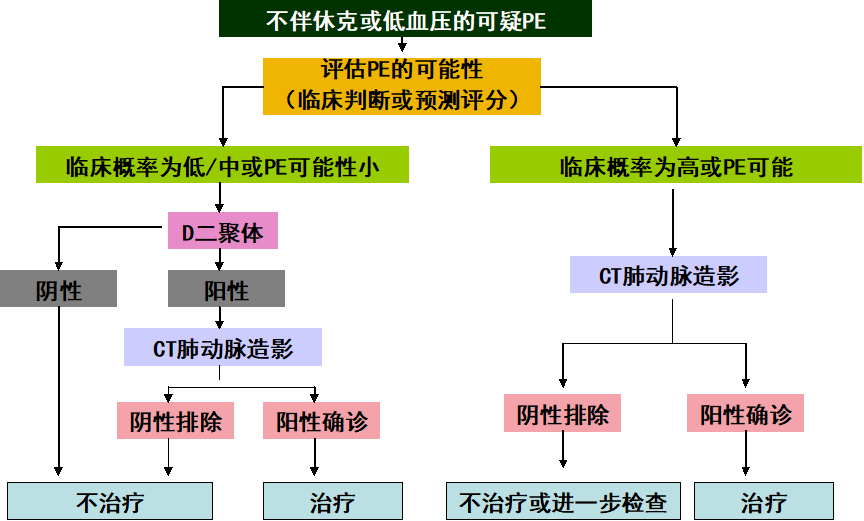
图3 可疑非高危PE患者诊断流程图
治疗
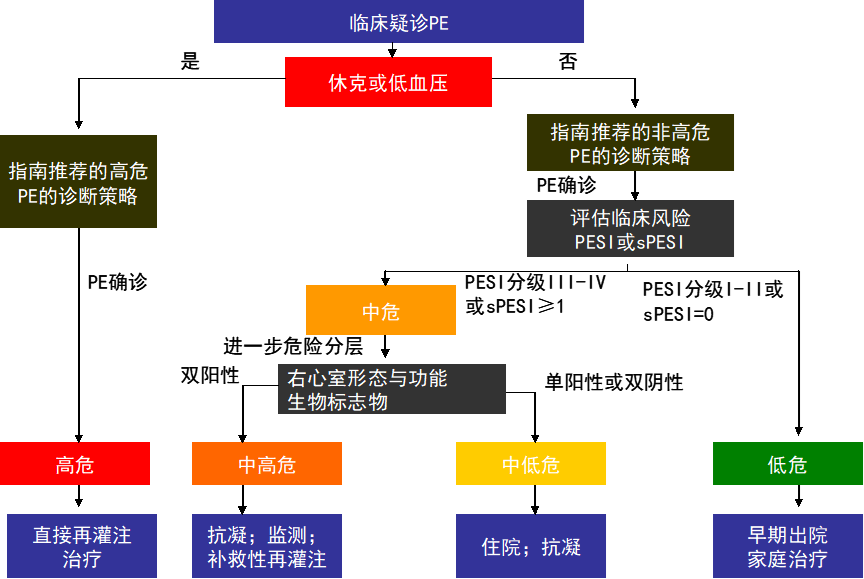
图4 基于危险度分层的急性PE治疗策略
急性期治疗
1.血流动力学和呼吸支持
急性右心衰及其导致的心排血量不足是PE患者死亡的首要原因。因此,PE合并右心衰患者的支持治疗极其重要。研究提示积极扩容不仅无益,反而有可能因过度机械牵张或反射机制抑制心肌收缩力而恶化右心功能。对心排血指数低、血压正常的PE患者,给予适度的液体冲击(500 ml),有助于增加心排血量。
在药物、外科或者介入再灌注治疗的同时,通常需使用升压药。去甲肾上腺素通过直接正性肌力作用能改善右心室功能,同时通过刺激外周血管α受体升高体循环血压,也能改善右心室冠状动脉灌注,但应限于低血压患者。多巴酚丁胺和(或)多巴胺对心排血指数低、血压正常的PE患者有益,但应掌握尺度,超过生理范围的心排血指数可导致血流由阻塞血管向未阻塞血管的进一步重新分配,从而加重通气/血流比失调。肾上腺素兼具去甲肾上腺素和多巴酚丁胺的优点,而无体循环扩血管效应,可能对PE伴休克患者有益。
血管扩张剂降低肺动脉压力和肺血管阻力,但这些药物缺乏肺血管特异性,经体循环给药后可能导致体循环血压进一步降低。吸入一氧化氮可能改善PE患者的血流动力学状态和气体交换。左西孟旦在扩张肺动脉的同时增加右心室收缩力,有助于恢复急性PE患者的右心室-肺动脉耦联。
PE患者常伴中等程度的低氧血症和低碳酸血症。低氧血症通常在吸氧后逆转。当给予机械通气时,需注意尽量减少其不良的血流动力学效应。机械通气造成的胸腔内正压会减少静脉回流,恶化血流动力学不稳定PE患者的右心衰。因此,呼气末正压要慎用。应给予较低的潮气量(约6 ml/kg去脂体重),以保持吸气末平台压力<30 cm H2O。
2. 抗凝
急性PE患者推荐抗凝治疗,目的在于预防早期死亡和VTE复发。
2.1 肠外抗凝剂
对于高或中等临床可能性PE患者,在等待诊断结果的同时应给予肠外抗凝剂(I,C)。肠外抗凝剂普通肝素、低分子量肝素或磺达肝癸钠均有即刻抗凝作用。初始抗凝治疗,低分子量肝素和磺达肝癸钠优于普通肝素,发生大出血和肝素诱导血小板减少症(heparin-induced thrombocytopenia,HIT)的风险也低。而普通肝素具有半衰期短、抗凝效应容易监测、可迅速被鱼精蛋白中和的优点,推荐用于拟直接再灌注的患者,以及严重肾功能不全(肌酐清除率<30 ml/min),或重度肥胖者。低分子量肝素和普通肝素主要依赖抗凝血酶系统发挥作用,如有条件,建议使用前和使用中检测抗凝血酶活性,如果抗凝血酶活性下降,需考虑更换抗凝药物。
-
普通肝素:首先给予负荷剂量2000~5000 IU或按80 IU/kg静脉注射,继之以18 IU/(kg·h)持续静脉滴注。抗凝必须充分,否则将严重影响疗效,导致血栓复发率明显增高。在初始24小时内需每4~6小时测定活化的部分凝血活酶时间(APTT) 1次,并根据APTT调整普通肝素的剂量(表5),每次调整剂量后3小时再测定APTT,使APTT尽快达到并维持于正常值的1.5~2.5倍。治疗达到稳定水平后,改为每日测定APTT 1次。应用普通肝素可能会引起HIT,在使用普通肝素的第3~5日必须复查血小板计数。若需较长时间使用普通肝素,应在第7~10日和14日复查血小板计数,普通肝素使用2周后则较少出现HIT。若患者出现血小板计数迅速或持续降低超过50%,或血小板计数小于100×109/L,应立即停用普通肝素,一般停用10日内血小板数量开始逐渐恢复。
-
低分子量肝素:所有低分子量肝素均应按照体重给药。一般不需常规监测,但在妊娠期间需定期监测抗Xa因子活性。抗Xa因子活性的峰值应在最近一次注射后4小时测定,谷值则应在下一次注射前测定,每日给药2次的抗Xa因子活性目标范围为0.6~1.0 IU/ml,每日给药1次的目标范围为1.0~2.0 IU/ml。
-
磺达肝癸钠:是选择性Xa因子抑制剂, 2.5 mg皮下注射,每天1次,无须监测,但由于其消除随体重减轻而降低,对体重<50 kg的患者慎用。严重肾功能不全的患者(肌酐清除率<30 ml/min),因其将在体内蓄积,增加出血的风险,禁用磺达肝癸钠。对于中度肾功能不全的患者(肌酐清除率30~50 ml/min)应减量50%使用。
2.2 口服抗凝药
应尽早给予口服抗凝药,最好与肠道外抗凝剂同日给予(I,B)。50多年来,维生素K拮抗剂(vitamin K antagonist, VKA)一直是口服抗凝治疗的“金标准”,包括华法林、硝华法林、苯丙香豆素、苯茚二酮等,其中华法林国内最为常用。近年来,一些新型口服抗凝药开始应用于临床。
-
华法林:华法林是一种维生素K拮抗剂,它通过抑制依赖维生素K凝血因子(Ⅱ、Ⅶ、Ⅸ、Ⅹ)的合成而发挥抗凝作用。初始通常与普通肝素、低分子量肝素或磺达肝癸钠联用。
国外指南对于年轻人(<60岁)或较为健康的门诊患者推荐起始剂量为10 mg,老年人和住院患者为5 mg,5-7天后根据国际标准化比值(international normalized ratio,INR)调整每日剂量,当INR稳定在2.0~3.0时停止使用普通肝素、低分子量肝素或磺达肝癸钠,继续予华法林治疗。与西方人比较,亚洲人华法林肝脏代谢酶存在较大差异,中国人的平均华法林剂量低于西方人。我国房颤抗栓临床试验的结果表明,华法林的维持剂量大约为3 mg。为了减少过度抗凝的情况,根据2013年《华法林抗凝治疗的中国专家共识》,通常不建议给予负荷剂量,推荐初始剂量为1~3 mg,某些患者如老年、肝功能受损、慢性心力衰竭和出血高风险患者,初始剂量还可适当降低。为达到快速抗凝目的,华法林应与普通肝素、低分子量肝素或磺达肝癸钠重叠应用5天以上,当INR达到目标范围(2.0~3.0)并持续2天以上时,停用普通肝素、低分子量肝素或磺达肝癸钠。
国内外已经将华法林量效有关的基因多态性检测商品化,主要是CYP2C9和VKORCI,通过基因多态性检测有助于初始剂量的选择。但基因多态性仅能解释30%~60%的华法林个体差异,临床仍需综合考虑患者的体表面积、肝肾功能及合并用药等因素来选择合适的剂量。目前,国外指南不推荐对所有服用华法林的患者常规进行基因检测。如有条件,基因检测可作为华法利剂量调整的辅助手段。
-
非维生素K依赖的新型口服抗凝药:近年来大规模临床试验为非维生素K依赖的新型口服抗凝药(Non-vitamin K-dependent new oral anticoagulants,NOACs)用于PE或VTE急性期治疗提供了证据,包括达比加群、利伐沙班、阿哌沙班和依度沙班。目前,NOACs可以替代华法林用于初始抗凝治疗(I,B)。利伐沙班和阿哌沙班可作为单药治疗(不需合用肠外抗凝剂),但急性期治疗的前3周(利伐沙班)或前7天(阿哌沙班)需要增加口服剂量;达比加群和依度沙班必须联合肠外抗凝剂应用(I,B)。以上4种新型口服抗凝药均不能用于严重肾功能损害患者(Ⅲ,A)。
3.溶栓治疗
溶栓药物可直接或间接地将纤维蛋白溶酶原转变成纤维蛋白溶酶,迅速降解纤维蛋白,使血栓溶解;通过清除和灭活纤维蛋白原、凝血因子Ⅱ、Ⅴ、Ⅷ及纤维蛋白溶酶原,干扰凝血功能;纤维蛋白原降解产物增多,抑制纤维蛋白原向纤维蛋白转变,并干扰纤维蛋白的聚合。溶栓治疗可迅速溶解血栓和恢复肺组织灌注,逆转右心衰竭,增加肺毛细血管血容量及降低病死率和复发率。欧美多项随机临床试验证实,溶栓治疗能够快速改善肺血流动力学指标,提高患者早期生存率。国内一项大样本回顾性研究也证实,对急性PE患者用尿激酶或重组组织型纤溶酶原激活剂(rt-PA)溶栓治疗+抗凝治疗总有效率96.6%,显效率42.7%,病死率3.4%,显著优于对症治疗组和单纯抗凝治疗组。
3.1 临床常用溶栓药物及用法
我国临床上常用的溶栓药物有尿激酶(UK)和重组组织型纤溶酶原激活剂阿替普酶(rt-PA)两种。
(1)尿激酶:UK 20000 IU/(kg·2 h)静脉滴注。
(2)rt-PA:50~100 mg持续静脉滴注2 h,体重< 65 kg的患者给药总剂量不应超过1.5 mg/kg。
3.2 禁忌证
绝对禁忌证:(1)出血性卒中;(2)6个月内缺血性卒中;(3)中枢神经系统损伤或肿瘤;(4)近3周内重大外伤、手术或者头部损伤;(5)1个月内消化道出血;(6)已知的出血高风险患者。
相对禁忌证:(1)6个月内短暂性脑缺血发作(transient ischemic attack, TIA)发作;(2)口服抗凝药应用;(3)妊娠,或分娩后1周;(4)不能压迫止血部位的血管穿刺;(5)近期曾行心肺复苏;(6)难于控制的高血压(收缩压 >180 mm Hg);(7)严重肝功能不全;(8)感染性心内膜炎;(9)活动性溃疡。
值得注意的是,对于危及生命的高危PE患者,大多数禁忌证应视为相对禁忌证。
3.3 溶栓时间窗
肺组织氧供丰富,有肺动静脉、支气管动静脉、肺泡内换气三重氧供,因此肺梗死的发生率低,即使发生也相对比较轻。PE溶栓治疗的目的主要是尽早溶解血栓疏通血管,减轻血管内皮损伤,降低慢性血栓栓塞性肺高压的发生危险。因此,在急性PE起病48小时内即开始行溶栓治疗,能够取得最大的疗效,但对于那些有症状的急性PE患者在6~14天内行溶栓治疗仍有一定作用。溶栓治疗结束后,应每2~4 h测定APTT,当其水平低于基线值的2倍(或<80 秒)时,开始规范的肝素治疗。常规使用普通肝素或低分子量肝素治疗。由于溶栓的出血风险,以及有时可能需要立即停用并逆转肝素的抗凝效应,推荐溶栓治疗后的数小时继续给予普通肝素,然后可切换成低分子量肝素或者磺达肝癸钠。如患者在溶栓开始前已接受低分子量肝素或磺达肝癸钠,则普通肝素输注应推迟至最近一剂低分子量肝素注射后12小时(每天2次给药),或最近一剂低分子量肝素或磺达肝癸钠注射后24小时(每天1次给药)。
4. 外科血栓清除术
在血流动力学崩溃前,多学科迅速干预并实施个体化血栓清除术,可使围手术期的死亡率降低至6%或更低。术前溶栓增加了出血风险,但不是外科血栓清除术的绝对禁忌证。系列结果表明,术后患者存活率、WHO功能分级和生活质量均获得提高。
5.经皮导管介入治疗
介入治疗可去除肺动脉及主要分支内的血栓,促进右心室功能恢复,改善症状和存活率。对于有溶栓绝对禁忌证的患者,介入方法包括:(1)猪尾导管或球囊导管进行血栓碎裂;(2)液压导管装置进行血栓流变溶解;(3)抽吸导管进行血栓抽吸;(4)血栓旋切。对于没有溶栓禁忌证的患者,可同时经导管溶栓或者机械捣栓基础上药物溶栓。
6.静脉滤器
不推荐PE患者常规植入下腔静脉滤器(Ⅲ,A)。在有抗凝药物绝对禁忌证以及接受足够强度抗凝治疗后复发的PE患者,可以选择静脉滤器植入(Ⅱa,C)。观察性研究表明,静脉滤器植入可以减少PE急性期病死率,但增加VTE复发风险。尚无证据支持对近端静脉有漂浮血栓的患者常规植入静脉滤器。
7. 早期出院和家庭治疗
筛选不良事件风险低的急性PE患者早期出院和行院外治疗。
作者:白静 薛亚军
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言