晚期卵巢癌的治疗取得新进展,GEN-1在I / II期临床中取得喜人结果!
2021-02-26 Allan MedSci原创
OVATION 2研究结果显示,与对照组(仅护理标准)相比,治疗组(护理标准+ GEN-1)将患者的无进展生存期提高了33%。
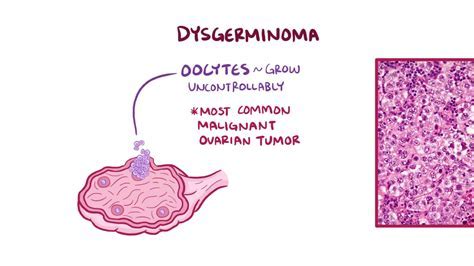
卵巢癌主要发生于50-70岁的女性。其发生率1/70。在美国,是位居第二位的常见妇科肿瘤。然而其死亡率高于其他妇科肿瘤。其病死率占女性肿瘤的第5位。
生物制药公司Celsion今天公布了GEN-1治疗晚期卵巢癌的I / II OVATION 2研究的最新信息。GEN-1是Celsion的DNA介导的白介素12(IL-12)免疫疗法,Celsion使用其专有的合成非病毒纳米颗粒递送系统平台设计。
OVATION 2研究探究了GEN-1联合标准新型辅助化疗(NACT)治疗初治III / IV期卵巢癌的有效性和安全性。NACT旨在最大程度地缩小肿瘤,以便在三个化疗周期后进行手术切除。NACT之后,患者接受间歇性减重手术,然后进行三个辅助化疗周期以及每周最多进行九次GEN-1附加治疗,其目的是延缓病情发展并改善总体生存期。
OVATION 2研究结果显示,与对照组(仅护理标准)相比,治疗组(护理标准+ GEN-1)将患者的无进展生存期提高了33%。
原始出处:
作者:Allan
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#I期临床#
47
#晚期卵巢癌#
62
#GEN-1#
49
#II期临床#
39