胰腺癌-CT分期2.0
2021-12-21 放射沙龙 网络
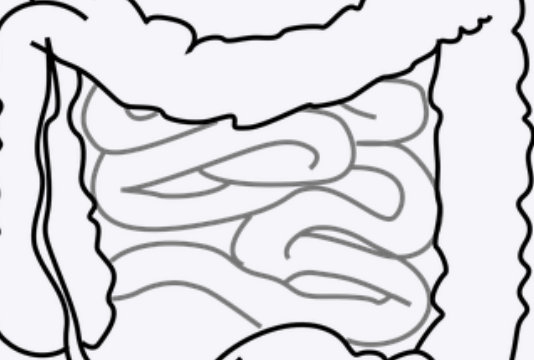
肿瘤的完全切除是唯一的治疗方法,但胰腺癌在早期很少被发现。40%的患者存在远处转移,40%的患者存在局部晚期胰腺癌(LAPC),这是无法切除的。
商务(微信):fsslong4
来源:缤纷影像
在这篇文章中,我们将重点讨论可切除性与不可切除性的标准,帮助您为胰腺癌分期和确定可切除性做出结构化报告。
肿瘤的完全切除是唯一的治疗方法,但胰腺癌在早期很少被发现。40%的患者存在远处转移,40%的患者存在局部晚期胰腺癌(LAPC),这是无法切除的。
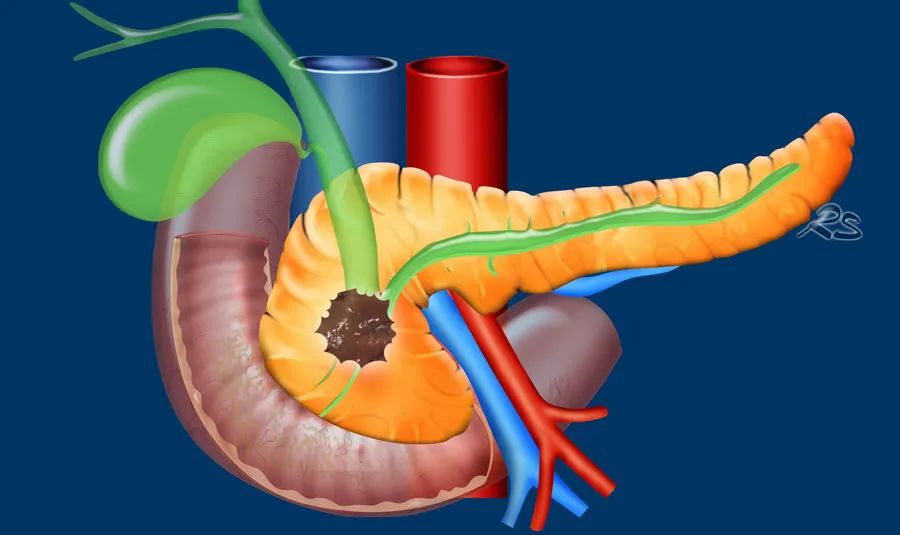
当没有远处转移时,是否可切除主要取决于以下因素:
-
肿瘤大小 -
临近血管结构的侵犯程度 -
侵犯邻近结构,如横系膜、肠系膜根和神经周浸润 -
淋巴结累及,区域或区域外
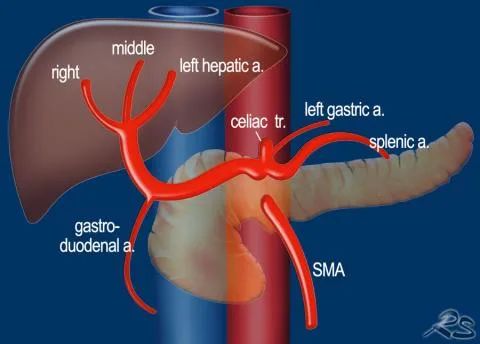
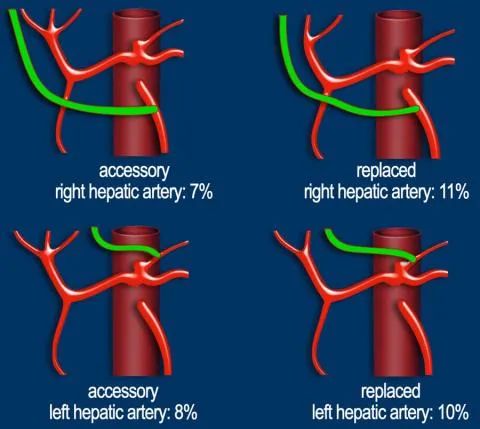
血管受累评估
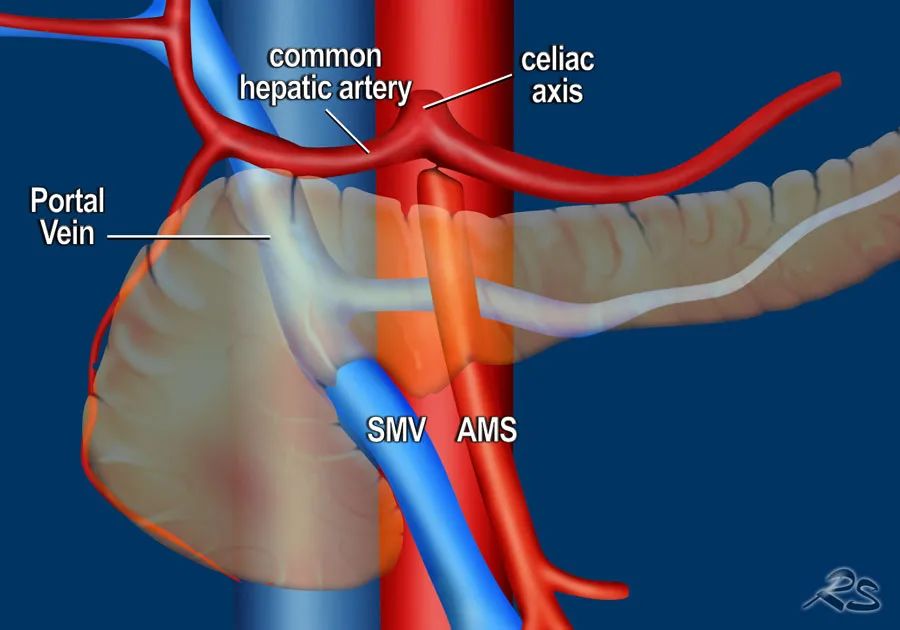
DPCG可切除性准则

-
神经周浸润 -
肠系膜根部侵犯 -
结肠系膜侵犯
-
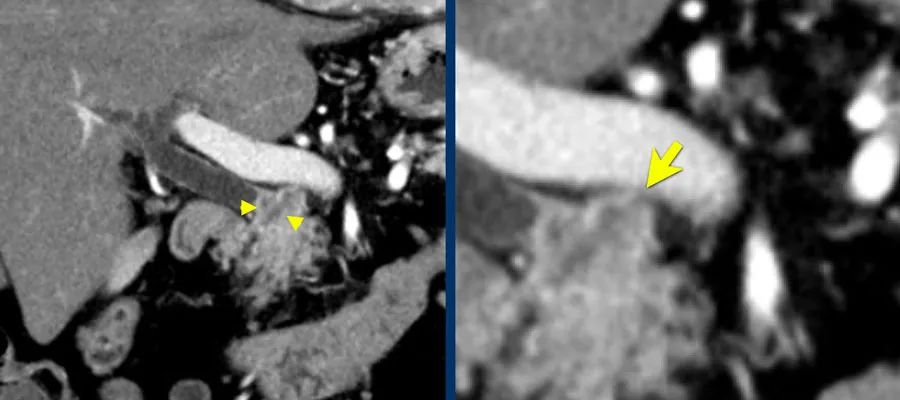
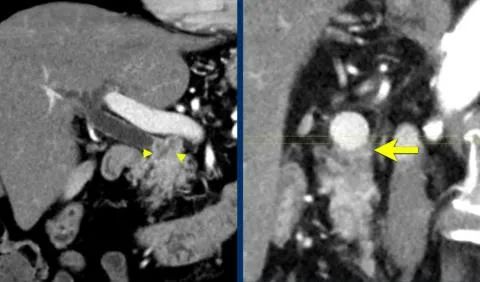
泪滴征 指PV或SMV的形状从椭圆形或圆形变为泪珠。这可能是肿瘤包裹或相邻纤维化所致。如下图 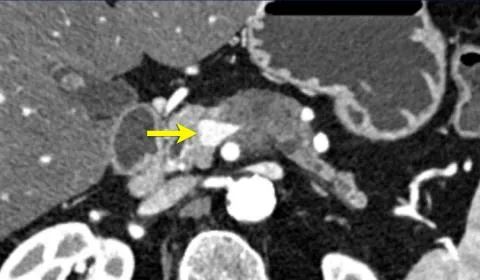
-
血管轮廓不规则 血管的不规则性暗示着血管的侵入。动脉的情况更是如此,因为动脉的壁比静脉的壁更厚。 -
血栓形成 动脉血栓的存在暗示着血管的侵入。
-
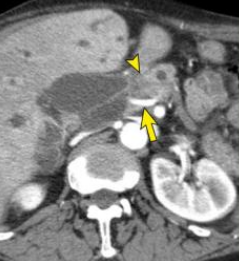
胰体肿瘤(白色箭头)。 -
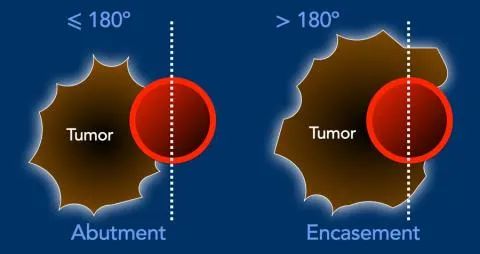
<90°的SMA接触。 -
与SMV有更广泛的90-180度接触,SMV略有缩小和变形(黄色箭头)。 -
胰管扩张
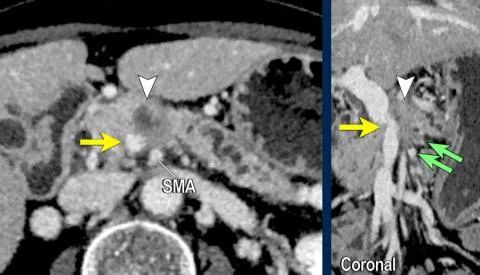
-
SMV的血管壁不规则(黄箭)。 -
胰体肿瘤(白色箭头)。 -
SMV侧支血栓形成(绿色小箭头)。
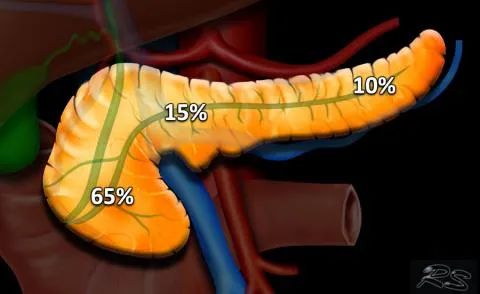
位置
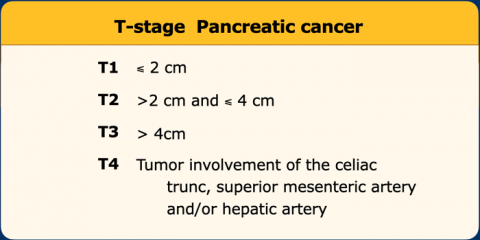
T-分期
其理由是,基于大小的定义更客观,因为很难确定胰外延伸。
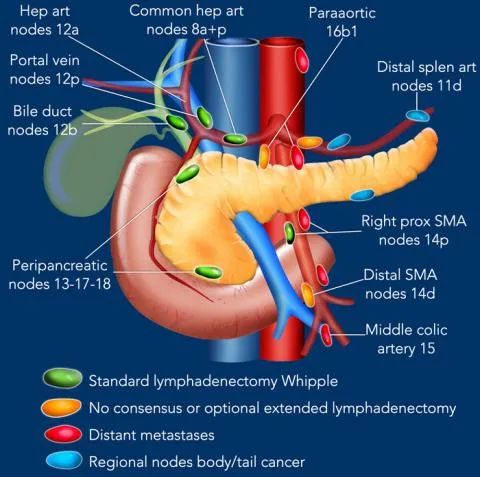
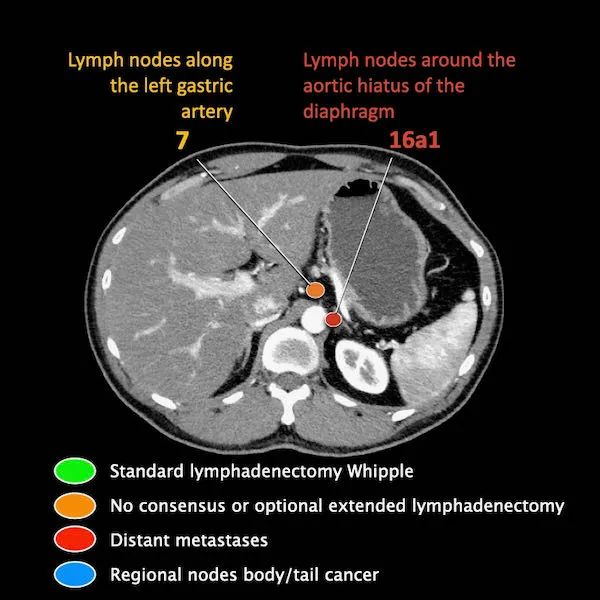
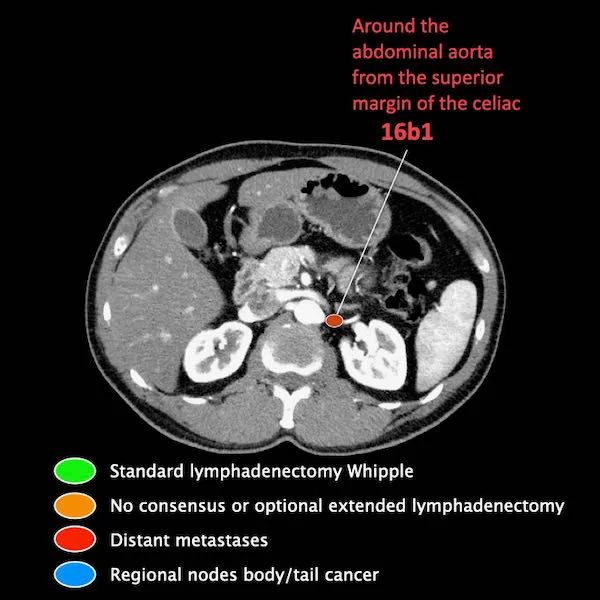
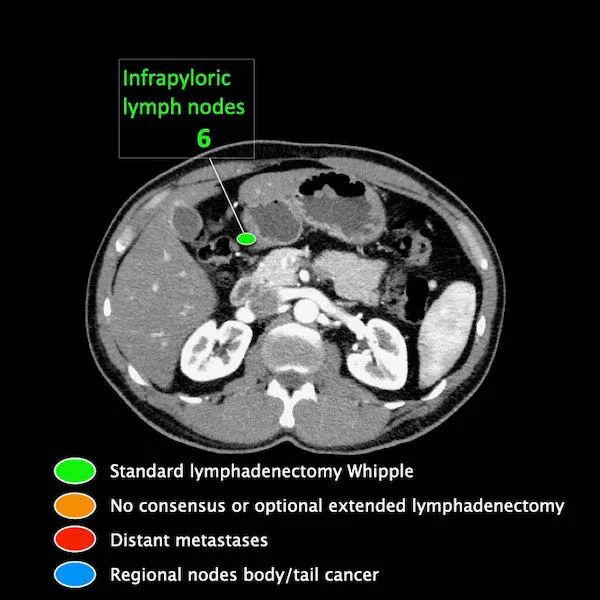
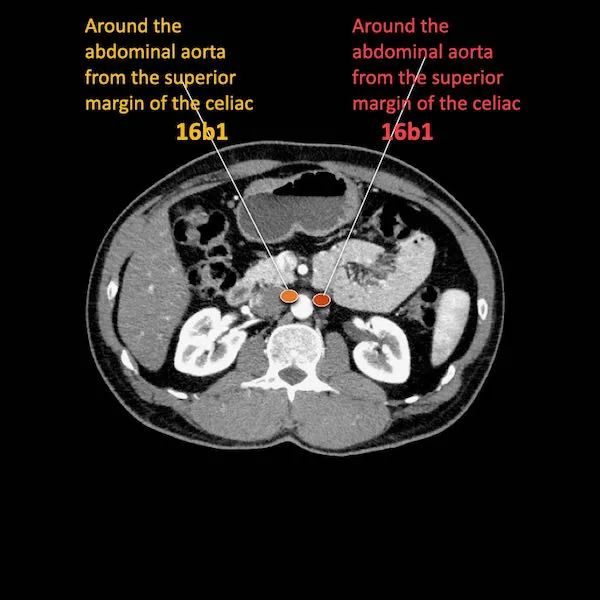
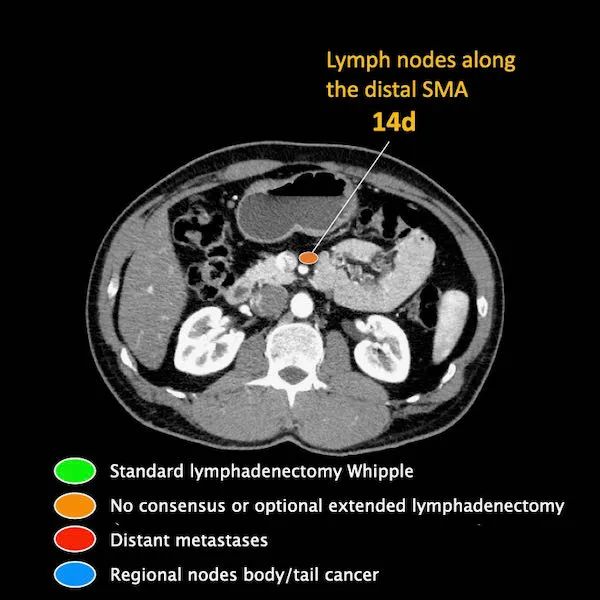
N分期
区域外的主要位置是主动脉旁和SMA旁。
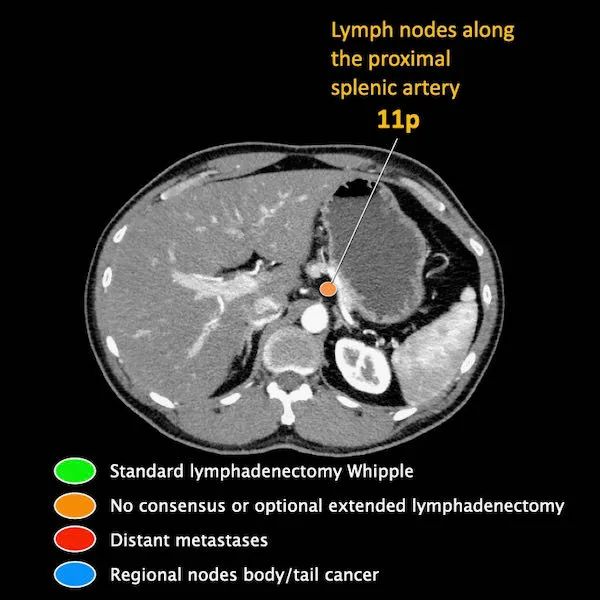
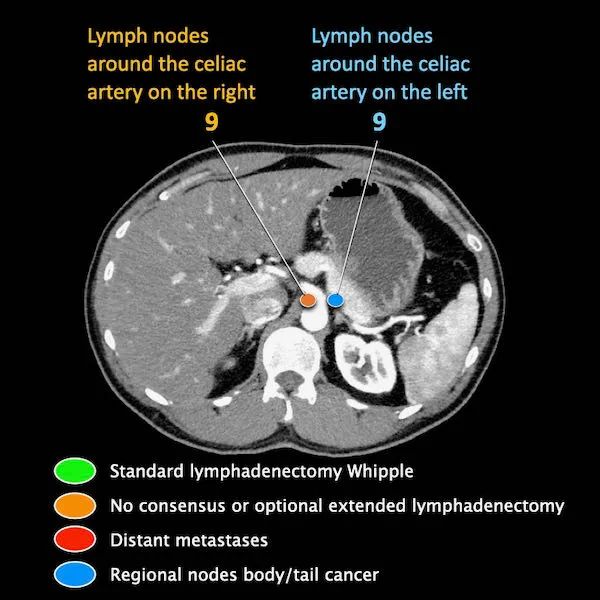
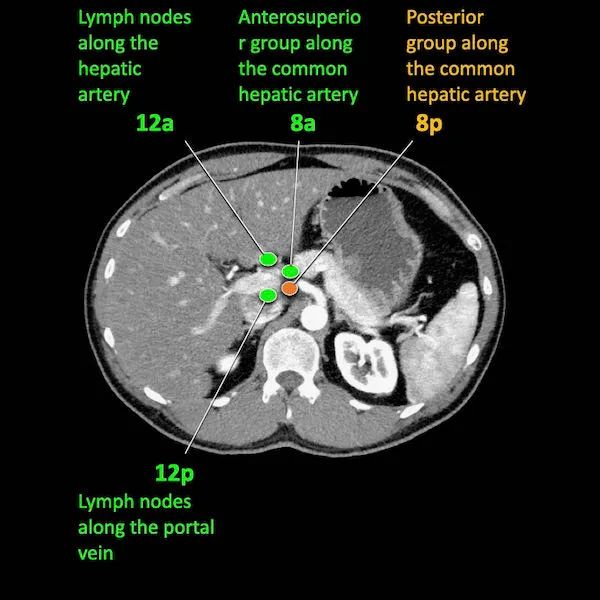
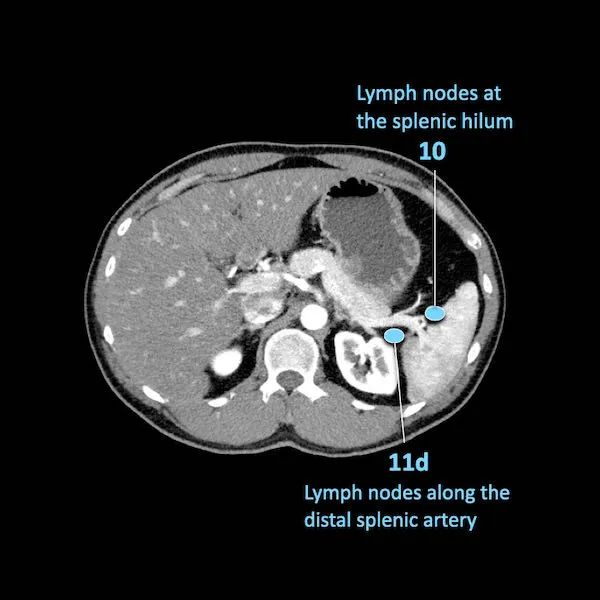

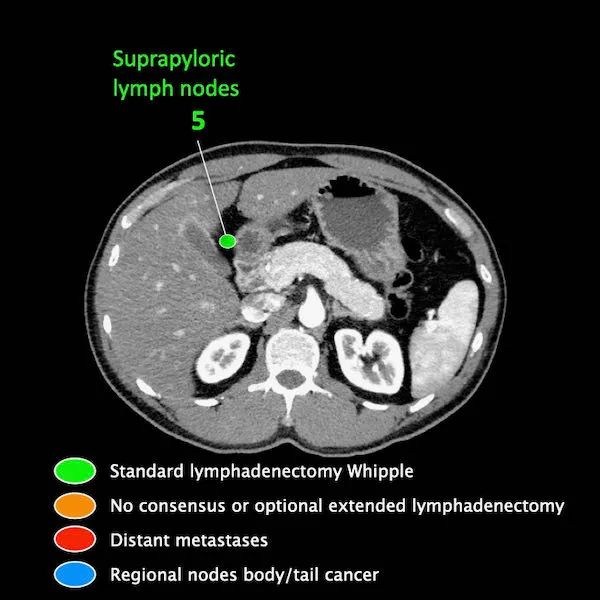
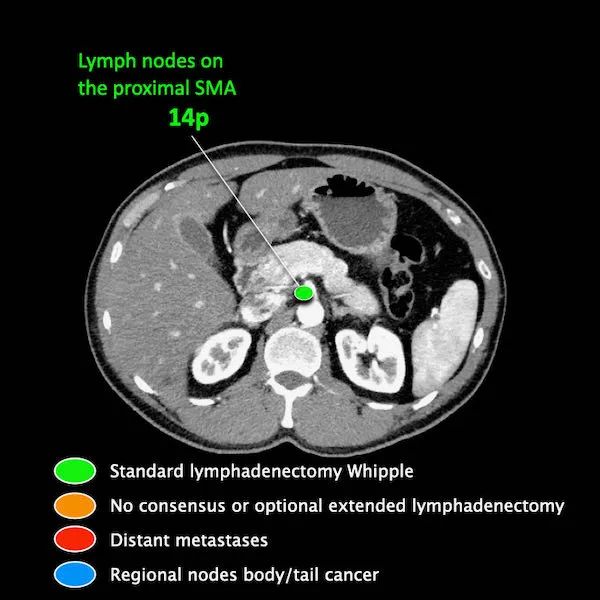
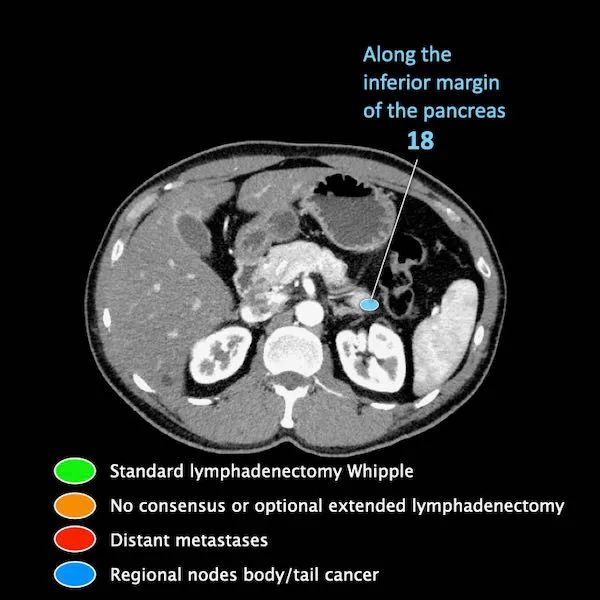
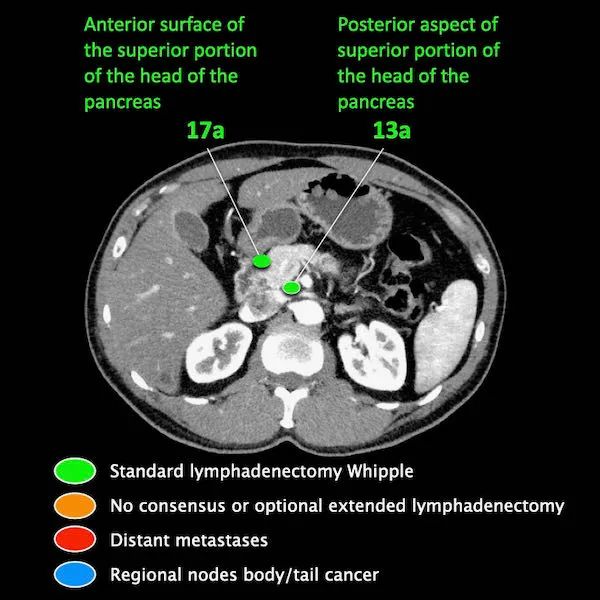
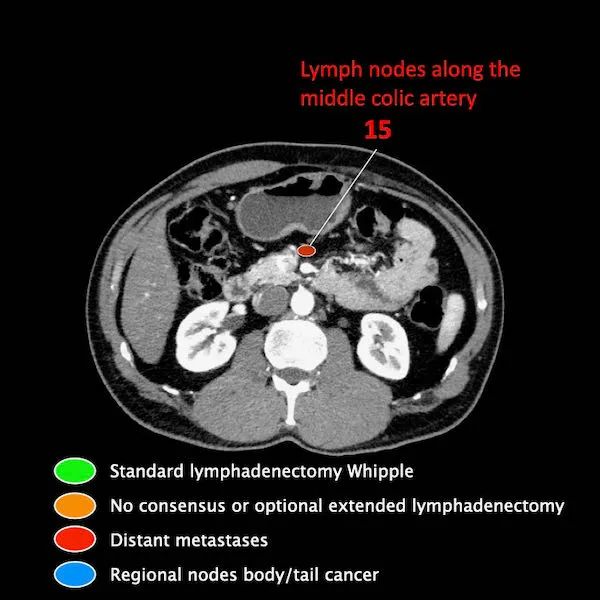

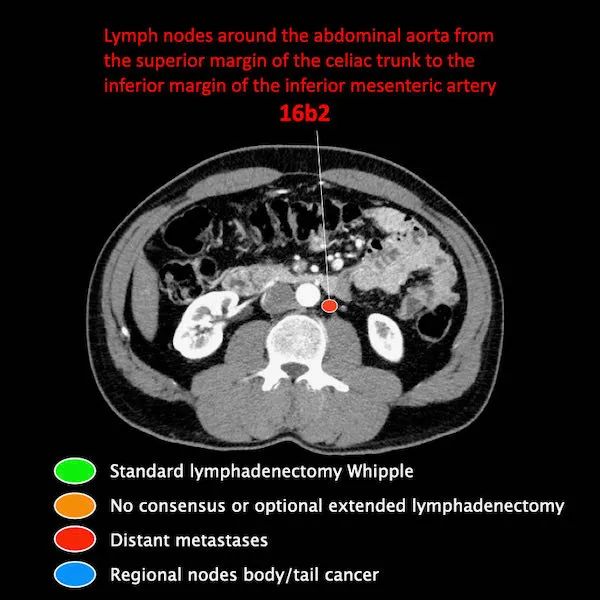
M分期
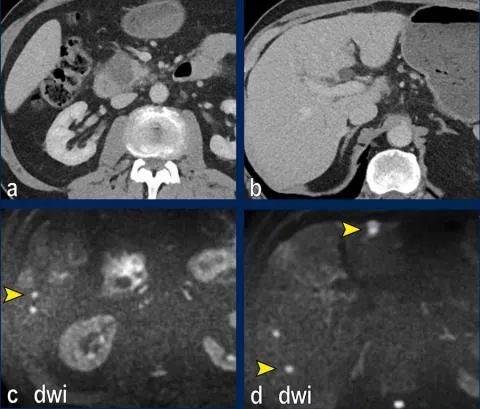
患者在几个星期后,DWI显示(c,d)超过10个肝转移。
外科医生感兴趣的其他发现
神经周浸润
它是早期复发和转移性疾病的重要预后因素。
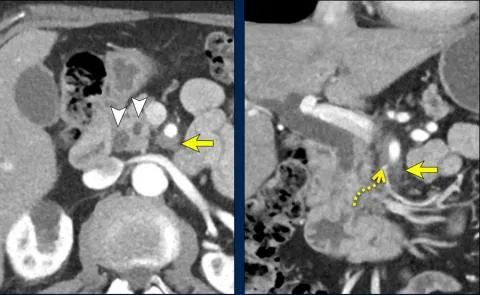
在这种情况下,导致与SMA 90-180度接触。
蔓延至肠系膜根部
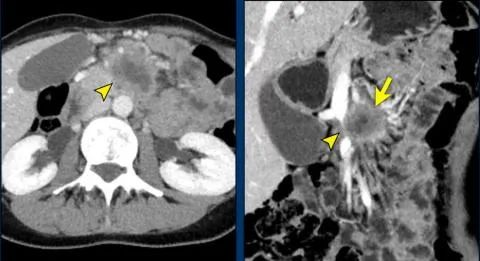
扩散到横结肠系膜
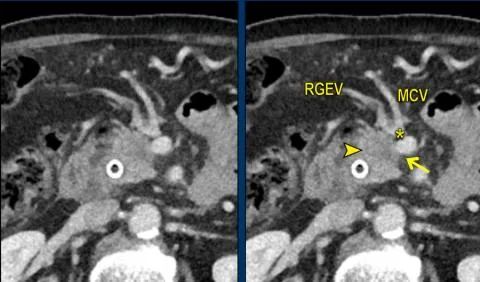
动脉解剖变异




作者:放射沙龙
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言