Cell子刊:中山大学赵洪云/张力发现晚期实体瘤和非霍奇金淋巴瘤的治疗新策略
2024-02-12 iNature iNature
该研究报道了ADG106在晚期实体瘤和非霍奇金淋巴瘤患者中的临床前特征和1期结果。
ADG106是一种靶向CD137 (4-1BB)的配体阻断激动抗体,在临床前研究中显示出令人鼓舞的结果,在多种动物模型中显示出肿瘤抑制作用,并显示出安全性和有效性之间的平衡。
2024年2月7日,中山大学赵洪云及张力共同通讯在Cell Reports Medicine 在线发表题为“Preclinical characterization and phase 1 results of ADG106 in patients with advanced solid tumors and non-Hodgkin’s lymphoma”的研究论文,该研究报道了ADG106在晚期实体瘤和非霍奇金淋巴瘤患者中的临床前特征和1期结果。
这项1期研究纳入了62例晚期恶性肿瘤患者,显示出良好的耐受性,高达5.0 mg/kg的剂量水平。10.0 mg/kg剂量限制性毒性仅发生在1例患者中(6.3%),导致4级中性粒细胞减少。最常见的治疗相关不良事件包括白细胞减少(22.6%)、中性粒细胞减少(22.6%)、丙氨酸转氨酶升高(22.6%)、皮疹(21.0%)、瘙痒(17.7%)和天冬氨酸转氨酶升高(17.7%)。晚期实体瘤和非霍奇金淋巴瘤的总体疾病控制率分别为47.1%和54.5%。循环生物标志物提示ADG106参与靶标,循环T、B和自然杀伤细胞以及细胞因子干扰素γ和白细胞介素6的免疫调节,这可能影响临床疗效的可能性。ADG106在晚期癌症患者中具有可控的安全性和初步的抗肿瘤疗效。

近年来,T细胞共抑制受体拮抗剂的出现,如程序性细胞死亡蛋白1 (PD-1)/程序性细胞死亡1配体1 (PD-L1)抗体和细胞毒性T淋巴细胞相关抗原-4 (CTLA-4)抗体,已经彻底改变了癌症治疗领域。遗憾的是,在很高比例的免疫治疗患者中,治疗失败和耐药性是常见的。因此,目前正在评估针对其他免疫调节途径的新方法。这些包括拮抗剂,如共抑制检查点T细胞免疫球蛋白(Ig)结构域和粘蛋白结构域-3和淋巴细胞活化基因3,以及靶向共刺激分子CD40、OX-40、糖皮质激素诱导的肿瘤坏死因子受体和CD137 (4-1BB)的激动剂抗体。
CD137 (4-1BB)属于肿瘤坏死因子(TNF)受体超家族,是一种共刺激分子。它存在于各种活化的免疫细胞类型,包括自然杀伤细胞(NK)、T细胞和树突状细胞(DCs)激活后,CD137通过核因子kB (NF-kB)和丝裂原激活的蛋白激酶途径传递细胞内信号,增强细胞因子产生、细胞增殖、存活和细胞毒性T细胞活性。此外,有大量证据表明,在肿瘤细胞中引入激动剂抗体或CD137配体可以有效地消除肿瘤,这使得CD137成为一个有希望的治疗靶点。
该研究评估了一种激动剂CD137抗体:ADG106。ADG106是一种针对CD137的全人源性单克隆IgG4抗体,靶向CD137独特的交叉反应性抗原表位,适用于不同物种,包括人、猴和小鼠。ADG106具有通过FcGRIIB介导的强交联激活CD137的机制,同时拮抗CD137配体。该研究检测了单药ADG106在晚期实体瘤和NHL患者中的临床前特征、临床安全性、初步抗肿瘤活性、药代动力学和药效学。
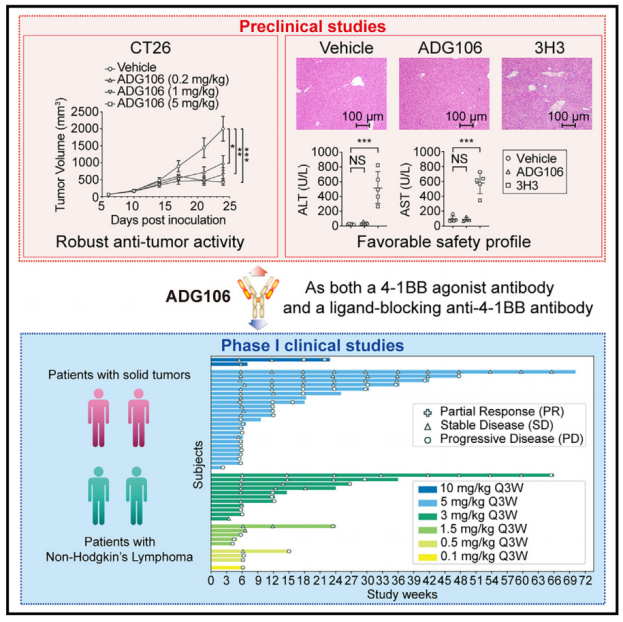
机理模式图(图源自Cell Reports Medicine )
在这项研究中,接受过多种既往治疗的晚期癌症患者中,ADG106在48.4%的患者中显示出更好的单药活性和疾病控制,包括一名鼻咽癌患者的uPR。同样,另一种CD137激动剂utomilumab已进入临床开发,但作为单药治疗,其抗肿瘤活性较弱,在实体瘤患者中的客观缓解率为3.8%。utomilumab和ADG106均表现出CD137受体依赖于FcgR参与的聚类,导致轻度的激动作用,随后的临床疗效较弱。
ADG106的总体安全性优于urelumab和GEN1046。与urelumab不同,ADG106以依赖于FcgR的方式刺激CD137受体,而urelumab独立于FcgR激活CD137受体。因此,ADG106独特的结合表位可能导致其聚集CD137单体或二聚体的效率低于urelumab,这可能是ADG106与urelumab相比相对有利的安全性的原因。综上所述,该研究结果表明ADG106具有良好的安全性和良好的临床疗效。这些发现支持进一步评估ADG106在晚期癌症患者中的作用的必要性。最重要的是,ADG106在TME内的有利调节提供了一种增强的免疫治疗方法。
原文链接:
https://doi.org/10.1016/j.xcrm.2024.101414
作者:iNature
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#实体瘤# #非霍奇金淋巴瘤# #ADG106#
23